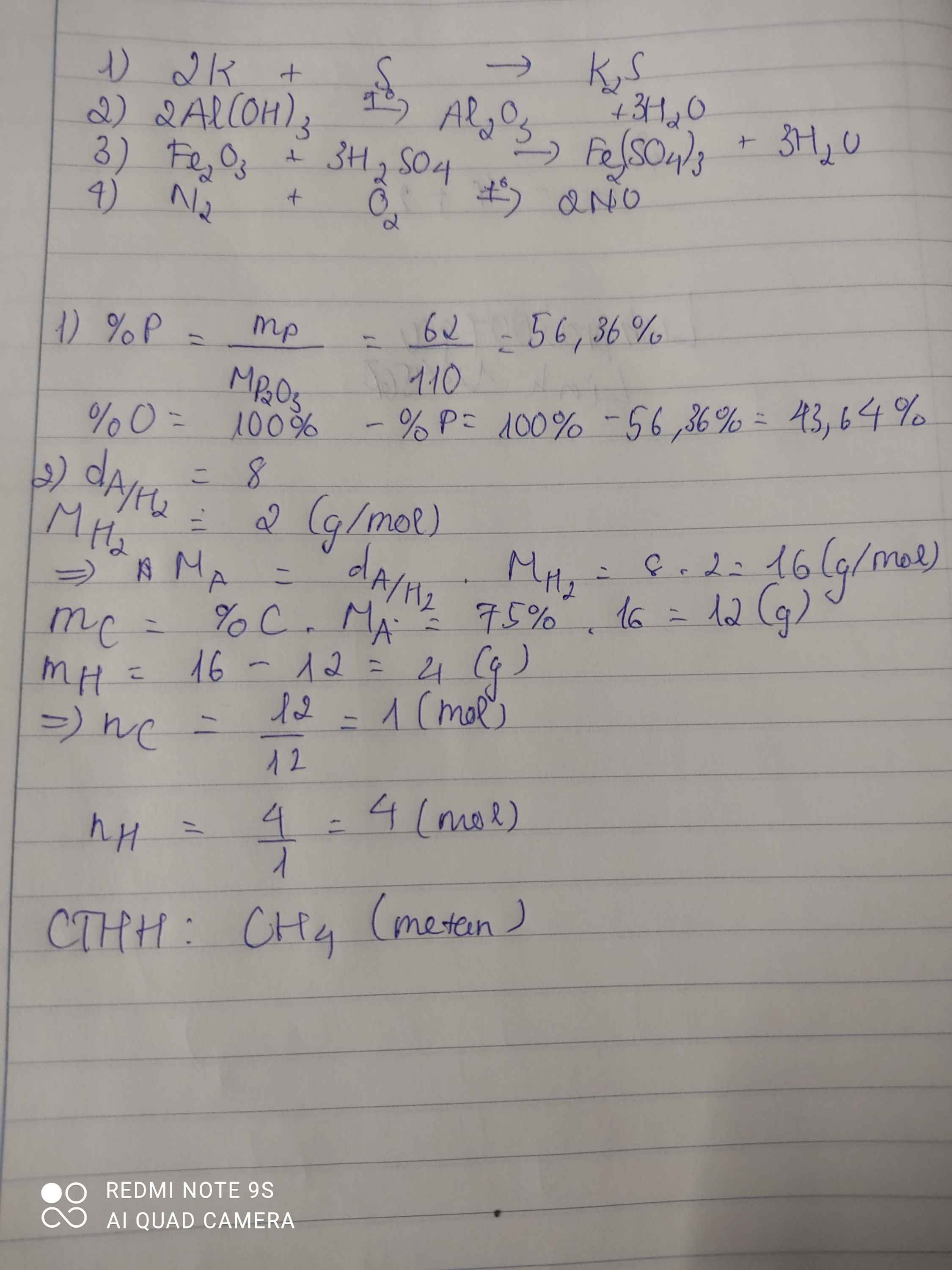Tính thành phần phần trăm theo khối lượng các nguyên tố hoá học có trong hợp chất đường mía (C¹² H²² O¹¹) (giúp mình vs ạhh, mik đang cần gấpp)

Những câu hỏi liên quan
Xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất.Hợp chấtkhối lượng mình mol( M )Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chấtKhối lượng của mỗi nguyên tố có trong 1 mol hợp chấtThành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chấtKMnO4 -Nêu các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất ....
Đọc tiếp
Xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất.
| Hợp chất | khối lượng mình mol( M ) | Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất | Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất | Thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất |
| KMnO4 |
-Nêu các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất .
-Viết công thức tính thành phần phần trăm theo khối lượng của 1 nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất.
Khối lượng mol :
MKMnO4 = 39 + 55 + 64 = 158 (g/mol)
Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất :
nK = 1 mol
nMn = 1 mol
nO = 4 mol
Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất :
mK = 39.1 = 39 (g)
mMn = 55.1 = 55 (g)
mO = 16.4 = 64 (g)
Thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất :
\(\%m_K=\frac{m_K}{M_{KMnO_4}}.100\%=\frac{39}{158}.100\%=24,7\%\)
\(\%m_{Mn}=\frac{m_{Mn}}{M_{KMnO_4}}.100\%=\frac{55}{158}.100\%=34,8\%\)
\(\%m_O=\frac{m_O}{m_{KMnO_4}}.100\%=\frac{64}{158}.100\%=40,5\%\)
Đúng 0
Bình luận (5)
Các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất :
B1 : Tính khối lượng mol (M) của hợp chất.
B2 : Tính số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Tính khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B4 : Tính thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất.
Đúng 0
Bình luận (0)
Công thức tính thành phần phần trăm theo khối lượng của 1 nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất :
\(\%m_A=\frac{m_A}{M_{h\text{/}c}}.100\%\)
Đúng 0
Bình luận (7)
Một hợp chất có công thức hoá học KClO3.Tính thành phần phần trăm theo khối lượng mỗi nguyên tố trong hợp chất(Biết nguyên tử khối của K=39 Cl=35,5 O=16
Ta có CTTH: KClO3
=> Gọi CTTQ là K1Cl1O3
=> \(M_{KClO_3}=122,5\) (g/mol)
\(\%m_K=\dfrac{1
.
39}{122,5}
.
100\%=31,84\%\)
\(\%m_{Cl}=\dfrac{1
.
35,5}{122,5}
.
100\%=28,98\%\)
\(\%m_O=100\%-\left(\%m_K+\%m_{Cl}\right)=100\%-\left(31,84\%+28,98\%\right)=39,18\%\)
Đúng 2
Bình luận (0)
Phần trăm K trong KClO3: \(\%K=\dfrac{39}{39+35,5+16.3}.100=31,84\%\)
Phần trăm Cl trong KClO3: \(\%Cl=\dfrac{35,5}{39+35,5+16.3}.100=28,98\%\)
Phần trăm O trong KClO3: \(\%O=100-31,84-28,98=39,18\%\)
Đúng 1
Bình luận (0)
Chất saccarozơ ( đường kính ) là hợp chất phân tử có 12 nguyên tử C , 22 nguyên tử H và 11 nguyên tử O
a, Tìm phân tử khối của hợp chất saccarozơ
b, Tính thành phần ,phần trăm theo khối lượng của các nguyên tố hóa học trong chất saccarozơ
\(CT:C_{12}H_{22}O_{11}\)
\(M=12\cdot12+22+11\cdot16=342\left(đvc\right)\)
\(\%C=\dfrac{12\cdot12}{342}\cdot100\%=42.1\%\)
\(\%H=\dfrac{22}{342}\cdot100\%=6.43\%\)
\(\%O=51.47\%\)
Đúng 2
Bình luận (0)
a)
PTH = 12.12 + 22 + 16.11 = 342(đvC)
b)
$\%C = \dfrac{12.12}{342}.100\% =42,1\%$
$\%H = \dfrac{22}{342}.100\% = 6,43\%$
$\%O = 100\% -42,1\% -6,43\% = 51,47\%$
Đúng 3
Bình luận (0)
tìm CTHH của hợp chất, biết:a/ khối lượng mol của hợp chất A là 142 gam,thành phần phần trăm theo khối lượng của các nguyên tố: 32,39%Na;22,54%S;45,07%Ob/ khối lượng mol của hợp chất B là 123 gam, thành phần phần trăm theo khối lượng của các nguyên tố: 58,5%C;4,1%H;11,4%N;26%Oc/ hợp chất C có khối lượng mol nặng gấp 23 lần khí hidro, thành phần phần trăm theo khối lượng của các nguyên tố: 52,17%C; 13,05%H; 34,74%O
Đọc tiếp
tìm CTHH của hợp chất, biết:
a/ khối lượng mol của hợp chất A là 142 gam,thành phần phần trăm theo khối lượng của các nguyên tố: 32,39%Na;22,54%S;45,07%O
b/ khối lượng mol của hợp chất B là 123 gam, thành phần phần trăm theo khối lượng của các nguyên tố: 58,5%C;4,1%H;11,4%N;26%O
c/ hợp chất C có khối lượng mol nặng gấp 23 lần khí hidro, thành phần phần trăm theo khối lượng của các nguyên tố: 52,17%C; 13,05%H; 34,74%O
a)
-Đặt công thức: NaxSyOz
x=\(\dfrac{32,29.142}{23.100}\approx2\)
y=\(\dfrac{22,54.142}{32.100}\approx1\)
z=\(\dfrac{45,07.142}{16.100}\approx4\)
-CTHH: Na2SO4
Đúng 1
Bình luận (0)
Câu b này mình giải cách khác câu a:
nC:nH:nN:nO=\(\dfrac{\%C}{12}:\dfrac{\%H}{1}:\dfrac{\%N}{14}:\dfrac{\%O}{16}=\dfrac{58,5}{12}:\dfrac{4,1}{1}:\dfrac{11,4}{14}:\dfrac{26}{16}\)
nC:nH:nN:nO=4,875:4,1:0,81:1,625=6:5:1:2
-Công thức nguyên: (C6H5NO2)n
-Ta có: (12.6+5+14+16.2)n=123\(\Leftrightarrow\)123n=123\(\Leftrightarrow\)n=1
-CTHH: C6H5NO2
Đúng 1
Bình luận (0)
Câu c:
\(M_C=23.2=46đvC\)
nC:nH:nO=\(\dfrac{\%C}{12}:\dfrac{\%H}{1}:\dfrac{\%O}{16}=\dfrac{52,17}{12}:\dfrac{13,05}{1}:\dfrac{34,74}{16}\)
nC:nH:nO=4,3475:13,05:2,17125\(\approx\)2:6:1
-Công thức nguyên: (C2H6O)n
-Ta có: (12.2+6+16)n=46\(\Leftrightarrow\)46n=46\(\Leftrightarrow\)n=1
-CTHH: C2H6O
Đúng 1
Bình luận (0)
1.Tính thành phần phần trăm khối lượng các nguyên tố hoá học có trong hợp chất P2O3 2. Hợp chất A có chứa 75%C và 25%H về khối lượng, biết tỉ khối của A so với khí hiđrô bằng 8. Xác định CTHH của chất A
1
\(MP_2O_3=110g/mol\)
\(\%P=\dfrac{31.2.100}{110}=58,2\%\)
\(\%O=100-58,2=41,8\%\)
2
\(MA=8.2=16g/mol\)
Tính theo hoá trị
=> cthh của A là CH\(_4\)
Đúng 1
Bình luận (1)
Tìm CTHH của một hợp chất khí có thành phần trăm theo khối lượng các nguyên tố như sau : %mc = 80% ; %mh = 20% . Biết tỉ khối của hợp chất so với hiđrô là 15
Giúp mik với mik đang cần gấp =((((
\(M_{hc}=15.M_H=15(g/mol)\)
\(\Rightarrow n_C=\dfrac{15.80\%}{12}=1(mol);n_H=\dfrac{15.20\%}{1}=3(mol)\\ \Rightarrow CTHH:CH_3\)
Đúng 1
Bình luận (1)
Gọi CTHH của hợp chất là: \(\left(C_xH_y\right)_n\)
Ta có: \(M_{\left(C_xH_y\right)_n}=15.1=15\left(\dfrac{g}{mol}\right)\)
Ta lại có: \(\dfrac{x}{y}=\dfrac{\dfrac{80\%}{12}}{\dfrac{20\%}{1}}=\dfrac{1}{3}\Leftrightarrow\left\{{}\begin{matrix}x=1\\y=3\end{matrix}\right.\)
Vậy CTHH của hợp chất là: \(\left(CH_3\right)_n\)
Mà: \(M_{\left(CH_3\right)_n}=\left(12+1.3\right).n=15\left(\dfrac{g}{mol}\right)\)
\(\Leftrightarrow n=1\)
Vậy CTHH của hợp chất là: CH3
Đúng 0
Bình luận (0)
Mhc = 15.2 = 30 (g/mol)
\(m_C=\dfrac{30.80}{100}=24\left(g\right)=>n_C=\dfrac{24}{12}=2\left(mol\right)\)
\(m_H=\dfrac{30.20}{100}=6\left(g\right)=>n_H=\dfrac{6}{1}=6\left(mol\right)\)
=> CTHH: C2H6
Đúng 0
Bình luận (0)
Công thức hoá học của sulfur dioxide là SO2.
a. Hãy cho biết số lượng nguyên tử của mỗi nguyên tố có trong phân tử đó.
b. Tính khối lượng phân tử
c. Tính thành phần phần trăm khối lượng các nguyên tố có trong hợp chất
`#3107.101107`
a. Sửa đề: Hãy cho biết khối lượng nguyên tử của mỗi nguyên tố có trong phân tử đó.
- Trong phân tử \(\text{SO}_2\) gồm 2 nguyên tử, nguyên tử S và O
`=>` NTK của S là `32` amu, NTK của phân tử O là `16` amu
b.
Khối lượng phân tử của SO2 là:
\(32+16\cdot2=64\left(\text{amu}\right)\)
c.
Số `%` của S có trong SO2 là:
\(\text{%S }=\dfrac{32\cdot100}{64}=50\left(\%\right)\)
Số `%` của O2 có trong SO2 là:
\(\text{%O = 100%}-\text{50% = 50%}\)
Vậy:
a. S: `32` amu, O: `16` amu
b. PTK của SO2 là `64` amu
c. \(\text{%S = 50%; %O = 50%.}\)
Đúng 1
Bình luận (0)
xác định công thức hóa học của hợp chất biết khối lượng mol phân tử là 100g, thành phần phần trăm theo khối lượng các nguyên tố là 40% Ca, 12% C và 48%O.
CÁC BẠN GIÚP MK VS
Gọi CTHH là CaxCyOz
Trong hợp chất: mCa = 100.40% = 40 (g) => x = 1
mC = 100.12% = 12 => y = 1
mO =100.48% = 48 => z = 3
=> Hợp chất là CaCO3
Đúng 1
Bình luận (0)
Viết công thức tính thành phần phần trăm theo khối lượng của 1 nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất
Nếu biết công thức của hợp chất ta có thể tính thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất đó theo các bước sau:
- Tính khối lượng mol của hợp chất AxBy:
- Xác định số mol nguyên tử của từng nguyên tố có trong 1 mol hợp chất AxBy.
1 mol AxBy có: x mol nguyên tử A và y mol nguyên tử B.
- Tìm khối lượng các nguyên tố trong 1 mol hợp chất AxBy.
mA=x.MA
mB=y.MB
- Tính phần trăm theo khối lượng của từng nguyên tố theo công thức:
%A= mA .100%= .100%
%B= .mB . 100%= .100%
Hoặc %B=100%-%A
Đúng 0
Bình luận (1)
Theo mình còn có một cách khác có thể giải tất cả dạng bài kiểu này
B1 : Gọi CTHH cần tìm la AxByCz
B2 : Ta có : x: y :z = %A/ MA : %B / MB : %C/ MC = a :b :c
B3 Chọn x=a ; y=b ; z=c
B4 Đưa ra công thức đơn giản AaBbCc
B5 Dựa vào PTK đưa ra CT phân tử
Làm tương tự với các bài hpas chỉ có 2 nguyên tố hóa học
Chúc bạn học tốt nha
Đúng 0
Bình luận (0)