Khử hoàn toàn 16g F e 2 O 3 bằng CO thành Fe và C O 2 Tính khối lượng chất rắn thu được.

Những câu hỏi liên quan
Khử hoàn toàn 27,6 g Fe2O3 và Fe3O4 ở nhiệt đọ cao phải dùng hết 11,2 l khí CO (đktc)
a) Viết các PTPƯ đã xảy ra
b) Tính thành phần % theo số mol và theo khối lượng của mỗi loại oxit sắt trên
c) Tính khối lượng sắt thu được ở mỗi phản ứng
a) Fe2O3 + 3CO \(\rightarrow\) 2Fe + 3CO2 (1)
x 3x 2x
Fe3O4 + 4CO \(\rightarrow\) 3Fe + 4CO2 (2)
y 4y 3y
b) Số mol khí CO = 11,2/22,4 = 0,5 mol. Gọi x, y tương ứng là số mol của hai oxi nói trên. Ta có:
160x + 232y = 27,6 và 3x + 4y = 0,5. Giải hệ thu được x = 0,1 và y = 0,05 mol.
%Fe2O3 = 160.0,1.100/27,6 = 57,97%; %Fe3O4 = 100 - 57,97 = 42,03 %.
c) Khối lượng Fe ở p.ư (1) = 56.2.0,1 = 11,2 g; ở p.ư (2) = 56.3.0,05 = 8,4 g.
Đúng 1
Bình luận (0)
có thể giải theo bảo toàn nguyên tố nhanh hơn thì phải
gọi số mol lần lượt là x,y (mol)
Hệ : (2x+3y) x 56 +(3x+4y)x16=27,6
3x+4y= 0,5
Đúng 0
Bình luận (0)
Khử 16g Fe2O3 bằng khí CO sau phản ứng thu đc chất rắn gồm 4 chất, sản phẩm khí thu đc cho đi vào bình đựng dd Ca(OH)2 dư thu đc a gam kết tủa. Giá trị của a là?
Khử hòa tan 16g Fe2O3 bằng khí H2
Kim loại thu được cho vào 600g HCl 3,65%.Tìm C% của dd thu được
Fe2O3 + 3H2 \(\rightarrow\)2Fe + 3H2O (1)
Fe + 2HCl\(\rightarrow\)FeCl2 + H2 (2)
nFe2O3=\(\dfrac{16}{160}=0,1\left(mol\right)\)
mHCl=\(600.\dfrac{3,65}{100}=21,9\left(g\right)\)
nHCl=\(\dfrac{21,9}{36,5}=0,6\left(mol\right)\)
Theo PTHH 1 ta có:
2nFe2O3=nFe=0,2(mol)
Vì 0,2.2<0,6 nên HCl dư 0,2mol,Fe hết
Theo PTHH 2 ta có:
nFe=nFeCl2=0,2(mol)
mFeCl2=127.0,2=25,4(g)
mHCl=36,5.0,2=7,3(g)
C% dd FeCl2=\(\dfrac{25,4}{11,2+600-0,2.2}.100\%=4,1\%\)
C% dd HCl=\(\dfrac{7,3}{11,2+600-0,2.2}.100\%=1,19\%\)
Đúng 0
Bình luận (0)
Tính thể tích khí CO (ở đktc) cần dùng để khử hoàn toàn 16g bột \(Fe_2O_3\) thành Fe.
Help me!!!
\(PTHH:Fe_2O_3+3CO\overset{t^o}{--->}3CO_2+2Fe\)
Ta có: \(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
Theo PT: \(n_{CO}=3.n_{Fe_2O_3}=3.0,1=0,3\left(mol\right)\)
\(\Rightarrow V_{CO}=0,3.22,4=6,72\left(lít\right)\)
Đúng 3
Bình luận (1)
Khử hoàn toàn 16g hh Fe2O3 và CuO bằng khí CO dư . Cho toàn bộ kim loại thu được hòa tan vào dd HCl dư thấy thoát ra 2,24l khí H2 (đktc) . Xác định thành phần % theo khối lượng mỗi oxit trong hh ban đầu .
Fe2O3 + 3CO ----> 2Fe + 3CO2
0,05 0,1 (mol)
CuO + CO ----> Cu + CO2
Fe + 2HCl ----> FeCl2 + H2
0,1 0,1 (mol)
=> mFe2O3 = 0,05.160 = 8 (g)
=> %Fe2O3 = \(\dfrac{8.100}{16}\)= 50%
=> %CuO = 100 - 50 = 50%
Đúng 0
Bình luận (0)
Hoàn thành PT phản ứng hóa học sau và cho biết những phản ứng nào là phản ứng õi hóa khử
a) Mg+CO2--------> MgO+C
b) Fe3O4+CO--------> Fe+CO2
c) FexOy+Al---------> Fe+Al2O3
d) KMnO4----------> K2MnO4+MnO2+O2
a) 2Mg + CO2 -----------> 2MgO + C .Đây là phản ứng oxi hóa khử
b) 2Fe3O4 +8CO--------->6Fe +8CO2 .Đây là phản ứng oxi hóa khử
c) 3FexOy + 2yAl ----------->3xFe +yAl2O3 .Đây là phản ứng oxi hóa khử
d) 2KMnO4 ------------> K2MnO4 + MnO2 + O2. Đây là phản ứng oxi hóa khử
Đúng 0
Bình luận (1)
1. Cho 6,96 hỗn hợp A gồm FeO, Fe2O3, Fe3O4 Khử hoàn toàn hỗn hợp trên bằng khí CO thu được 5,04 gam Fe. Tính thể tích dung dịch HCl 1M cần dùng để phản ứng vừa đủ với 6,96 gam hỗn hợp trên.
Khử 16 gam sắt (III) oxit F*e_{2} * O_{3} bằng 13,44 lít khí hiđro ở đktc tạo thành sắt và hơi
nước.
a/ Viết phản ứng.
b/ Tính khối lượng sắt tạo thành?
C/ Cần dùng thêm bao nhiêu gam CuO nữa d hat e tác dụng hết lượng chất dư ở trên?
Cho biết: Fe = 56 O = 16 , H = I , Cu=56.
a.b.\(n_{Fe_2O_3}=\dfrac{m_{Fe_2O_3}}{M_{Fe_2O_3}}=\dfrac{16}{160}=0,1mol\)
\(n_{H_2}=\dfrac{V_{H_2}}{22,4}=\dfrac{13,44}{22,4}=0,6mol\)
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,1 < 0,6 ( mol )
0,1 0,3 0,2 ( mol )
\(m_{Fe}=n_{Fe}.M_{Fe}=0,2.56=11,2g\)
c.\(n_{H_2}=0,6-0,3=0,3mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,3 0,3 ( mol )
\(m_{CuO}=n_{CuO}.M_{CuO}=0,3.80=24g\)
Đúng 3
Bình luận (0)
Để khử hoàn toàn 17,6 gam hỗn hợp gồm Fe, FeO, Fe3O4, Fe2O3 đến Fe thì cần đủ 2,24 lít CO (đktc). Khối lượng sắt thu được là :
A. 15g
B. 16g
C. 17g
D. 18g
nCO = 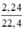 = 0,1 mol
= 0,1 mol
BT nguyên tố C ⇒ nCO2 = nCO = 0,1 mol
BT khối lượng: mhỗn hợp + mCO = mFe + mCO2
⇒ mFe = 17,6 + 0,1. 28 – 0,1. 44 = 16g
Đáp án B
Đúng 0
Bình luận (0)






















