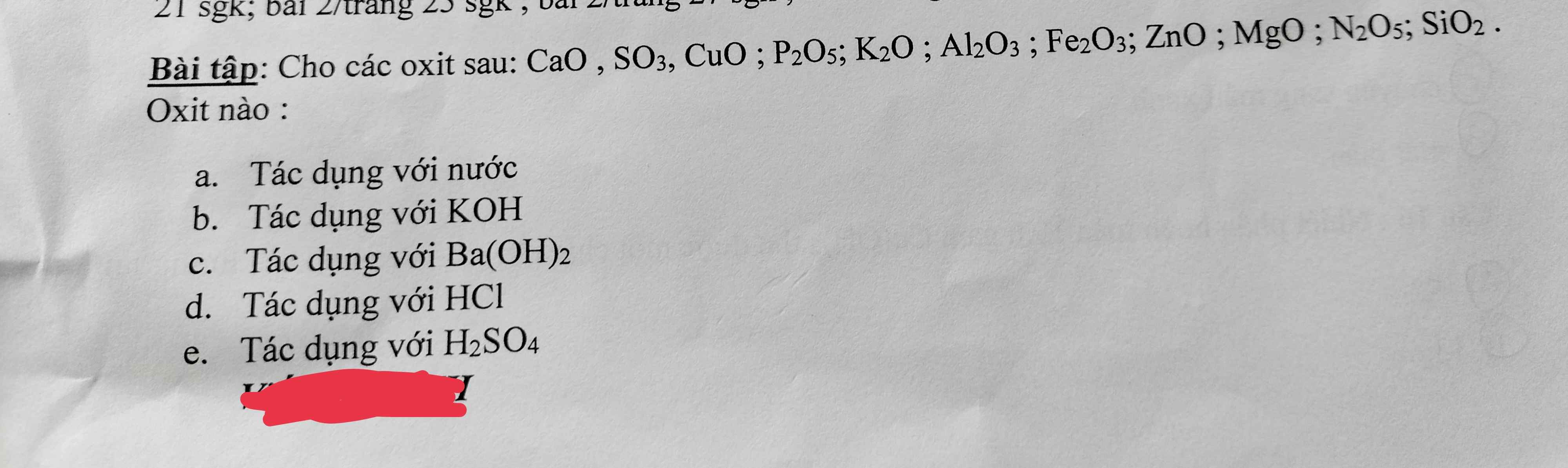cho 20 g Fe2O3 tác dụng với dung dịch H2SO4 có nồng độ 25%.sau phản ứng thu được dung dịch B. a). viết phương trình hóa học b). tính khối lượng H2SO4 đã tham gia phản ứng c). tính nồng độ phần trăm chất có trong dung dịch B
Đề kiểm tra 1 tiết chương I: Oxit-Axit -Đề 2
\(n_{Fe_2O_3}=\dfrac{20}{160}=0,125\left(mol\right)\)
PTHH:
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
0,125 0,375 0,125 0,375
\(m_{ddH_2SO_4}=\dfrac{0,375.98.100}{25}=147\left(g\right)\)
\(C\%_{Fe_2\left(SO_4\right)_3}=\dfrac{0,125.406}{20+147}\approx30,39\%\)
Đúng 2
Bình luận (0)
Giải giúp mình câu 4 với câu 5 ạ , cảm ơn rất nhiều 
Câu 4:
Cho giấy quỳ tím vào từng dung dịch:
nếu quỳ tím đổi màu thì là h2so4 và hcl
lọ còn lại là naOH, dán nhãn.
Nhỏ từ từ dung dịch Bacl2 vào từng dung dịch nếu có chất kết tủa màu trắng thì là h2so4, dán nhãn.
pthh: h2so4 + bacl2 -> 2hcl + baso4
lọ còn lại là hcl không phản ứng dán nhãn.
Đúng 1
Bình luận (0)
PT: \(MgO+2HCl\rightarrow MgCl_2+H_2O\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
Gọi: nH2O = x (mol)
Theo PT: \(n_{HCl}=2n_{H_2O}=2x\left(mol\right)\)
Theo ĐLBT KL, có: m oxit + mHCl = mmuối + mH2O
\(\Rightarrow12,2+2x.36,5=31,45+18x\)
⇒ x = 0,35 (mol)
⇒ nHCl (pư) = 0,35.2 = 0,7 (mol)
Ta có: \(n_{NaOH}=0,02.2=0,04\left(mol\right)\)
PT: \(NaOH+HCl_{\left(dư\right)}\rightarrow NaCl+H_2O\)
____0,04____0,04 (mol)
⇒ nHCl = 0,7 + 0,04 = 0,74 (mol)
\(\Rightarrow m_{ddHCl}=\dfrac{0,74.36,5}{20\%}=135,05\left(g\right)\)
Đúng 2
Bình luận (0)
quá trình sản xuất phân bón kép
nêu vai trò của phân bón kép
Câu 2: Cho 8g MgO tác dụng với 200 g dung dịch HCL 18,25%.
a. Viết PTHH
b. Tính nồng độ % của các chất có trong dung dịch sau phản ứng.
a) \(\left\{{}\begin{matrix}n_{MgO}=\dfrac{8}{40}=0,2\left(mol\right)\\n_{HCl}=\dfrac{200.18,25\%}{36,5}=1\left(mol\right)\end{matrix}\right.\)
PTHH: MgO + 2HCl ---> MgCl2 + H2O
bđ 0,2 1
pư 0,2---->0,4
sau pư 0 0,6 0,2
b) \(\left\{{}\begin{matrix}C\%_{MgCl_2}=\dfrac{0,2.95}{200+8}.100\%=9,13\%\\C\%_{HCl\left(dư\right)}=\dfrac{0,8.36,5}{200+8}.100\%=14,04\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
\(n_{MgO}=\dfrac{8}{40}=0,2\left(mol\right)\) \(n_{HCl}=\dfrac{200\times18,25}{100\times36,5}=1\left(mol\right)\)
PT: \(MgO+2HCl\rightarrow MgCl_2+H_2O\)
0,2 0,4 0,2 (mol)
TL: \(\dfrac{0,2}{1}\) < \(\dfrac{1}{2}\) \(\Rightarrow\) HCl dư
\(C\%_{HCl\left(dư\right)}=\dfrac{\left(1-0,4\right)\times36,5\times100}{8+200}\approx10,5\%\)
\(C\%_{MgCl_2}=\dfrac{0,2\times95\times100}{8+200}\approx9,13\%\)
Đúng 0
Bình luận (0)
a)
`CaO + H_2O -> Ca(OH)_2`
`SO_3 + H_2O -> H_2SO_4`
`P_2O_5 + 3H_2O -> 2H_3PO_4`
`K_2O + H_2O -> 2KOH
`N_2O_5 + H_2O -> 2HNO_3`
b)
`SO_3 + 2KOH -> K_2SO_4 + H_2O`
`P_2O_5 + 6KOH -> 2K_3PO_4 + 3H_2O`
`Al_2O_3 + 2KOH -> 2KAlO_2 + H_2O`
`ZnO + 2KOH -> K_2ZnO_2 + H_2O`
`N_2O_5 + 2KOH -> 2KNO_3 + H_2O`
`SiO_2 + 2KOH_{đ} -> K_2SiO_3 + H_2O`
c)
`SO_3 + Ba(OH)_2 -> BaSO_4 + H_2O`
`P_2O_5 + 3Ba(OH)_2 -> Ba_3(PO_4)_2 + 3H_2O`
`Al_2O_3 + Ba(OH)_2 -> Ba(AlO_2)_2 + H_2O`
`ZnO + Ba(OH)_2 -> BaZnO_2 + H_2O`
`N_2O_5 + Ba(OH)_2 -> Ba(NO_3)_2 + H_2O`
`SiO_2 + Ba(OH)_2_{đ} -> BaSiO_3 + H_2O`
d)
`CaO + 2HCl -> CaCl_2 + H_2O`
`CuO + 2HCl -> CuCl_2 + H_2O`
`K_2O + 2HCl -> 2KCl + H_2O`
`Al_2O_3 + 6HCl -> 2AlCl_3 + 3H_2O`
`Fe_2O_3 + 6HCl -> 2FeCl_3 + 3H_2O`
`ZnO + 2HCl -> ZnCl_2 + H_2O`
`MgO + 2HCl -> MgCl_2 + H_2O`
e)
`CaO + H_2SO_4 -> CaSO_4 + H_2O`
`CuO + H_2SO_4 -> CuSO_4 + H_2O`
`K_2O + H_2SO_4 -> K_2SO_4 + H_2O`
`Al_2O_3 + 3H_2SO_4 -> Al_2(SO_4)_3 + 3H_2O`
`Fe_2O_3 + 3H_2SO_4 -> Fe_2(SO_4)_3 + 3H_2O`
`ZnO + H_2SO_4 -> ZnSO_4 + H_2O`
`MgO + H_2SO_4 -> MgSO_4 + H_2O`
Đúng 1
Bình luận (0)
Hoàn thành sơ đồ phản ứng, ghi rõ điều kiện nếu có:
S ---> SO2 ---> SO3 ----> H2SO4 ---> MgSO4
S+O2->SO2
2SO2+O2->2SO3
SO3+H2O->H2SO4
H2SO4+MG->MGSO4+H2
Đúng 1
Bình luận (0)
Mọi người cho e hỏi là: Các muối HCO3 và muối HSO3 có tác dụng với các Axit, bazo và muối ở điều kiện thường được ko ạ, hay phải cần nhiệt độ cao
Các muối HCO3 và HSO3 là muối có tính lưỡng tính nên có thể tác dụng với cả Axit và Bazo ở nhiệt độ thường, không cần điều kiện. Còn tác dụng với muối, sản phẩm sau phản ứng phải có kết tủa, khí hoặc nước.
Đúng 0
Bình luận (0)
Viêt các phương trình phản ứng xảy ra?
A, nhôm và dd đồng clorua B, Nhôm và dd Magie clorua
C, Nhôm sunfat và Magie D, Nhôm hiddroxit và axitsunfuric
a) Pt : \(2Al+3CuCl_2\rightarrow2AlCl_3+3Cu\)
b) Pt : phản ứng không xảy ra
c) Pt : \(Al_2\left(SO_4\right)_3+3Mg\rightarrow3MgSO_4+2Al\)
d) Pt : \(2Al\left(OH\right)_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+6H_2O\)
Chúc bạn học tốt
Đúng 5
Bình luận (0)
Các phản ứng xảy ra: a;cd
a)\(2Al+3CuSO_4\rightarrow Al_2\left(SO_4\right)_3+3Cu\)
c)\(Al_2\left(SO_4\right)_3+3Mg\rightarrow3MgSO_4+2Al\)
d)\(2Al\left(OH\right)_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+6H_2O\)
Đúng 2
Bình luận (0)
\(a,2Al+3CuCl_2\rightarrow2AlCl_3+3Cu\\ b,Al+MgCl_2\rightarrow\times\\ c,Al_2\left(SO_4\right)_3+3Mg\rightarrow2Al+3MgSO_4\\ d,2Al\left(OH\right)_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+6H_2O\)
Đúng 1
Bình luận (0)