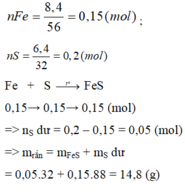Những câu hỏi liên quan
Đốt cháy 3,2 gam lưu huỳnh cháy trong không khí thu được 6,4 gam lưu huỳnh đioxit SO2. Tính khối lượng oxi đã tham gia phản ứng? Biết lưu huỳnh cháy là tham gia phản ứng với khí oxi.
Định luật bảo toàn khối lượng :
\(m_S+m_{O2}=m_{SO2}\)
3,2 + \(m_{O2}\) = 6,4
⇒ \(m_{O2}=6,4-3,2=3,2\left(g\right)\)
Chúc bạn học tốt
Đúng 2
Bình luận (0)
\(BTKL: \\ m_S+m_{O_2}=m_{SO_2}\\ 3,2+m_{O_2}=6,4\\ m_{O_2}=6,4-3,2=3,1(g)\)
Đúng 0
Bình luận (1)
Cho 8,4 gam sắt tác dụng với 6,4 gam lưu huỳnh trong bình chân không sau phản ứng thu được m gam chất rắn. Giá trị của m là
A. 11,0.
B. 13,2.
C. 17,6.
D. 14,8
Đáp án D
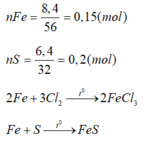
0,15→ 0,15→ 0,15 (mol)
=> nS dư = 0,2 – 0,15 = 0,05 (mol)
=> mrắn = mFeS + mS dư = 0,05.32 + 0,15.88 = 14,8 (g)
Đúng 0
Bình luận (0)
Cho 8,4 gam sắt tác dụng với 6,4 gam lưu huỳnh trong bình chân không sau phản ứng thu được m gam chất rắn. Giá trị của m là
A. 11,0.
B. 13,2.
C. 17,6.
D. 14,8.
Bài 5: Đốt cháy 6,4 gam lưu huỳnh trong bình chứa khí oxi tạo thành Lưu huỳnh đioxit (SO2).
a. Viết phương trình hóa học
b. Tính khối lượng chất tạo thành
c. Tính thể tích khí oxi tham gia phản ứng ở đktc
a, \(n_S=\dfrac{6,4}{32}=0,2\left(mol\right)\)
PTHH: S + O2 ----to----> SO2
Mol: 0,2 0,2 0,2
b, \(m_{SO_2}=0,2.64=12,8\left(g\right)\)
c, \(V_{O_2}=0,2.22,4=4,48\left(l\right)\)
Đúng 3
Bình luận (0)
đốt 5g lưu huỳnh trong bình chứa 6,4g oxi, thu đc m gam SO2. Gía trị của m là?
A.5
B.5,7
C.10
D.11,4
em có làm rồi nhưng ra kết quả sai mong mng làm lại giúp em ạ
\(n_S=\dfrac{5}{32}=0,15625\left(mol\right)\)
\(n_{O_2}=\dfrac{6.4}{32}=0,2\left(mol\right)\)
Ta thấy : 0,15625 < 0,2 => S đủ , O2 dư
PTHH : S + O2 --to--> SO2
0,15625 0,15625
\(m_{SO_2}=0,15625.64=10\left(g\right)\)
Đúng 2
Bình luận (9)
Người ta đốt cháy lưu huỳnh trong bình chứa 15 gam oxi. Sau phản ứng thu được 19,2 gam khí sunfurơ (SO2)
a. Tính số gam lưu huỳnh đã cháy
b. Tính số gam oxi còn dư sau phản ứng cháy
Bài làm
S + O2 ---to---> SO2
a) nSO2 = 19,2 : ( 32 + 32 ) = 0,3 ( mol )
Theo phương trình nS = nSO2 = 0,3 mol
=> mS = 0,3 . 32 = 9,6 ( g )
b) nO2 = 15 : 32 = 0,46875 ( mol )
Xét tỉ lệ: \(\frac{n_{O2}}{1}=0,46875>\frac{n_S}{1}=0,3\)
=> O2 dư, S hết.
=> Bài toán tính theo S.
Theo phương trình:
nO2 = nS = 0,3 ( mol )
=> nO2 sau phản ứng = nO2 ban đầu - nO2 vừa tìm được
Hay nO2 sau phản ứng = 0,46875 - 0,3 = 0,16875 ( mol )
=> mO2 sau phản ứng = 0,16875 . 32 = 5,4 ( g )
# Học tốt #
a) \(PT:S+O_2\rightarrow SO_2\)
\(n_{SO_2}=\frac{m}{M}=\frac{19,2}{64}=0,3\)
\(\)Theo pt: \(n_S=n_{SO_2}=0,3\)
\(\Rightarrow m_s=0,3.32=9,6\)
b, Ta có: \(n_{O_2}=\frac{m}{M}=\frac{15}{32}=0,46875\)
Theo pt: \(n_{O_{2\left(pư\right)}}=n_S=0,3\)
\(\Rightarrow n_{O_{2\left(dư\right)}}=n_{O_2}-n_{O_{2\left(pư\right)}}=0,4875-0,3=0,1875\)
\(\Rightarrow m_{O_{2\left(dư\right)}}=n_{O_{2\left(dư\right)}}.M_{O_2}=0,1875.32=6\)
nO=\(\frac{15}{32}\)= 0,4
nSO2= \(\frac{19,2}{64}=0,3\)
PTHH : S + O2 = SO2
Đề bài 0,4 0,3
Tỉ lệ 0,3 0,3
a, mS = 0,3.32=9,6g
Số gam õi còn dư là 0,4 - 0,3 = 0,1 gam
Xem thêm câu trả lời
Bài 11: Đốt cháy 6,4 gam lưu huỳnh trong bình chứa 16 gam khí oxi tạo thành Lưu huỳnh đioxit
a) Lưu huỳnh hay oxi chất nào còn dư và số mol chất còn dư là bao nhiêu?
b) Chất nào được tạo thành? Khối lượng là bao nhiêu?
\(n_S=\dfrac{6,4}{32}=0,2mol\)
\(n_{O_2}=\dfrac{16}{32}=0,5mol\)
\(S+O_2\underrightarrow{t^o}SO_2\)
0,2 0,5 0,2
Sau phản ứng oxi còn dư và dư \(0,5-0,2=0,3mol\)
Oxit axit được tạo thành là \(SO_2\) và có khối lượng:
\(m_{SO_2}=0,2\cdot64=12,8g\)
Đúng 2
Bình luận (0)
1 Đốt cháy mgam cacbon cần 16,5 gam oxi thì thu được 22, 5 gam khí Cacbônic Tính m
2 đốt cháy 3,2 g lưu huỳnh trong ko khía thu đc 6,4 g lưu huỳnh đioxit . Tính khối lượng của Ỗi đã phản ứng
1)
C+O2\(\overset{t^0}{\rightarrow}CO_2\)
-Áp dụng định luật bảo toàn khối lượng:
\(m_C+m_{O_2}=m_{CO_2}\rightarrow m_C=m_{CO_2}-m_{O_2}=22,5-16,5=6gam\)
2)
S+O2\(\overset{t^0}{\rightarrow}SO_2\)
-Áp dụng định luật bảo toàn khối lượng:
\(m_S+m_{O_2}=m_{SO_2}\rightarrow m_{O_2}=m_{SO_2}-m_S=6,4-3,2=3,2gam\)
Đúng 0
Bình luận (0)
người ta đốt cháy lưu huỳnh trong bình chứa 15g oxi.. sau pư thu đc 19,2g khí sunfurơ (SO2)
a) Tính số gam lưu huỳnh đã cháy
b) Tính số gam oxi còn dư sau phản ứng cháy
b)
\(n_{O_2}=\dfrac{15}{32}=0.46875\left(mol\right)\)
\(n_{SO_2}=\dfrac{19.2}{64}=0.3\left(mol\right)\)
\(S+O_2\underrightarrow{t^0}SO_2\)
\(0.3...0.3....0.3\)
\(m_S=0.3\cdot32=9.6\left(g\right)\)
\(m_{O_2\left(dư\right)}=\left(0.46875-0.3\right)\cdot32=5.4\left(g\right)\)
Đúng 2
Bình luận (0)
Bài 3: Đốt cháy m(g) cacbon (C) cần 16 g oxi thì thu được 22 gam khí cacbonic (CO2).
a/ Lập phương trình khối lượng cho quá trình trên.
b/Tính m
Bài 4. Đốt cháy 3,2 g lưu huỳnh ( S) trong không khí thu được 6,4 g lưu huỳnh đioxit(SO2).
a/ Lập phương trình khối lượng cho quá trình trên.
b/ Tính khối lượng của oxi(O2) đã phản ứng
Bài 3:
\(a,m_C+m_{O_2}=m_{CO_2}\\ b,m=22-16=6\left(g\right)\)
Bài 4:
\(a,m_S+m_{O_2}=m_{SO_2}\\ b,m_{O_2}=6,4-3,2=3,2\left(g\right)\)
Đúng 3
Bình luận (0)
bài 3:
a) Lập phương trình: C + O2 -> CO2
b) Do: Trong một phản ứng hóa học, tổng khối lượng của các chất tham gia phản ứng bằng tổng khối lượng chất sản phẩm
=> m + 16 = 22 (g)
=> m = 22-16= 6 g
Vậy m bằng 6g.
Bài 4 giải tương tự
Đúng 0
Bình luận (0)