dung dịch axit làm giấy quỳ tím chuyển thành màu:
A. Đỏ
B. Xanh
C. Vàng
D. Không đổi màu
Dung dịch tạo thành khi nước hoá hợp với Na2O sẽ làm quỳ tím chuyển sang màu gì?
A. Đỏ
B. Xanh
C. Vàng
D. Không đổi
\(Na_2O+2H_2O->2NaOH\)
Vì là một bazo nên quỳ tím sẽ chuyển sang màu xanh
=>B
\(Na_2O+H_2O\rightarrow2NaOH\)
NaOH là bazo (kiềm) nên làm quỳ tím hoá xanh, làm dd phenolphtalein hoá hồng
Dung dịch tạo thành khi nước hoá hợp với CO2 sẽ làm quỳ tím chuyển sang màu gì?
A. Đỏ
B. Xanh
C. Vàng
D. Không đổi
\(CO_2+H_2O->H_2CO_3\)
vì là một axit nên quỳ tím sẽ hóa đỏ
=>A
\(CO_2+H_2O⇌H_2CO_3\)
Vì H2CO3 là axit yếu nên sẽ làm quỳ tím hoá đỏ nhạt
=> Chọn A
Câu 1 Oxit bazo;
a. CaO, Fe2O3, CuO, MgO
b. Mn2O7, SiO2, NO, ZnO
c. Fe2O3, CO, Al2O3, P2O5
d. Fe2O3, ZnO, CO, P2O5
Câu 2: Dung dịch axit tác dụng với chất chỉ thị màu, làm quỳ tím:
a. Hoá đỏ
b. Hoá xanh
c. Không đổi màu
d. Kết quả khác
Câu 3: Có những chất khí sau: CO2, H2, O2, CO. Khí nào làm đục nước vôi trong (Ca(OH)2):
a. CO2, H2S
b. CO2, CO, H2
c. CO2
d. CO2, O2, CO
Câu 4: Axit sunfuric được sản xuất theo quy trình sau:
S + X ➜ Y
Y + X ➜ Z
Z + H2O ➜ H2SO4
X, Y, Z lần lượt là:
a. SO2, H2, O2 c. H2, O2, SO2
b. O2, SO2, SO3 d. SO2, SO3, O2
Câu 5: Hợp chất nào sau đây là bazo:
a. Canxi nitrat c. Đồng(III) sunfat
b. Natri clorua d. Sắt(III) hidroxit
Câu 6: Khi cho 64g KOH tác dụng với 22,5g HNO3, kết quả là:
a. Dư kiềm c. Trung hoà hoàn toàn
b. Dư axit d. Tất cả đều đúng
Câu 7: Trung hoà 80ml dung dịch H2SO4, 1M bằng dung dịch NaOh 40%. Khối lượng dung dịch NaOH cần dùng là:
a. 10g c. 9g
b. 8g d. Kết quả khác
Câu 8: Oxit nào sau đây tác dụng với NaOH và H2SO4:
a. CO c. Fe2O3
b. Al2O3 d. SO2
Câu 1 Oxit bazo;
a. CaO, Fe2O3, CuO, MgO
b. Mn2O7, SiO2, NO, ZnO
c. Fe2O3, CO, Al2O3, P2O5
d. Fe2O3, ZnO, CO, P2O5
Câu 2: Dung dịch axit tác dụng với chất chỉ thị màu, làm quỳ tím:
a. Hoá đỏ
b. Hoá xanh
c. Không đổi màu
d. Kết quả khác
Câu 3: Có những chất khí sau: CO2, H2, O2, CO. Khí nào làm đục nước vôi trong (Ca(OH)2):
a. CO2, H2S
b. CO2, CO, H2
c. CO2
d. CO2, O2, CO
Câu 4: Axit sunfuric được sản xuất theo quy trình sau:
S + X ➜ Y
Y + X ➜ Z
Z + H2O ➜ H2SO4
X, Y, Z lần lượt là:
a. SO2, H2, O2 c. H2, O2, SO2
b. O2, SO2, SO3 d. SO2, SO3, O2
Câu 5: Hợp chất nào sau đây là bazo:
a. Canxi nitrat c. Đồng(III) sunfat
b. Natri clorua d. Sắt(III) hidroxit
Câu 6: Khi cho 64g KOH tác dụng với 22,5g HNO3, kết quả là:
a. Dư kiềm c. Trung hoà hoàn toàn
b. Dư axit d. Tất cả đều đúng
Câu 7: Trung hoà 80ml dung dịch H2SO4, 1M bằng dung dịch NaOh 40%. Khối lượng dung dịch NaOH cần dùng là:
a. 10g c. 9g
b. 8g d. Kết quả khác
Câu 8: Oxit nào sau đây tác dụng với NaOH và H2SO4:
a. CO c. Fe2O3
b. Al2O3 d. SO2
. Nhúng mẩu giấy quỳ tím vào sản phẩm của phản ứng giữa Zn và dung dịch axit clohiđric lấy dư, khi đó quỳ tím chuyển màu gì?
A. Màu xanh B. Màu đỏ C. Không đổi màu
Nếu rót 300 ml dung dịch Ca(OH)2 1M vào ống nghiệm đựng 100 ml dung dịch H2SO4 1M thì dung dịch sau phản ứng sẽ làm giấy quì tím biến đổi như thế nào?
A. Làm quỳ tím chuyển đỏ.
B. Làm quỳ tím chuyển xanh.
C. Làm dung dịch phenolphtalein không màu chuyển đỏ.
D. Không làm thay đổi màu quỳ tím.
Nếu rót 300 ml dung dịch Ca(OH)2 1M vào ống nghiệm đựng 100 ml dung dịch H2SO4 1M thì dung dịch sau phản ứng sẽ làm giấy quì tím biến đổi như thế nào?
A. Làm quỳ tím chuyển đỏ.
B. Làm quỳ tím chuyển xanh.
C. Làm dung dịch phenolphtalein không màu chuyển đỏ.
D. Không làm thay đổi màu quỳ tím.
Cho 10,0 ml dung dịch NaOH 0,1M vào cốc đựng 15,0 ml dung dịch HCl 0,1M. Dung dịch tạo thành sẽ làm cho
A. phenolphtalein không màu chuyển thành màu hồng. C. giấy quỳ tím hóa đỏ.
B. phenolphtalein không màu chuyển thành màu xanh. D. giấy quỳ tím không chuyển màu.
\(n_{OH^-}=0,01.0,1=0,001\left(mol\right)\)
\(n_{H^+}=0,015.0,1=0,0015\left(mol\right)\)
\(\Rightarrow n_{H^+dư}=0,0005\left(mol\right)\)
\(\Rightarrow\left[H^+\right]=\dfrac{0,0005}{0,01+0,015}=0,02\left(mol\right)\)
\(\Rightarrow pH\approx1,7\)
\(\Rightarrow\) Quỳ tím hóa đỏ.
Câu 33: Khi cho quỳ tím vào dung dịch axit, quỳ tím chuyển màu gì:
A. Đỏ B. Xanh
C. Tím D. Không màu
Câu 34: Kim loai tác dụng với nước ở nhiệt độ thường là:
A. Fe, Mg, Al B. Fe, Cu, Ag
C. Zn, Al, Ag D. Li, Na, K
Câu 35: Điện phân hoàn toàn 2 lít nước ở trạng thái lỏng (biết khối lượng riêng của nước là 1kg/l). Thể tích khí hidro và thể tích khí oxi thu được ở đktc là:
A. 1244,4 lít và 622,2 lít B. 3733,2 lít và 1866,6 lít
C. 4977,6 lít và 2488,8 lít D. 2488,8 lít và 1244,4 lít
Câu 36: Cho mẩu Na vào nước thấy có 4,48 lít khí bay lên. Tính khối lượng Na
A.9,2 g B. 4,6g C. 2g D. 9,6g
Câu 37: Đốt hoàn toàn 2 mol khí H2 thì thể tích O2 cần dùng ở đktc là bao nhiêu lít?
A. 22,4 lít B. 11,2 lít C. 44,8 lít D. 8,96 lít
Câu 33: Khi cho quỳ tím vào dung dịch axit, quỳ tím chuyển màu gì:
A. Đỏ B. Xanh
C. Tím D. Không màu
Câu 34: Kim loai tác dụng với nước ở nhiệt độ thường là:
A. Fe, Mg, Al B. Fe, Cu, Ag
C. Zn, Al, Ag D. Li, Na, K
Câu 35: Điện phân hoàn toàn 2 lít nước ở trạng thái lỏng (biết khối lượng riêng của nước là 1kg/l). Thể tích khí hidro và thể tích khí oxi thu được ở đktc là:
A. 1244,4 lít và 622,2 lít B. 3733,2 lít và 1866,6 lít
C. 4977,6 lít và 2488,8 lít D. 2488,8 lít và 1244,4 lít
Giải thích:
\(2H_2O\underrightarrow{đp}2H_2+O_2\)
\(\dfrac{1}{9}\) --->\(\dfrac{1}{9}\)------>\(\dfrac{1}{18}\)
\(n_{H_2O}=\dfrac{2000}{18}=\dfrac{1000}{9}\left(mol\right)\)
\(V_{H_2}=\dfrac{1000}{9}.22,4=2488,89\left(l\right)\\ V_{O_2}=\dfrac{1000}{18}.22,4=1244,44\left(l\right)\)
Câu 36: Cho mẩu Na vào nước thấy có 4,48 lít khí bay lên. Tính khối lượng Na
A.9,2 g B. 4,6g C. 2g D. 9,6g
Giải thích:
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
0,4<---------------------------0,2
\(n_{Na}=0,4.23=9,2\left(g\right)\)
Câu 37: Đốt hoàn toàn 2 mol khí H2 thì thể tích O2 cần dùng ở đktc là bao nhiêu lít?
A. 22,4 lít B. 11,2 lít C. 44,8 lít D. 8,96 lít
Giải thích:
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
2----->1
\(V_{O_2}=1.22,4=22,4\left(l\right)\)
Câu 33: A
Câu 34: D
Câu 35:
\(m_{H_2O}=2\left(kg\right)=2000\left(g\right)\Rightarrow n_{H_2O}=\dfrac{2000}{18}=\dfrac{1000}{9}\left(mol\right)\)
PT: \(2H_2O\underrightarrow{đp}2H_2+O_2\)
Theo PT: \(\left\{{}\begin{matrix}n_{H_2}=n_{H_2O}=\dfrac{1000}{9}\left(mol\right)\\n_{O_2}=\dfrac{1}{2}n_{H_2O}=\dfrac{500}{9}\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=\dfrac{1000}{9}.22,4\approx2488,8\left(l\right)\\V_{O_2}=\dfrac{500}{9}.22,4\approx1244,4\left(l\right)\end{matrix}\right.\)
→ Đáp án: D
Câu 36: A (giống câu 30)
Câu 37:
PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{H_2}=1\left(mol\right)\Rightarrow V_{O_2}=1.22,4=22,4\left(l\right)\)
→ Đáp án: A
Đổ dung dịch chứa 1g HBr vào dung dịch chứa 1g NaOH. Nhúng giấy quỳ tím vào dung dịch thu được thì giấy quỳ tím chuyển sang nàu nào sau đây:
A. Màu đỏ.
B. Màu xanh.
C. Không đổi màu.
D. Không xác được.
B đúng.
nHBr = 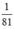 mol
mol
nNaOH = 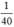 mol
mol
NaOH + HBr → NaBr + H2O
nNaOH > nHBr (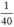 >
> 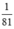 ) ⇒ sau phản ứng NaOH dư
) ⇒ sau phản ứng NaOH dư
⇒ nhúng giấy quỳ vào dung dịch thu được giấy quỳ sẽ chuyển màu xanh