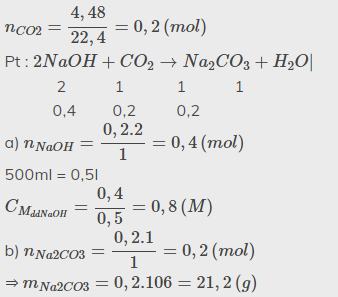Dẫn 4,48l khí CO2 (ở đktc) vào 500ml dung dịch NaOH a) Tính nồng độ mol/l của dung dịch NaOH đã phản ứng b) Tính khối lượng muối thu được sau phản ứng

Những câu hỏi liên quan
Dẫn 4,48l khí CO2 (ở đktc) vào 500ml dung dịch NaOH a) Tính nồng độ mol/l của dung dịch NaOH đã phản ứng b) Tính khối lượng muối thu được sau phản ứng
\(nCO_2=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
pthh:
\(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
1mol 2mol 1mol 1mol
0,2 0,4 0,2 0,2
\(CM_{NaOH}=\dfrac{0,4}{0,5}=0,8M\)
\(mNa_2CO_3=\) 0,2 . 106 = 21,2 gam
n CO2=\(\dfrac{4,48}{22,4}\)=0,2 mol
TH1
CO2+2NaOH->Na2CO3+H2O
0,2-----0,4--------------0,2 mol
CMNaOH=\(\dfrac{0,4}{0,5}\)=0,8 M
=>m muối=0,2.106=21,2g
TH2 :
NaOH+CO2->NaHCO3
0,2--------0,2---------0,2 mol
CmNaOH =\(\dfrac{0,2}{0,5}=0,4M\)
=>m NaHCO3=0,2.84=16,8g
Đúng 1
Bình luận (1)
Xem thêm câu trả lời
Dẫn 6,72(l) khí CO2(đktc) qua 500ml dung dịch NaOH 1(M). Tính khối lượng muối thu được sau phản ứng?
nCO2=0,3(mol)
nNaOH=0,5(mol)
Vì: 1< nNaOH/nCO2=0,5/0,3=1,67<2
=> Sp thu được là hỗn hợp 2 muối
PTHH: 2 NaOH + CO2 -to-> Na2CO3 + H2O
2x____________x_________x(mol)
NaOH + CO2 -> NaHCO3
y_____y______y(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}2x+y=0,5\\x+y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
=> m(muối)= mNa2CO3 + mNaHCO3=0,2.106+0,1.84= 29,6(g)
Đúng 3
Bình luận (0)
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(PTHH:CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
Mol: 0,3 0,3
\(\Rightarrow m_{Na_2CO_3}=0,3.106=31,8\left(g\right)\)
Đúng 0
Bình luận (1)
nCO2= \(\dfrac{V}{22,4}\)=\(\dfrac{6,72}{22,4}\)=0,3 (mol).
nNaOH= CM.V= 1 . 0,5= 0,5(mol).
\(\dfrac{n_{NaOH}}{n_{CO2}}\)=\(\dfrac{0,5}{0,3}\)= 1,67 mà 1<1,67<2 ⇒ tạo 2 muối (1) và (2).
CO2 + NaOH -> NaHCO3 (1)
CO2 + NaOH -> Na2CO3 + H2O (2)
Lập TLSS: \(\dfrac{0,3}{1}\) > \(\dfrac{0,5}{0,1}\)
⇒Tính theo NaOH.
mNaHCO3= 0,5 . 84 = 42g
mNa2CO3= 0,5 . 106= 53g
Đúng 0
Bình luận (2)
Cho 12,6 gam Natri sunfit phản ứng vừa đủ với 150ml dung dịch HCl.Sau phản ứng thu được V lít khí (đktc)
a. Tính V
b.Tính nông độ mol của dung dịch HCl đã dùng
c. Dẫn toàn bộ lượng khí trên qua 40 gam dd NaOH 10% .Tính khối lượng muối thu được sau phản ứng ?
\(a,n_{Na_2SO_3}=\dfrac{12,6}{126}=0,1mol\\ Na_2SO_3+2HCl\rightarrow2NaCl+SO_2+H_2O\\ n_{SO_2}=n_{Na_2SO_4}=0,1mol\\ V_{SO_2}=0,1.22,4=2,24l\\ b,n_{HCl}=0,1.2=0,2mol\\ C_{M_{HCl}}=\dfrac{0,2}{0,15}=\dfrac{4}{3}M\\ c,n_{NaOH}=\dfrac{40.10}{100.40}=0,1mol\\ T=\dfrac{0,1}{0,1}=1\\ \Rightarrow Tạo,NaHSO_3\\ NaOH+SO_2\rightarrow NaHSO_3\\ m_{NaHSO_3}=0,1.64+0,1.40=10,4g\)
Đúng 3
Bình luận (0)
1. Hấp thụ hoàn toàn 2,24 lít CO2 (đktc) vào 100ml dd NaOH. Sau phản ứng nung từ từ dung dịch thu đc 9,5g muối khan. Tính nồng độ mol của dd NaOH đã dùng
2. Người ta dẫn 2,24 lít CO2 qua bình đựng dd NaOH. Khí CO2 bị hấp thụ hoàn toàn. Sau phản ứng thu được muối nào tạo thành? khối lượng là bn?
1.nCO2=0,1 (mol )
TH1: Số mol của CO2 dư => Khối lượng muối khan tối đa tạo được là:
mmuối=0,1.84=8,4<9,5 (loại )
TH2: CO2 hết
Gọi số mol CO2 tạo muối Na2CO3;NaHCO3 lần lượt là x, y
2NaOH+CO2→Na2CO3+H2O
NaOH+CO2→NaHCO3
Ta có : \(\left\{{}\begin{matrix}x+y=0,1\\106x+84y=9,5\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,05\\y=0,05\end{matrix}\right.\)
⇒nNaOH=2.0,05+0,05=0,15 (mol)
⇒CMNaOH=\(\dfrac{0,15}{0,1}\)=1,5M
Đúng 3
Bình luận (4)
Câu 2 thật ra anh thấy chưa chặt chẽ nha!
Đúng 0
Bình luận (3)
2. Vì CO2 bị hấp thụ hoàn toàn
=> CO2 hết, NaOH dư
nCO2 = 0,1 (mol)
CO2 + 2NaOH -------> Na2CO3 + H2O
\(n_{Na_2CO_3}=n_{CO_2}=0,1\left(mol\right)\)
=> \(m_{Na_2CO_3}=0,1.106=10,6\left(g\right)\)
Đúng 1
Bình luận (0)
Dẫn từ từ 13,44 lít khí CO2 ở đktc vào 500 ml dung dịch NaOH 1,5. Tính nồng độ mol/l của các chất có trong dung dịch sau phản ứng.
$n_{CO_2} = \dfrac{13,44}{22,4} = 0,6(mol) ; n_{NaOH} = 0,5.1,5 = 0,75(mol)$
Ta có :
$1 < n_{NaOH} : n_{CO_2} = 0,75 : 0,6 = 1,25 < 2$ nên sản phẩm có $Na_2CO_3(a\ mol) ; NaHCO_3(b\ mol)$
Ta có :
$n_{CO_2} = a + b = 0,6(mol)$
$n_{NaOH} = 2a + b = 0,75(mol)$
Suy ra: a = 0,15 ; b = 0,45
$C_{M_{Na_2CO_3}} = \dfrac{0,15}{0,5} = 0,3M$
$C_{M_{NaHCO_3}} = \dfrac{0,45}{0,5} = 0,9M$
Đúng 2
Bình luận (0)
Bài 8. Dẫn khí CO2 vào 100 ml dung dịch NaOH 3M , sau phản ứng thu được hai muối có mol bằng nhau. Tính thể tích khí CO2 ở đktc đã dùng.
Trung hòa 100 ml dung dịch CH3COOH 0,3M bằng dung dịch NaOH 1,5M. a) Tính thể tích dung dịch NaOH đã dùng ? b) Tính khối lượng muối thu được sau phản ứng ? c) Tính nồng độ mol của chất tan có trong dung dịch sau phản ứng ( biết thể tích thay đổi không đáng kể) ? Biết C= 12; O= 16; H = 1 ; Na=23
a) \(n_{CH_3COOH}=0,1.0,3=0,03\left(mol\right)\)
PTHH: CH3COOH + NaOH --> CH3COONa + H2O
0,03---->0,03--------->0,03
=> \(V_{dd.NaOH}=\dfrac{0,03}{1,5}=0,02\left(l\right)\)
b) mCH3COONa = 0,03.82 = 2,46 (g)
c) \(C_{M\left(CH_3COONa\right)}=\dfrac{0,03}{0,1+0,02}=0,25M\)
Đúng 2
Bình luận (0)
Bài 7: Hấp thụ hoàn toàn 3,36 lít CO2 (đktc) vào trong 200ml dung dịch NaOH 1M (khối lượng riêng D 1,25 g/ml) sau phản ứng thu được dung dịch X. Biết rằng khí CO2 tham gia được phản ứng sau: CO2 +H2O + muối trung hòa --- muối axit. Tính nồng độ phần trăm của chất tan trong dung dịch X.
Bài 8: Hòa tan muối RCO3 trong lượng vừa đủ dung dịch HNO3 20% thu được dung dịch có nồng độ muối là 26,582%. Tìm CTHH của muối cacbonat đã dùng.
Giúp mình vs
Đọc tiếp
Bài 7: Hấp thụ hoàn toàn 3,36 lít CO2 (đktc) vào trong 200ml dung dịch NaOH 1M (khối lượng riêng D = 1,25 g/ml) sau phản ứng thu được dung dịch X. Biết rằng khí CO2 tham gia được phản ứng sau: CO2 +H2O + muối trung hòa ---> muối axit. Tính nồng độ phần trăm của chất tan trong dung dịch X. Bài 8: Hòa tan muối RCO3 trong lượng vừa đủ dung dịch HNO3 20% thu được dung dịch có nồng độ muối là 26,582%. Tìm CTHH của muối cacbonat đã dùng. Giúp mình vs
Bài 7:
Ta có: \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\n_{NaOH}=0,2\cdot1=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Tạo 2 muối
PTHH: \(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
a_______2a__________a (mol)
\(CO_2+NaOH\rightarrow NaHCO_3\)
b_______b__________b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}a+b=0,15\\2a+b=0,2\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,05\\b=0,1\end{matrix}\right.\)
Mặt khác: \(m_{dd}=m_{CO_2}+m_{ddNaOH}=0,15\cdot44+200\cdot1,25=256,6\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{Na_2CO_3}=\dfrac{0,05\cdot106}{256,6}\cdot100\%\approx2,1\%\\C\%_{NaHCO_3}=\dfrac{0,1\cdot72}{256,6}\cdot100\%\approx2,8\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Bài 8:
PTHH: \(RCO_3+2HNO_3\rightarrow R\left(NO_3\right)_2+CO_2\uparrow+H_2O\)
Giả sử \(n_{RCO_3}=1\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_{HNO_3}=2\left(mol\right)\\n_{R\left(NO_3\right)_2}=1\left(mol\right)=n_{CO_2}\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{ddHNO_3}=\dfrac{2\cdot63}{20\%}=630\left(g\right)\\m_{R\left(NO_3\right)_2}=R+124\left(g\right)\\m_{CO_2}=44\left(g\right)\end{matrix}\right.\) \(\Rightarrow C\%_{R\left(NO_3\right)_2}=\dfrac{124+R}{R+60+630-44}=0,26582\)
\(\Leftrightarrow R=65\) (Kẽm) \(\Rightarrow\) CTHH của muối cacbonat là ZnCO3
Đúng 2
Bình luận (0)
Bài 7: Hấp thụ hoàn toàn 3,36 lít CO2 (đktc) vào trong 200ml dung dịch NaOH 1M (khối lượng riêng D = 1,25 g/ml) sau phản ứng thu được dung dịch X. Biết rằng khí CO2 tham gia được phản ứng sau: CO2 +H2O + muối trung hòa ---> muối axit. Tính nồng độ phần trăm của chất tan trong dung dịch X.