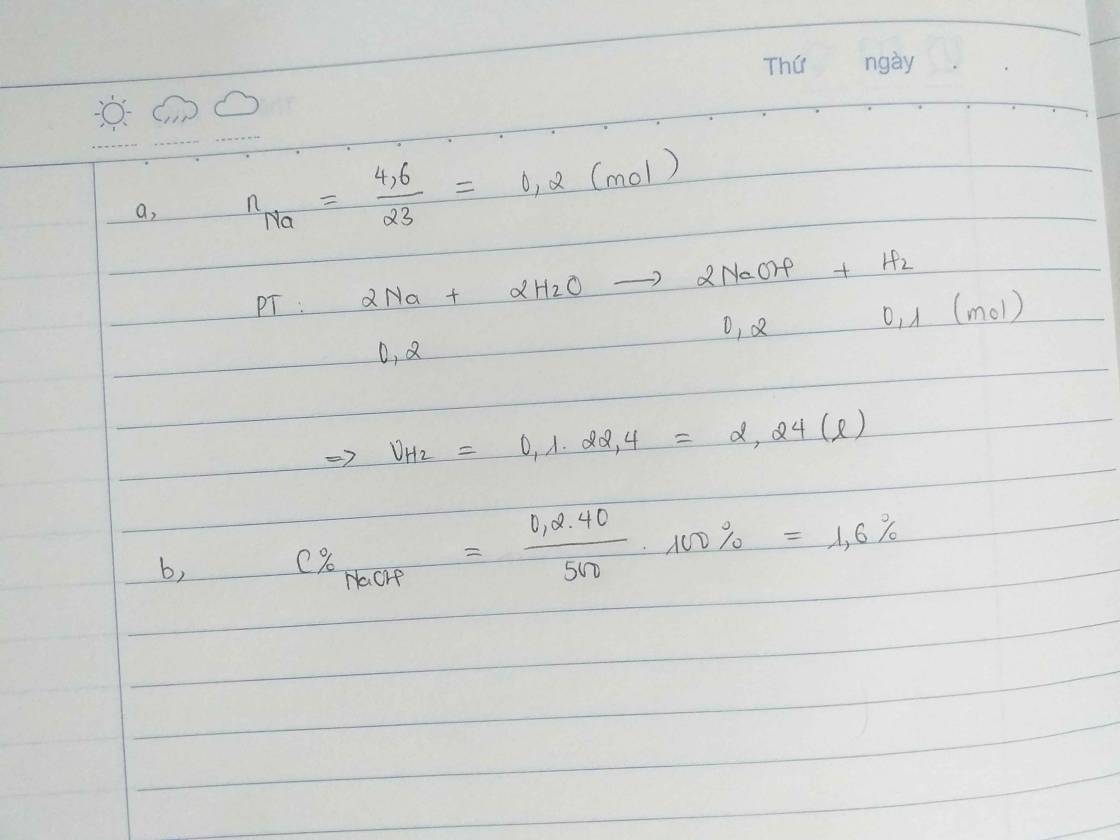hòa tan 2.3 g Na vào 47.8g H2O. Tính C%

Những câu hỏi liên quan
Xác định chất tan và tính khối lượng dung dịch thu được cho mỗi thí nghiệm sau:
1/ Hòa tan 10ml C2H5OH vào 100ml H2O
Biết khối lượng riêng của C2H5OH là 0,8 g/ml của H2O là 1 g/ml 2/ Hòa tan hoàn toàn 2,3 gam Na vào 100gam nước.
2) nNa=0,1(mol)
PTHH: Na + H2O -> NaOH + 1/2 H2
0,1_____________0,1_______0,05(mol)
- Chất tan: NaOH
mddNaOH= mNa+ mH2O - mH2= 2,3+100-0,05.2=102,2(g)
Đúng 0
Bình luận (0)
1) mC2H5OH=0,8.10=8(g)
mH2O=100.1=100(g)
mddC2H5OH=100+8=108(g)
Đúng 1
Bình luận (1)
Tính nồng độ % của dd trong các TH sau đây
a) Hòa tan 200g đường vào 2800g H2O
b) Hòa tan 20g Na vào 180g H2O
a)
C% đường = 200/(200 + 2800) .100% = 6,67%
b)
2Na + 2H2O $\to$ 2NaOH + H2
n Na = 20/23(mol)
=> n H2 = 1/2 n Na = 10/23(mol)
Sau phản ứng:
n NaOH= n Na =20/23(mol)
m dd = 20 + 180 - 10/23 . 2 = 199,13(gam)
C% (20/23 .40)/199,13 .100% = 17,47%
Đúng 2
Bình luận (0)
hòa tan 6.9g Na vào 150g H2o thì thu được dung dịch có tính Bazo . Tính c% của dung dịch thu được
\(n_{Na}=\dfrac{6,9}{23}=0,3mol\)
\(n_{H_2O}=\dfrac{150}{18}=\dfrac{25}{3}mol\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(0,3\) \(\dfrac{25}{3}\) 0 0
0,3 0,3 0,3 0,15
\(m_{NaOH}=0,3\cdot40=12g\)
\(m_{H_2}=0,15\cdot2=0,3g\)
\(m_{ddNaOH}=6,9+150-0,3=156,6g\)
\(C\%=\dfrac{12}{156,6}\cdot100\%=7,66\%\)
Đúng 2
Bình luận (0)
\(2Na+2H_2O\rightarrow2NaOH+H_2\uparrow\)
\(nNa=\dfrac{6,9}{23}=0,3\left(mol\right)\)
\(nH_2O=\dfrac{150}{18}=8,3\left(mol\right)\)
Xét tỉ lê :
\(\dfrac{0,3}{2}< \dfrac{8,3}{2}\)
H2O dư , tính số mol dd theo số mol của Na
\(\Rightarrow nNaOH=nNa=0,3\left(mol\right)\)
\(\Rightarrow mNaOH=0,3.40=12\left(g\right)\)
\(C\%=\dfrac{12}{6,9+150}.100\%=7,64\%\)
Đúng 0
Bình luận (0)
Hòa tan 6,9 g Na vào H2O . Sau phản ứng ngta thu đc V(lít) khí Hidro . Cạn dung dịch phản ứng thu đc m(g) xút khan (NaOH) . Tính V,m ( Khí đo ở ĐKTC)
Ta có: \(n_{Na}=\dfrac{6,9}{23}=0,3\left(mol\right)\)
PT: \(2Na+2H_2O\rightarrow2NaOH+H_2\)
____0,3______________0,3_____0,15 (mol)
\(\Rightarrow V=V_{H_2}=0,15.22,4=3,36\left(l\right)\)
\(m=m_{NaOH}=0,3.40=12\left(g\right)\)
Bạn tham khảo nhé!
Đúng 3
Bình luận (3)
Hòa tan hoàn toàn 4.6g Na vào H2O thì thu đc 500 dd
a) Tính Vkhí(đktc)
b) Tính C% đ bazơ tạo ra
PTHH : 2Na + 2H2O -> 2NaOH + H2
Câu 1. Hòa tan hoàn toàn 5,85 g một kim loại M thuộc nhóm IA vào 194,3 g H2O, thu được 1,68 lít H2 (đktc) và dung dịch#A. Kim loại M và nông độ % của chất tan trong dung dịch A là
A. Na và 4,2% B. K và 4,2% C. Na và 5,4% D. K và 5,3%
M + H2O -> MOH + 1/2 H2
nH2= 0,075(mol) -> nM=0,15(mol)
=>M(M)= mM/nM= 5,85/0,15=39(g/mol)
=> M(I) cần tìm là Kali (K=39)
K + H2O -> KOH + 1/2 H2
nKOH= nK=0,15(mol) => mKOH=0,15.56=8,4(g)
mddKOH=mK + mH2O - mH2= 5,85+194,3 - 0,075.2= 200(g)
=>C%ddKOH= (8,4/200).100=4,2%
=>CHỌN B
Đúng 1
Bình luận (0)
Tính khối lượng chất tan :
a) Hòa tan NaCl vào H2O được 200 dung dịch C% = 8%
b) Hòa tan HCl vào H2O được 250 dung dịch C% = 14%
c) Hòa tan H2SO4 vào H2O được 300 dung dịch C% = 19,6%
\(a,m_{NaCl}=\dfrac{8.200}{100}=16\left(g\right)\\ b,m_{HCl}=\dfrac{250.14}{100}=35\left(g\right)\\ m_{H_2SO_4}=\dfrac{19,6.300}{100}=58,8\left(g\right)\)
Đúng 3
Bình luận (1)
Hòa tan 12.4 g NaOH vào 37.6 ml H2O. tính C% dd tạo thành
\(m_{H_2O}=37,6.1=37,6\left(g\right)\\ m_{ddNaOH}=12,4+37,6=50\left(g\right)\\ C\%_{ddNaOH}=\dfrac{12,4}{50}.100=24,8\%\)
Đúng 1
Bình luận (0)
Ta có: \(D_{H_2O}=1\left(g/mol\right)\Rightarrow m_{H_2O}=37,6.1=37,6\left(g\right)\)
\(\Rightarrow C\%_{ddNaOH}=\dfrac{12,4.100\%}{37,6}=32,98\%\)
Đúng 0
Bình luận (2)
xác định chất tan và khối lượng dung dịch thu được ở mỗi thí nghiệm sau :
a)hòa tan hoàn toàn 2,3 g Na vào 100 g H2O
b)hòa tan hoàn toàn 100ml C2H5(OH) vào 100ml nước biết khối lượng riêng của C2H5(OH) là 0,8 g/ml và của nước là 1g/ml