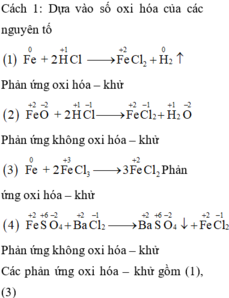Fe + ? ---> FeCl2 + ?

Những câu hỏi liên quan
Fe --> FeCl2 --> Fe(OH)2 --> FeO --> FeCl2
\(Fe+2HCl\rightarrow FeCl_2+H_2\\ FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaCl\\ Fe\left(OH\right)_2\rightarrow\left(t^o\right)FeO+H_2O\\ FeO+2HCl\rightarrow FeCl_2+H_2O\)
Đúng 2
Bình luận (1)
Fe+2HCl->FeCl2+H2
FeCl2+2NaOH->Fe(OH)2+2NaCl
Fe(OH)2-to>FeO+H2O
FeO+2HCl->FeCl2+H2O
Đúng 1
Bình luận (1)
Fe->FeCl2->FeCl3->Fe(OH)3->Fe2(SO4)3->FeCl3->FeCl2->Fe(OH2)
\(Fe+2HCl\rightarrow FeCl_2+H_2\\ 2FeCl_2+Cl_2\xrightarrow[]{t^0}2FeCl_3\\ FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl\\ 2Fe\left(OH\right)_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+6H_2O\\ Fe_2\left(SO_4\right)_3+3BaCl_2\rightarrow2FeCl_2+3BaSO_4\\ 2FeCl_2+Fe\xrightarrow[]{t^0}3FeCl_2\\ FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaCl\)
Đúng 2
Bình luận (0)
Viết ptpứ và cân bằng các phản ứng :::: Fe2o3=>fe Fe=>fecl3 Fecl3=>fecl2 Fecl2=>fe
Xem chi tiết
\(Fe_2O_3+3H_2\underrightarrow{t^0}2Fe+3H_2O\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{t^0}FeCl_3\)
\(2FeCl_3+Fe\rightarrow3FeCl_2\)
\(FeCl_2\underrightarrow{dpdd}Fe+Cl_2\)
Đúng 2
Bình luận (0)
\(Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O\\ 2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3\\ 2FeCl_3 + Fe \to 3FeCl_2\\ Mg + FeCl_2 \to Fe + MgCl_2\)
Đúng 2
Bình luận (0)
Hoàn thành phương trình hóa học của các phản ứng theo sơ đồ chuyển hóa sau ghi rõ điều kiện (nếu có) :1.Fe==>Fe3O42.fe3o4==>fecl23.fecl2==>fe(oh)24.fe(oh)2==>fe(oh)35.fe(oh)3==>fe2o36.fe2o3==>fe7.fe==>fecl38.fecl3==>fecl29.fecl2==>fecl310.fecl2==>fe
Xem chi tiết
\(3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\\ Fe_3O_4 + 8HCl \to 2FeCl_3 + FeCl_2 + 4H_2O\\ FeCl_2 + 2KOH \to Fe(OH)_2 + 2KCl\\ 2Fe(OH)_2 + \dfrac{1}{2}O_2 + H_2O \to 2Fe(OH)_3\\ 2Fe(OH)_3 \xrightarrow{t^o} Fe_2O_3 + 3H_2O\)
Đúng 2
Bình luận (0)
\(Fe+O_2-->Fe_3O_4\\ Fe_3O_4+HCl-->FeCl_2+FeCl_3+H_2O\\ FeCl_2+NaOH-->Fe\left(OH\right)_2+NaCl\\ Fe\left(OH\right)_2+O_2+H_2O-->Fe\left(OH\right)_3\\ Fe\left(OH\right)_3-t^o->Fe_2O_3+H_2O\)
Đúng 0
Bình luận (0)
fe(oh)2 -< feso4-<fecl2-<fe(no3)2 -<fe(oh)2-<feo_<fecl2
H2->Hcl->Cl2->FeCl2->Fe(No3)2->Fe(OH)2->FeSo4->FeCl2->AgNo3 nhanh với ạ
\(H_2+Cl_2\underrightarrow{a/s}2HCl\)
\(4HCl+MnO_2\rightarrow MnCl_2+Cl_2+2H_2O\)
\(4Cl_2+2Fe_2O_3\underrightarrow{t^o}4FeCl_2+3O_2\uparrow\)
\(FeCl_2+2AgNO_3\rightarrow Fe\left(NO_3\right)_3+2AgCl\downarrow\)
\(Fe\left(NO_3\right)_2+2KOH\rightarrow2KNO_3+Fe\left(OH\right)_2\downarrow\)
\(Fe\left(OH\right)_2+H_2SO_4\rightarrow FeSO_4+2H_2O\)
\(FeSO_4+BaCl_2\rightarrow FeCl_2+BaSO_4\downarrow\)
Đúng 1
Bình luận (2)
Hoàn thành các PTHH sau
1.Fe+.................➜ FeSO4
2.FeSO4+.................➜ Fe(OH)2
3.Fe(SO4)3+...................➜ Fe(OH)3
4.Fe(OH)2+.................➜ FeO
5.Fe(OH)3+.................➜ Fe2O3
6.FeO+...................➜ FeCl2
7.Fe2O3+.................➜FeCl3
8.Fe+.................➜FeCl2
9.Fe+.................➜FeCl3
10.FeCl3+...............➜FeCl2
1.Fe+H2SO4.➜ FeSO4+H2
2.FeSO4+ NaOH➜ Fe(OH)2 + Na2SO4
3.Fe2(SO4)3+ 6NaOH➜ 2Fe(OH)3 +3Na2SO4
4.Fe(OH)2➜ FeO +H2O
5.2Fe(OH)3➜ Fe2O3 +3H2O
6.FeO+ 2HCl ➜ FeCl2 +H2O
7.Fe2O3+ 6HCl ➜2FeCl3 +3H2O
8.Fe+Cl2➜FeCl2
9.2Fe+6HCl ➜2FeCl3 +3H2
10.2FeCl3.➜2FeCl2 +Cl2
Chúc bạn học tốt
Nhớ tích cho mình nhé
Đúng 0
Bình luận (1)
Mình làm bạn tự cân bằng nhé:
1.Fe+......H2SO4...........➜ FeSO4 + H2
2.FeSO4+.........NaOH........➜ Fe(OH)2 + Na2SO4
3.Fe2(SO4)3+........NaOH...........➜ Fe(OH)3 + Na2SO4
4.Fe(OH)2 \(\underrightarrow{t^o}\) FeO + H2O
5.Fe(OH)3 \(\underrightarrow{t^o}\) Fe2O3 + H2O
6.FeO+........HCl...........➜ FeCl2 + H2O
7.Fe2O3+........HCl.........➜FeCl3 +H2O
8.Fe+......HCl...........➜FeCl2 +H2
9.Fe+........Cl2.........➜FeCl3
10.FeCl3+........Fe.......➜FeCl2
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Cho các phương trình hóa học sau:(1)
Fe
+
2
HCl
→
FeCl
2
+
H
2
(2)
FeO
+
2
HCl
→
FeCl
2
+
H
2
O...
Đọc tiếp
Cho các phương trình hóa học sau:
(1) Fe + 2 HCl → FeCl 2 + H 2
(2) FeO + 2 HCl → FeCl 2 + H 2 O
(3) Fe + 2 FeCl 3 → 3 FeCl 2
(4) FeSO 4 + BaCl 2 → BaSO 4 ↓ + FeCl 2
Số phản ứng oxi hóa – khử là
A. 1.
B. 2.
C. 3.
D. 4.
Fe->FeCl2->FeSO4->Fe(OH)2->FeO->Fe
\(Fe+2HCl\rightarrow FeCl_2+H_2\\ FeCl_2+Ag_2SO_4\rightarrow FeSO_4+2AgCl\\ FeSO_4+Ba\left(OH\right)_2\rightarrow Fe\left(OH\right)_2+BaSO_4\\ Fe\left(OH\right)_2\xrightarrow[]{t^0}FeO+H_2O\\ FeO+H_2\xrightarrow[]{t^0}Fe+H_2O\)
Đúng 1
Bình luận (0)
Hòa tan Fe trong HCl thu được FeCl2 và 3,36 lít H2 ở điều kiện tiêu chuẩn .Tính khối lượng của Fe ,FeCl2
\(PTHH:Fe+2HCl->FeCl_2+H_2\)
0,15<--0,3<------0,15<-----0,15 (mol)
\(n_{H_2\left(dktc\right)}=\dfrac{V}{22,4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(m_{Fe}=n\cdot M=0,15\cdot56=8,4\left(g\right)\)
\(m_{FeCl_2}=n\cdot M=0,15\cdot\left(56+71\right)=19,05\left(g\right)\)
Đúng 4
Bình luận (0)
PTPU: Fe + 2HCl ----> FeCl2 + H2
nH2= V / 22,4 = 3,36 / 22,4 = 0,15 mol
nFe = nH2 = 0,15 mol
=> mFe = n . M = 0,15 . 56 = 8,4g
nHCl = 2nH2 = 0,3 mol
=> nHCl = n . M = 0,3 . 36,5 = 10,95g
Đúng 0
Bình luận (0)