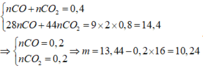Những câu hỏi liên quan
Dẫn từ từ 8,96 lít H2 (đktc) qua m gam oxit sắt FexOy nung nóng. Sau phản ứng thu được 7,2 gam nước và hỗn hợp A gồm 2 chất rắn nặng 28,4 gam (phản ứng xảy ra hoàn toàn) :
a/ Tính giá trị của m?
b/ Lập công thức phân tử của oxit sắt, biết A chứa 59,155% khối lượng sắt đơn chất.
\(n_{H_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(BTKL:\)
\(m+0.4\cdot2=28.4+7.2\)
\(\Rightarrow m=34.8\left(g\right)\)
\(b.\)
\(m_{Fe}=0.59155\cdot28.4=16.8\left(g\right)\)
\(n_{Fe}=\dfrac{16.8}{56}=0.3\left(mol\right)\)
\(PTHH:\)
\(\dfrac{x}{y}=\dfrac{n_{Fe}}{n_{H_2}}=\dfrac{0.3}{0.4}=\dfrac{3}{4}\)
\(CT:Fe_3O_4\)
Đúng 3
Bình luận (0)
Dẫn từ từ 8,96 lít H2 ( đktc ) qua m gam oxit sắt FexOy nung nóng. Sau phản ứng thu được hỗn hợp A gồm 2 chất rắn nặng 28,4 gam . Đem hỗn hợp A phản ứng với dung dịch HCL dư thì thấy đc 6.72 lít khí ko màu thoát ra . ( phản ứng xảy ra hoàn toàn , các khí đo ở đktc a,Tìm giá trị m ?b,Xác định công thức háo học của oxit sắt
Đọc tiếp
Dẫn từ từ 8,96 lít H2 ( đktc ) qua m gam oxit sắt FexOy nung nóng. Sau phản ứng thu được hỗn hợp A gồm 2 chất rắn nặng 28,4 gam . Đem hỗn hợp A phản ứng với dung dịch HCL dư thì thấy đc 6.72 lít khí ko màu thoát ra . ( phản ứng xảy ra hoàn toàn , các khí đo ở đktc
a,Tìm giá trị m ?
b,Xác định công thức háo học của oxit sắt
- Cho phản ứng xảy ra hoàn toàn (2 chất trong A có sắt và oxit khác oxit sắt ban đầu)
\(yH_2+Fe_xO_y\rightarrow\left(t^o\right)xFe+yH_2O\left(1\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\left(2\right)\\ n_{H_2\left(2\right)}=n_{Fe\left(2\right)}=n_{Fe\left(1\right)}=0,3\left(mol\right)\\ n_{O\left(trong.oxit\right)}=n_{H_2O}=n_{H_2}=0,4\left(mol\right)\\ BTKL:m_{H_2}+m_{oxit}=m_A+m_{H_2O}\\ \Leftrightarrow0,4.2+m=28,4+18.0,4\\ \Leftrightarrow m=34,8\left(g\right)\\ b,x:y=0,3:0,4=3:4\Rightarrow x=3;y=4\\ \Rightarrow CTHH:Fe_3O_4\)
Đúng 4
Bình luận (1)
Dẫn từ từ 8,96 lít khí H2 (đktc) qua m gam oxit sắt FexOy nung nóng. sau phản ứng được 7,2 gam nước và hỗn hợp A gồm 2 chất nặng 28,4 gam(PƯ xảy ra hoàn toàn)
a. Tìm giá trị m?
b lập công thức phân tử của oxit sắt, biết A có chứa 59,155% khối lượng đơn chất sắt.
a, Số mol các chất: \(nH_2=\dfrac{8,96}{22}.4=0,4\left(mol\right)\)
Số mol \(H_2O=\dfrac{7,2}{18}=0,4\left(mol\right)\)
=> Số mol nguyên tử Oxi là 0,4 mol
\(\Rightarrow m_O=0,4.16=6,4\left(g\right)\)
Vậy khối lượng FexOy ban đầu bằng kl hh 2 chất rắn sau phản ứng cộng với kl nguyên tử Oxi mất đi từ
\(Fe_xO_y\): \(m=28.4+6,4=34,8\left(g\right)\)
b, Trong hỗn hợp A kl sắt đôn chất là:
\(m_{Fe}=59,155.28,4=16,8\left(g\right)\Rightarrow n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
Gọi CT của Oxit sắt là \(Fe_xO_y\left(x;y>0\right)\)
Ta có:
\(Fe_xO_y+yH_2\underrightarrow{to}xFe+yH_2O\) (*)
\(.........y.....x.....y\)
\(..0,4mol...0,3mol..0,4mol\)
Theo (*): \(\dfrac{x}{y}=\dfrac{0,3}{0,4}=\dfrac{3}{4}\Rightarrow x=3;y=4\)
Vậy CT của Oxit sắt cần tìm là: \(Fe_3O_4\)
Đúng 0
Bình luận (0)
Dẫn 2,24 lít H2(đktc) qua m gam bột oxit sắt (FexOy) nung nóng, sau phản ứng xảy ra hoàn toàn thu được chất rắn B và hỗn hợp khí và hơi D. Tỉ khối hơi của D so với H2 bằng 7,4. Cho chất rắn B vào bình đựng dung dịch HCl dư, sau phản ứng xảy ra hoàn toàn thấy khối lượng bình tăng 3,24 gam. Viết các phương trình phản ứng xảy ra và xác định công thức oxit sắt
Đọc tiếp
Dẫn 2,24 lít H2(đktc) qua m gam bột oxit sắt (FexOy) nung nóng, sau phản ứng xảy ra hoàn toàn thu được chất rắn B và hỗn hợp khí và hơi D. Tỉ khối hơi của D so với H2 bằng 7,4. Cho chất rắn B vào bình đựng dung dịch HCl dư, sau phản ứng xảy ra hoàn toàn thấy khối lượng bình tăng 3,24 gam. Viết các phương trình phản ứng xảy ra và xác định công thức oxit sắt
PTHH: \(Fe_xO_y+yH_2\underrightarrow{t^o}xFe+yH_2O\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
Đặt \(\left\{{}\begin{matrix}n_{Fe\left(oxit\right)}=a\left(mol\right)=n_{H_2}\\n_{O\left(oxit\right)}=b\left(mol\right)\end{matrix}\right.\)
Ta có: \(m_{tăng}=m_{Fe}-m_{H_2}\) \(\Rightarrow56a-2a=3,24\) \(\Rightarrow a=n_{Fe}=0,06\left(mol\right)\)
Hỗn hợp D gồm \(\left\{{}\begin{matrix}n_{CO_2\left(dư\right)}=c\left(mol\right)\\n_{H_2O}=n_{O\left(oxit\right)}=b\left(mol\right)\end{matrix}\right.\)
Ta có hệ phương trình: \(\left\{{}\begin{matrix}c+b=0,1\\18b+2c=7,4\cdot2\cdot\left(b+c\right)\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}b=0,08\\c=0,02\end{matrix}\right.\)
\(\Rightarrow x:y=a:b=0,06:0,08=3:4\)
\(\Rightarrow\) Công thức cần tìm là Fe3O4
Đúng 1
Bình luận (0)
Dẫn từ từ 8,96 lít H2 ( đktc ) qua m gam oxit sắt FexOy nung nóng. Sau phản ứng thu được 7,2 gam nước và hỗn hợp A gồm 2 chất rắn nặng 28,4 gam ( phản ứng xảy ra hoàn toàn )
a,Tìm giá trị m ?
b, Lập công thức phân tử của oxit sắt, biết A có chứa 59,155% khối lượng sắt đơn chất
a)
yH2 + FexOy --> xFe + yH2O
nH2 = 8,96/22,4 = 0,4 (mol)
nH2O = 7,2/18 = 0,4 (mol)
=> H2 đã phản ứng hết hay FexOy dư
mH2 = 2.0,4 = 0,8 (g)
Ta có m = mA + mH2O - mH2 = 28,4 + 7,2 - 0,8 = 34,8 (g)
b)
Trong A chứa 59,155% Fe
=> mFe = 59,155%.28,4 = 16,8 (g)
=> nFe = 16,8/56 = 0,3 mol
Từ pt pư ta có
x/y = nFe/nH2 = 0,3/0,4 = 3/4
=> Oxit sắt đã dùng là Fe3O4
Đúng 3
Bình luận (1)
a)
yH2 + FexOy \(\rightarrow\) xFe + yH2O
nH2 = \(\dfrac{8,96}{22,4}\) = 0,4 (mol)
nH2O = \(\dfrac{7,2}{18}\) = 0,4 (mol)
=> H2 đã phản ứng hết hay FexOy dư
mH2 = 2.0,4 = 0,8 (g)
Ta có m = mA + mH2O - mH2 = 28,4 + 7,2 - 0,8 = 34,8 (g)
b)
Trong A chứa 59,155% Fe
=> mFe = 59,155%.28,4 = 16,8 (g)
=> nFe = \(\dfrac{16,8}{56}\) = 0,3 mol
Từ pt pư ta có
x/y = nFe/nH2 = \(\dfrac{0,3}{0,4}\) = 3/4
=> Oxit sắt đã dùng là Fe3O4
Đúng 1
Bình luận (6)
Dẫn từ từ 8,96 lít H2 đo ở điều kiện tiêu chuẩn qua m gam oxit sắt nung nóng. Sau phản ứng thu được 7,2 gam nước và hỗn hợp A gồm 2 chất rắn nặng 28,4 gam. (Biết phản ứng xảy ra hoàn toàn)
a) Tính giá trị m
b) Lập công thức phân tử của oxit sắt biết A có chứa 59,155% khối lượng của đơn chất sắt.
a/ \(n_{H_2}=\frac{8,96}{22,4}=0,4\)
\(\Rightarrow m_{H_2}=2.0,4=0,8\)
Theo định luật bảo toàn khối lượng thì:
\(m_{H_2}+m=m_{H_2O}+m_r\)
\(\Leftrightarrow m=m_{H_2O}+m_r-m_{H_2}=7,2+28,4-0,8=34,8\)
Đúng 0
Bình luận (2)
Cái đề này câu b sai số rồi nha bạn
Đúng 0
Bình luận (0)
Dẫn 8.96l hidro(dktc) qua m gam oxit sắt FexOy nung nóng. Sau phản ứng thu được 7,2g nước và hỗn hợp A gồm 2 chất rắn nặng 28,4g. Biết p.ư xảy ra hoàn toàn.
a/ tìm m
b/ lập cthh của oxit sắt, biết A chứa 59.155% k.lg sắt đơn chất
1)yH2 + FexOy --> xFe + yH2On
H2 = 8,96/22,4 = 0,4 (mol)
nH2O = 7,2/18 = 0,4 (mol)
=> H2 đã phản ứng hết hay FexOy dư
mH2 = 2.0,4 = 0,8 (g)
Ta có m = mA + mH2O - mH2 = 28,4 + 7,2 - 0,8 = 34,8 (g)
2)Trong A chứa 59,155% Fe=
> mFe = 59,155%.28,4 = 16,8 (g)
=> nFe = 16,8/56 = 0,3 mol
Từ pt pư ta cóx/y = nFe/nH2 = 0,3/0,4 = 3/4=> Oxit sắt đã dùng là Fe3O4
Đúng 0
Bình luận (5)
Thổi từ từ V lít hỗn hợp khí (đktc) gồm CO và H2 đi qua ống đựng 16,8 gam hỗn hợp 3 oxit CuO, Fe3O4, Al2O3 nung nóng, phản ứng hoàn toàn. Sau phản ứng thu được m gam chất rắn và một hỗn hợp khí nặng hơn khối lượng của hỗn hợp V là 0,32 gam. Tính V và m A. 0,224 lít và 14,48 gam B. 0,672 lít và 18,46 gam C. 0,112 lít và 12,28 gam D. 0,448 lít và 16,48 gam
Đọc tiếp
Thổi từ từ V lít hỗn hợp khí (đktc) gồm CO và H2 đi qua ống đựng 16,8 gam hỗn hợp 3 oxit CuO, Fe3O4, Al2O3 nung nóng, phản ứng hoàn toàn. Sau phản ứng thu được m gam chất rắn và một hỗn hợp khí nặng hơn khối lượng của hỗn hợp V là 0,32 gam. Tính V và m
A. 0,224 lít và 14,48 gam
B. 0,672 lít và 18,46 gam
C. 0,112 lít và 12,28 gam
D. 0,448 lít và 16,48 gam
Đáp án D.
Ta có: mO = 0,32 (g) ⟹ nO = 0 , 32 16 = 0,02 (mol) nên số mol của hỗn hợp CO, H2 cũng bằng 0,02 (mol) ⟹ V = 0,02.22,4 = 0,448 (l).
Theo định luật bảo toàn khối lượng, m = 16,8 – 0,02.16 = 16,48 (g).
Đúng 0
Bình luận (0)
Dẫn 8,96 lít khí CO (đktc) qua 13,44 gam hỗn hợp rắn gồm Fe3O4, Fe2O3 và CuO nung nóng, đến khi phản ứng xảy ra hoàn toàn, thu được m gam rắn X và hỗn hợp khí Y có tỉ khối so với He bằng 9. Giá trị của m là A. 9,68 gam B. 10,24 gam C. 9,86 gam D. 10,42 gam
Đọc tiếp
Dẫn 8,96 lít khí CO (đktc) qua 13,44 gam hỗn hợp rắn gồm Fe3O4, Fe2O3 và CuO nung nóng, đến khi phản ứng xảy ra hoàn toàn, thu được m gam rắn X và hỗn hợp khí Y có tỉ khối so với He bằng 9. Giá trị của m là
A. 9,68 gam
B. 10,24 gam
C. 9,86 gam
D. 10,42 gam