\(Fe_3O_4+Al=Fe_xO_y+Al_2O_3\)

Những câu hỏi liên quan
Cân bằng PTHH:
KMnO_4+HClrightarrow KCl+MnCl_2+Cl_2+H_2O
Fe_3O_4+HClrightarrow FeCl_2+FeCl_3+H_2O
Fe_xO_y+COunderrightarrow{t^o}FeO+CO_2
Fe_xO_y+Alunderrightarrow{t^o}Fe+Al_2O_3
Fe_xO_y+H_2SO_4underrightarrow{t^o}Fe_2left(SO_4right)_3+SO_2+H_2O
Fe_xO_y+H_2underrightarrow{t^o}Fe+H_2O
Đọc tiếp
Cân bằng PTHH:
\(KMnO_4+HCl\rightarrow KCl+MnCl_2+Cl_2+H_2O\)
\(Fe_3O_4+HCl\rightarrow FeCl_2+FeCl_3+H_2O\)
\(Fe_xO_y+CO\underrightarrow{t^o}FeO+CO_2\)
\(Fe_xO_y+Al\underrightarrow{t^o}Fe+Al_2O_3\)
\(Fe_xO_y+H_2SO_4\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+SO_2+H_2O\)
\(Fe_xO_y+H_2\underrightarrow{t^o}Fe+H_2O\)
1: 2KMnO4 + 16HCl -> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
2: Fe3O4 + 8HCl --> FeCl2 + 2FeCl3 + 4H2O
3: 3FexOy + 2yAl --> 3xFe + yAl2O3
4: 2FexOy + (6x-2y)H2SO4 --> xFe2(SO4)3 + (3x-2y)SO2 + (6x-2y)H2O
5: FexOy + yH2 --> xFe + yH2O
Đúng 0
Bình luận (0)
Cân bằng các PTHH sau:
\(Al+Fe_xO_y\rightarrow Fe_nO_m+Al_2O_3\)
\(FeO+HCl\rightarrow Fe_xCl_y+H2O\)
\(FeCl_x+Cl_2\rightarrow FeCl_y\)
3nAl + (6n-4m)FexOy \(\underrightarrow{t^0}\) 6FenOm + (3n-2m)Al2O3
FeO + 2HCl => FeCl2 + H2O
xFeClx + Cl2 => xFeCl3
Bạn xem lại đề nha , mình sửa lại rồi đấy
Đúng 0
Bình luận (0)
Hoàn thành PTHH:
\(Fe_xO_y+CO-->Fe+CO_2\)
\(CaO+H_3PO_4-->Ca_3\left(PO_4\right)_2+H_2O\)
\(Fe_3O_4+HCl-->FeCl_2+FeCl_3+H_2O\)
\(Fe_xO_y+HCl-->FeCl_{\dfrac{2y}{x}}+H_2O\)
\(Al_2O_3+HCl-->AlCl_3+H_2O\)
FexOy+yCO--->xFe+yCO2
3CaO+2H3PO4--->Ca3(PO4)2+3H2O
Fe3O4+8HCl--->FeCl2+2FeCl3+4H2O
FexOy+2yHCl--->xFeCl2y/x+yH2O
Al2O3+6HCl--->2AlCl3+3H2O
Đúng 0
Bình luận (0)
FexOy + yCO --to--> xFe + yCO2
3CaO + 2H3PO4 --> Ca3(PO4)2 + 3H2O
Fe3O4 + 8HCl --> FeCl2 + 2FeCl3 + 4H2O
FexOy + 2yHCl --> xFeCl2y/x + yH2O
Al2O3 + 6HCl --> 2AlCl3 + 3H2O
Đúng 0
Bình luận (9)
Hoàn thành các phương trình hóa học sau: \(Fe_xO_y+Al\rightarrow FeO+Al_2O_3\)
Chỉ mình cách làm thôi chứ đưa ra kết quả thôi thì trên mạng cũng có. Chỉ dễ hiểu nha
\(Fe_xO_y+Al\rightarrow FeO+Al_2O_3\)
Hóa trị của \(Fe\) trong chất \(Fe_xO_y\) là \(\frac{2y}{x}\) ( quy tắc đường chéo )
Độ tăng denta hóa trị:
\(Al\rightarrow Al_2O_3\left(Al:0;Al_2O_3:III\right)\Rightarrow\Delta_1=3\)
Độ giảm denta hóa trị:
\(FeO\rightarrow Fe_xO_y\left(FeO:II;Fe_xO_y:\frac{2y}{x}\right)\Rightarrow\Delta_2=\frac{2y}{x}-2\)
Đổi chéo denta hóa trị ta được:( \(\Delta_1\)đổi cho \(Fe_xO_y\) \(\Delta_2\) đổi cho \(Al_2O_3\)hay gọi là đổi hệ số, sau đó cân bằng theo thứu tự \(Fe\rightarrow O\rightarrow Al\) )
\(3Fe_xO_y+\left(\frac{y-x}{x}\right)Al\rightarrow3xFeO+\left(\frac{2y}{x}-2\right)Al_2O_3\)
Chúc bạn học tốt !
Đúng 0
Bình luận (0)
À nếu bạn muốn thử lại có đúng hay không, bạn chỉ cần thay x và y là một số tự nhiên. VD: mình thay \(x=2;y=3\) cho ra chất \(Fe_2O_3\) . Sau đó bạn tính có bao nhiên phân tử Fe, O, Al trước phản ứng và sau phản ứng. Nếu như bằng nhau thì đúng rồi nha bạn.
Với lại phía trước \(Al\) mình nhầm bạn sửa giúp mình thành là \(\left(\frac{4y}{x}-4\right)Al\)
Đúng 0
Bình luận (0)
Nhôm tác dụng với \(Fe_3O_4\) theo sơ đồ \(Al+Fe_3O_4->Al_2O_3+Fe\)
Trộn 5,4g bột Al tác dụng với 17,4g Fe3O4 rồi nung hỗn hợp ở nhiệt độ cao trong đk ko có oxi.Hòa tan chất rắn được 5,376 lít H2 đktc.Tính hiệu suất pư Biết các oxit kim loại tác dụng với axit tạo ra muối và nước
GIÚP MK NHANH NHÉ MK ĐANG CẦN GẤP
Thực hiện chuỗi phản ứng sau:b) Al_2O_3rightarrow Alrightarrow Al_2left(SO_4right)_3rightarrow AlCl_3rightarrow Alleft(OHright)_3rightarrow Al_2O_3c) Alrightarrow AlCl_3rightarrow Alleft(OHright)_3rightarrow Al_2O_3rightarrow Al_2left(SO_4right)_3rightarrow AlCl_3
Đọc tiếp
Thực hiện chuỗi phản ứng sau:
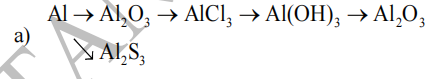
b) \(Al_2O_3\rightarrow Al\rightarrow Al_2\left(SO_4\right)_3\rightarrow AlCl_3\rightarrow Al\left(OH\right)_3\rightarrow Al_2O_3\)
c) \(Al\rightarrow AlCl_3\rightarrow Al\left(OH\right)_3\rightarrow Al_2O_3\rightarrow Al_2\left(SO_4\right)_3\rightarrow AlCl_3\)
a)\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
\(2AlCl_3+3Ba\left(OH\right)_2\rightarrow2Al\left(OH\right)_3\downarrow+3BaCl_2\)
\(2Al\left(OH\right)_3\underrightarrow{t^o}Al_2O_3+3H_2O\)
\(2Al+3S\underrightarrow{t^o}Al_2S_3\)
Đúng 2
Bình luận (0)
Cân bằng các phương trình sau theo phương pháp thăng bằng electron:
\(1.FeO+HNO_3\rightarrow Fe\left(NO_3\right)_3+N_xO_y+H_2O\\ 2.M+HNO_3\rightarrow M\left(NO_3\right)_n+N_xO_y+H_2O\\ 3.Fe_2O_3+Al\rightarrow Fe_xO_y+Al_2O_3\\ 4.Fe_mO_n+HNO_3\rightarrow Fe\left(NO_3\right)_3+NO+H_2O\\ 5.FeS_2+HNO_3\rightarrow Fe\left(NO_3\right)_3+N_2O_x+H_2O+H_2SO_4\)
1)
(5x-2y)FeO+(16x-6y)HNO3\(\rightarrow\)(5x-2y)Fe(NO3)3+NxOy+(8x-3y)H2O
2)
(5x-2y)M+(6nx-2ny)HNO3\(\rightarrow\)(5x-2y)M(NO3)n+nNxOy+(3nx-ny)H2O
3)
3xFe2O3+(6x-4y)Al\(\rightarrow\)6FexOy+(3x-2y)Al2O3
4)
3FemOn+(12m-2n)HNO3\(\rightarrow\)3mFe(NO3)3+(3m-2n)NO+(6m-n)H2O
5)
(10-2x)FeS2+(60-6x)HNO3\(\rightarrow\)(10-2x)Fe(NO3)3+15N2Ox+(10+x)H2O+(20-4x)H2SO4
Đúng 0
Bình luận (1)
Viết pt hoàn thành sơ đồ phản ứng sau:
1 2 3 4 5
Al → \(Al_2O_3\)→\(AlCl_3\)→\(Al\left(OH\right)_3\)→\(Al_2O_3\)→Al
\(4Al+3O_2->2Al_2O_3\)
\(Al_2O_3+6HCl->2AlCl_3+3H_2\)
Đúng 0
Bình luận (0)
\(\left(1\right)4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\\\left(2\right)Al_2O_3+6HCl\rightarrow 2AlCl_3+3H_2O\\ \left(3\right)AlCl_3+3KOH\rightarrow Al\left(OH\right)_3+3KCl\\ \left(4\right)2Al\left(OH\right)_3\rightarrow\left(t^o\right)Al_2O_3+3H_2O\\ \left(5\right)2Al_2O_3\rightarrow\left(\text{đ}pnc,xt\right)4Al+3O_2\)
Đúng 0
Bình luận (0)
Cân bằng: KHCO_3+Caleft(OHright)_{2left(dright)}rightarrow K_2CO_3+CaCO_3+H_2O
Al_2O_3+KHSO_4rightarrow Alleft(SO_4right)_3+K_2SO_4+H_2O
Fe_3O_3+H_2underrightarrow{t^o}Fe_xO_y+H_2O
NaHSO_4+BaCOrightarrow Na_2SO_4+BaSO_4+CO_2+H_2O
H_2SO_4+Feunderrightarrow{t^o}Fe_2left(SO_4right)_3+SO_2+H_2O
Đọc tiếp
Cân bằng: \(KHCO_3+Ca\left(OH\right)_{2\left(d\right)}\rightarrow K_2CO_3+CaCO_3+H_2O\)
\(Al_2O_3+KHSO_4\rightarrow Al\left(SO_4\right)_3+K_2SO_4+H_2O\)
\(Fe_3O_3+H_2\underrightarrow{t^o}Fe_xO_y+H_2O\)
\(NaHSO_4+BaCO\rightarrow Na_2SO_4+BaSO_4+CO_2+H_2O\)
\(H_2SO_4+Fe\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+SO_2+H_2O\)
\(2KHCO_3+Ca\left(OH\right)_2\rightarrow K_2CO_2+CaCO_3+2H_2O\)
\(Al_2O_3+6KHSO_4\rightarrow Al_2\left(SO_4\right)_3+3K_2SO_4+3H_2O\)
\(nFe_2O_3+\left(3y-2x\right)H_2\rightarrow2Fe_xO_y+\left(3y-2x\right)H_2O\)
\(2NaHSO_4+BaCO_3\rightarrow Na_2SO_4+BaSO_4+CO_2+H_2O\)
\(6H_2SO_4+2Fe\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
Đúng 0
Bình luận (0)
























