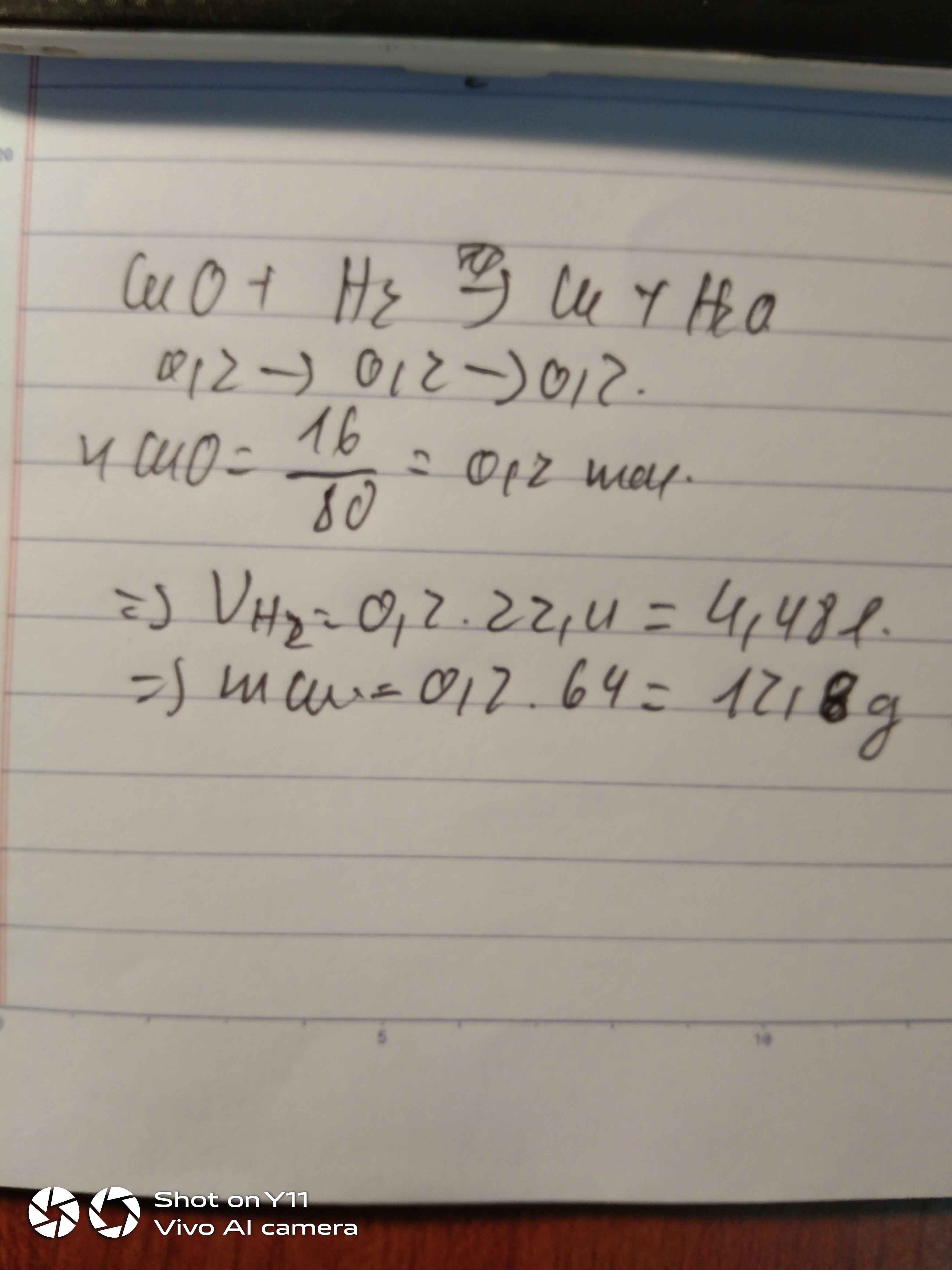Ở nhiệt độ cao, CuO phản ứng với H2 tạo thành Cu và H2O. Tính khối lượng Cu thu được khi sử dụng 16 gam CuO.
Cho Cu=64; O=16; H=1

Những câu hỏi liên quan
Cho khí H2 đi qua CuO thu được Cu và H2O CuO+H2->Cu+H2O A viết pthh của phản ứng B.cho biết thu được 12,8g kim loại Cu - tính khối lượng Cu0 đã tham giá phản ứng - tính thể tích khi H2 (đktc) - tính khới lượng H20 tạo thành
\(A:CuO+H_2\underrightarrow{t^0}Cu+H_2O\\ B.n_{Cu}=\dfrac{12,8}{64}=0,2mol\\ n_{CuO}=n_{H_2}=n_{H_2O}=0,2mol\\ m_{CuO}=0,2.80=16g\\ V_{H_2}=0,2.22,4=4,48l \\ m_{H_2O}=0,2.18=3,6g\)
Đúng 3
Bình luận (0)
Cho 16 gam đồng (II) oxit phản ứng hết V lít khí hidro H2 (đktc) ở nhiệt độ thích hợp, sau phản ứng thu được Cu và H2O. Biết phản ứng xảy ra vừa đủ. a/ Tính giá trị V./ b/ Tính khối lượng Cu thu được sau phản ứng.
Đọc tiếp
Cho 16 gam đồng (II) oxit phản ứng hết V lít khí hidro H2 (đktc) ở nhiệt độ thích hợp, sau phản ứng thu được Cu và H2O. Biết phản ứng xảy ra vừa đủ. a/ Tính giá trị V./ b/ Tính khối lượng Cu thu được sau phản ứng.
\(CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ n_{H_2} = n_{CuO} = \dfrac{16}{80} = 0,2(mol)\\ \Rightarrow V_{H_2} = 0,2.22,4 = 4,48(lít)\)
Đúng 2
Bình luận (0)
Theo gt ta có: $n_{CuO}=0,2(mol)$
$CuO+H_2\rightarrow Cu+H_2O$
Ta có: $n_{H_2}=n_{CuO}=0,2(mol)\Rightarrow V_{H_2}=4,48(mol)$
Đúng 1
Bình luận (0)
nhưng mà còn câu b nữa mà các bạn giúp mình với ;-;
Đúng 0
Bình luận (4)
Xem thêm câu trả lời
B5: Cho 16 (g) Fe2O3 bị khử bởi khí H2. Sau phản ứng thu được là Fe và H2O. Tính khối lượng Fe, khối lượng H2O. Biết H80%.B 6: Dùng khí CO để khử CuO ở to cao . Sau phản ứng thu được 19,2 (g) Cu . Tính khối lượng CuO. Tính V CO đã dùng ở đktc Biết H 85%.B7: Dùng khí CO để khử ZnO ở to cao . Sau phản ứng thu được 26 (g) Zn. Tính khối lượng ZnO. V CO ở đktc Biết H 75%.
Đọc tiếp
B5: Cho 16 (g) Fe2O3 bị khử bởi khí H2. Sau phản ứng thu được là Fe và H2O. Tính khối lượng Fe, khối lượng H2O. Biết H=80%.
B 6: Dùng khí CO để khử CuO ở to cao . Sau phản ứng thu được 19,2 (g) Cu . Tính khối lượng CuO. Tính V CO đã dùng ở đktc Biết H = 85%.
B7: Dùng khí CO để khử ZnO ở to cao . Sau phản ứng thu được 26 (g) Zn. Tính khối lượng ZnO. V CO ở đktc Biết H = 75%.
1. cho 13g kẽm phản ứng hoàn toàn với dd HCl. a) Viết PTHH b) Tính thể tích khí hidro tạo thành( ở đktc). c) Nếu dùng toàn bộ lượng H2 bay ở trên đem khử 12g bột CuO ở nhiệt độ cao thì chất nào còn dư bao nhiêu g?(Zn=65, Cl= 35,5; Cu=64; O=16; H=1)
a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, Ta có: \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\) \(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c, PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Ta có: \(n_{CuO}=\dfrac{12}{80}=0,15\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,15}{1}< \dfrac{0,2}{1}\), ta được H2 dư.
Theo PT: \(n_{H_2\left(pư\right)}=n_{CuO}=0,15\left(mol\right)\)
\(\Rightarrow n_{H_2\left(dư\right)}=0,2-0,15=0,05\left(mol\right)\)
\(\Rightarrow m_{H_2\left(dư\right)}=0,05.2=0,1\left(g\right)\)
Đúng 1
Bình luận (0)
Cacbohiđrat là gì?
Đáp án là D. Cacbohiđrat là những hợp chất hữu cơ đa chức và đa số chúng có công thức chung là Cn(H2O)m. Các hợp chất cacbohiđrat bao gồm đường, tinh bột và các chất tương tự. Chúng đóng vai trò quan trọng trong nhiều quá trình sinh học, bao gồm cung cấp năng lượng cho cơ thể, hỗ trợ cấu trúc tế bào và chức năng của não.
2 / 2Đáp án là D. Este no, đơn chức, mạch hở có công thức tổng quát dạng CnH2nO (n ≥ 2).
Trong các este no đơn chức, mạch hở, nhóm chức cac
Đáp án là B. CH3COOH không phải là este. Đó là axit axetic.
Các phương trình hóa học cho các chất trong câu hỏi là:
A. HCOOCH3 - este metyl formiat (hay metyl fomiat)
B. CH3COOH - axit axetic
C. CH3COOCH3 - este metyl axetat (hay metyl acetat)
D. HCOOC6H5 - este benzylic formiat (hay benzylic fomiat)
Este là một dạng hợp chất hữu cơ, trong đó có một nhóm este (-COO-) được tạo thành bởi liên kết giữa một nhóm hydroxyl (-OH) của một axit với một nhóm hydroxyl của một rượu.
Đáp án là B. Khi đun nóng este CH3COOC2H5 với một lượng vừa đủ dung dịch NaOH,
2 / 2Đáp án là D. Công thức của este X là CH3COOC2H5.
Khi este CH3COOC2H5 thủy ph
Đáp án là B. Có 2 loại cacbohiđrat quan trọng là đường đơn và tinh bột.
Đường đơn là các đường đơn giản nhất
Đáp án là B. Saccarozơ là chất thuộc loại đisaccarit.
Saccarozơ là một loại đường mạch không quá ngọt, được tìm thấy trong một số thực vật như mía đường, củ cải đường và cỏ lúa mì. Nó là một hợp chất đường đơn gồm glucose và fructose liên kết với nhau thông qua liên kết glycosidic giữa carbon thứ 1 của glucose và carbon thứ 2 của fructose. Các chất khác trong câu hỏi bao gồm:
Glucozơ: là đường đơn, được tìm thấy trong nhiều thực phẩm, bao gồm trái cây, mật ong và nước ép trái cây.Xenlulozơ: là một chất polymer của glucose và là thành phần chính của thành tế bào thực vật.Fructozơ: là đường đơn tự nhiên, thường được tìm thấy trong trái cây như cam, táo, nho, dưa hấu, vv.Đáp án là A và D.
Anilin có tính bazơ, do đó nó phản ứng với axit để tạo muối. Do đó, nó phản ứng với dung dịch HCl để tạo ra muối anilinium. Công thức của muối này là C6H5NH3Cl.
Phản ứng của anilin với dung dịch NaOH cũng có thể xảy ra, tạo ra muối anilinat. Công thức của muối này là C6H5NH2Na.
Với dung dịch Na2CO3, phản ứng sẽ không xảy ra vì Na2CO3 không có tính axit hoặc bazơ đủ mạnh để tác động lên anilin.
Với dung dịch NaCl, phản ứng cũng không xảy ra vì NaCl là muối và không có khả năng tác động lên các chất khác.
Để tạo ra este, cần sử dụng một phân tử ancol và một phân tử axit. Trong trường hợp này, có hai ancol có cùng công thức phân tử C3H8O, đó là propanol (CH3CH2CH2OH) và isopropanol [(CH3)2CHOH]. Có ba axit có công thức phân tử C4H8O2, đó là axit butanoic (CH3CH2CH2COOH), axit 2-metylpropanoic [(CH3)2CHCOOH] và axit 2-metylbutanoic [(CH3)2CHCH2COOH].
Để tạo ra đồng phân cấu tạo, ta cần ghép mỗi ancol với từng axit, sau đó kiểm tra xem các sản phẩm este thu được có khác nhau không. Bằng cách làm như vậy, ta có thể tạo ra tất cả các este đồng phân cấu tạo của nhau.
Với propanol:
Khi phản ứng với axit butanoic, thu được propyl butanoate (CH3CH2CH2OCOCH2CH2COOH).Khi phản ứng với axit 2-metylpropanoic, thu được isopropyl 2-metylpropanoate [(CH3)2CHOCOCH(CH3)2COOH].Khi phản ứng với axit 2-metylbutanoic, thu được isopropyl 2-metylbutanoate [(CH3)2CHOCOCH2CH(CH3)COOH].Với isopropanol:
Khi phản ứng với axit butanoic, thu được isopropyl butanoate [(CH3)2CHOCOCH2CH2COOH].Khi phản ứng với axit 2-metylpropanoic, thu được tert-butyl 2-metylpropanoate [(CH3)3COCOCH(CH3)2COOH].Khi phản ứng với axit 2-metylbutanoic, thu được tert-butyl 2-metylbutanoate [(CH3)3COCOCH2CH(CH3)COOH].Tổng cộng, ta thu được 6 este đồng phân cấu tạo của nhau: propyl butanoate, isopropyl butanoate, isopropyl 2-metylpropanoate, isopropyl 2-metylbutanoate, tert-butyl 2-metylpropanoate và tert-butyl 2-metylbutanoate. Do đó, đáp án là D.
a) Viết phương trình hóa học
Zn + 2HCl -> ZnCl2 + H2
b) Tính thể tích khí hidro tạo thành
Theo định luật Avogadro, 1 mol khí ở đktc chiếm thể tích 22,4 lít. Ta cần tìm số mol khí H2 tạo thành:
n(H2) = m(Zn) / MM(Zn) = 13 / 65 = 0.2 mol
Theo phương trình phản ứng, 1 mol Zn tạo ra 1 mol H2, vậy số mol H2 tạo thành bằng 0.2 mol.
Vậy thể tích khí H2 tạo thành là: V = n x Vm = 0.2 x 22.4 = 4.48 lít.
c) Xác định số mol CuO cần dùng để khử hoàn toàn lượng H2 tạo thành:
2 mol HCl + CuO -> CuCl2 + H2O
n(H2) = n(CuO) / 2
n(CuO) = 2 x n(H2) = 0.2 mol
Khối lượng CuO cần dùng:
m(CuO) = n(CuO) x MM(CuO) = 0.2 x 79.5 = 15.9 g
Nhưng ta chỉ có 12g CuO, vậy lượng CuO dư là:
12 - 15.9 = -3.9 g
Vậy không có chất nào dư, và kết quả này không hợp lý vì lượng CuO dư âm.
Đúng 0
Bình luận (0)
Cho 16 gam đồng(III) oxit phản ứng hết V lít khí H2(đktc) ở nhiệt độ thích hợp, sau phản ứng thu được Cu và H2O.Biết phản ứng xảy ra vừa đủ.
a/ Tính giá trị V.
B/Tính khối lượng Cu thu được sau phản ứng.
PTHH: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Ta có: \(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)=n_{Cu}=n_{H_2}\)
\(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,2\cdot22,4=4,48\left(l\right)\\m_{Cu}=0,2\cdot64=12,8\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Khử 16g Copper(II) oxide (CuO ) bằng khí hydrogen (H2 ) a.Tính thể tích khí hydrogen (H2 ) tham gia phản ứng? b. Tính khối lượng kim loại tạo thành? Fe= 56, O=16, Cu=64, H=1
Dẫn khí hiđro đi qua CuO nung nóng. Viết phương trình hóa học xảy ra. Sau phản ứng, thu được 19,2 gam Cu. Tính khối lượng CuO tham gia phản ứng và thể tích khí hiđro (đktc) cần dùng. (Biết O=16, Cu=64, Al=27, H=1, S=32).
cho 11 gam hỗn hợp gồm al và fe tác dụng vừa đủ với đ hcl tạo 8,96 lít khí h2 thoát thành ra ở đktc. Viết pthh và tính:
a)tính % về khối lượng các chất ban đầu
b)dẫn toàn bộ khí trên qua 16 gam bột cuo đun nóng đến phản ứng kết thúc. tính cu thu được
a) PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
a_____________________\(\dfrac{3}{2}\)a (mol)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
b____________________b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}27a+56b=11\\\dfrac{3}{2}a+b=\dfrac{8,96}{22,4}=0,4\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2\cdot27}{11}\cdot100\%\approx49,09\%\\\%m_{Fe}=50,91\%\end{matrix}\right.\)
b) PTHH: \(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\\n_{H_2}=\dfrac{3}{2}a+b=0,4\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) H2 còn dư, tính theo CuO
\(\Rightarrow n_{Cu}=0,2\left(mol\right)\) \(\Rightarrow m_{Cu}=0,2\cdot64=12,8\left(g\right)\)
Đúng 3
Bình luận (1)
Gọi n Al = a ( mol ) , n Fe = b ( mol )
Có: n H2 = 0,4 ( mol )
PTHH
2AL + 6HCL ===> 2ALCL3 + 3H2
a--------------------------------------a
Fe + 2HCl ====> FeCL2 + H2
b------------------------------------b
Ta có hpt:
\(\left\{{}\begin{matrix}27a+56b=11\\1,5a+b=0,4\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
=> m AL = 5,4 ( g ) ; m Fe = 5,6 ( g )
b) Có : n CuO = 0,2 ( mol )
PTHH:
CuO + H2 ====> Cu +H2O
0,2----0,2-----------0,2
theo pthh: n Cu = 0,2 ( mol ) => m Cu = 12,8 ( g )
Đúng 1
Bình luận (1)
\(n_{H2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Pt : \(2Al+6HCl\rightarrow2AlCl_3+3H_2|\)
2 6 2 3
a 1,5a
\(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
b 1b
a) Gọi a là số mol của Al
b là số mol của Fe
\(m_{Al}+m_{Fe}=11\left(g\right)\)
⇒ \(n_{Al}.M_{Al}+n_{Fe}.M_{Fe}=11g\)
⇒ 27a + 56b = 11g (1)
Theo phương trình : 1,5a +1b = 0,4(2)
Từ (1),(2), ta có hệ phương trình :
27a + 56b = 11
1,5a + 1b = 0,4
⇒ \(\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(m_{Al}=0,2.27=5,4\left(g\right)\)
\(m_{Fe}=0,1.56=5,6\left(g\right)\)
0/0Al = \(\dfrac{5,4.100}{11}=49,09\)0/0
0/0Fe = \(\dfrac{5,6.100}{11}=50,91\)0/0
b) Pt : \(H_2+CuO\rightarrow\left(t_o\right)Cu+H_2O|\)
1 1 1 1
0,4 0,4
\(n_{Cu}=\dfrac{0,4.1}{1}=0,4\left(mol\right)\)
⇒ \(m_{Cu}=0,4.64=25,6\left(g\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (2)
Cho 13g kẽm phản ứng hoàn toàn với dung dịch HCl
a.Viết PTHH
b.Tính thể tích khí H2 sinh ra (đktc)
c.Nếu dùng toàn bộ lượng H2 bay ra ở trên đem khử 12 g bột CuO ở nhiệt độ cao thì chất nào còn dư bao nhiêu gam?(Zn=65;Cl=35.5;Cu=64;O=16;H=1)
\(n_{Zn}=\dfrac{13}{65}=0,2mol\)
a)\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2 0,2 0,2
b)\(V_{H_2}=0,2\cdot22,4=4,48l\)
c)\(n_{CuO}=\dfrac{12}{80}=0,15mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,15 0,2
Sau phản ứng H2 còn dư và dư:
\(m_{H_2}=\left(0,2-0,15\right)\cdot2=0,1g\)
Đúng 3
Bình luận (1)
a) PTHH
Zn + 2HCl -> ZnCl2 + H2↑
0,2 0,2
nZn= 13/65= 0,2 (mol)
b)VH2= 0,2.22,4= 4,48 (l)
sorry bt mỗi phần a;b thui
Đúng 1
Bình luận (1)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\ n_{CuO}=\dfrac{12}{80}=0,15\left(mol\right)\)
PTHH: Zn + 2HCl ---> ZnCl2 + H2
0,2 -----------------------> 0,2
\(\rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
LTL: \(0,15< 0,2\rightarrow\)H2 dư
\(\rightarrow m_{H_2\left(dư\right)}=\left(0,2-0,15.1\right).2=0,1\left(g\right)\)
Đúng 2
Bình luận (0)