Muối A có chứa Fe,S,O có thành phần % các nguyên tố : 36,8%Fe, 21%S, còn lại O.Tìm CTHH của A. Biết khối lượng mol của A là 152 g/mol

Những câu hỏi liên quan
Tìm CTHH của một hợp chất có chứa 36,8% Fe, 21% S, còn lại là Oxi, biết khối lượng mol của hợp chất là 152g
Gọi CTHH của hợp chất là FexSyOz
=> 56x = 152.36,8% => x = 1
32y = 152.21% => y = 1
16z = 152 - 56.1 - 32.1=64 => z = 4
Vậy CTHH của hợp chất là FeSO4
Đúng 1
Bình luận (0)
Hợp chất A có khối lượng mol phân tử là 106 g/mol,thành phần các nguyên tố theo khối lượng:43,4%Na,11,3%Cvà 45,3%O.Tìm CTHH của hợp chất A
Hãy tìm công thức hóa học của một hợp chất có thành phần theo khối lượng là 36,8% Fe; 21,0% S; 42,2% O. Biết khối lượng mol của hợp chất bằng 152 g/mol.
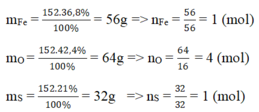
Vậy trong 1 phân tử hợp chất có 1 nguyên tử Fe, 4 nguyên tử O, 1 nguyên tử S.
⇒ CTHH là FeSO4.
Đúng 1
Bình luận (0)
Lập CTHH các chất sau:A) Al và OB) Zn và ClC)H và S(II)D) Fe(III) và nhóm OHE) hợp chất khí A có thành phần trăm các nguyên tô (theo hối lượng) 5,88% H, 94,12%S.biết tỉ khối của khí A so với Hidro là 17.F)hợp chất A có thành phần % các nguyên tố: 2,04% H, 32,65% S và còn lại là oxi.G) hợp chất A có thành phần % các nguyên tố: 40% S còn lại là oxi. Biết khối lượng mol của A là 80g
Đọc tiếp
Lập CTHH các chất sau:
A) Al và O
B) Zn và Cl
C)H và S(II)
D) Fe(III) và nhóm OH
E) hợp chất khí A có thành phần trăm các nguyên tô (theo hối lượng) 5,88% H, 94,12%S.biết tỉ khối của khí A so với Hidro là 17.
F)hợp chất A có thành phần % các nguyên tố: 2,04% H, 32,65% S và còn lại là oxi.
G) hợp chất A có thành phần % các nguyên tố: 40% S còn lại là oxi. Biết khối lượng mol của A là 80g
a)\(Al_2O_3\)
b)\(ZnCl_2\)
c)\(H_2S\)
d)\(Fe\left(OH\right)_3\)
Đúng 0
Bình luận (0)
a) Al2O3
B) ZnCl2
C) H2S
D) Fe(OH)3
e) H2S
F) H2SO4
G) SO3
Đúng 0
Bình luận (0)
Hãy tìm công thức hóa học của một hợp chất có thành phần theo khối lượng là 36,8% Fe; 21,0% S; 42,2% O. Biết khối lượng mol của hợp chất bằng 152 g/mol
Khối lượng mol của Fe là MFe = = 56 g
Khối lượng mol của S là: MS = = 32 g
Khối lượng mol của O là: MO = = 64 g
Gọi công thức hóa học của hợp chất là FeXSyOz, ta có:
56 . x = 56 => x = 1
32 . y = 32 => y = 1
16 . z = 64 => z = 4
Vậy hợp chât có công thức hóa học là FeSO4
Đúng 0
Bình luận (0)
Khối lượng mol của Fe là \(M_{Fe}\) = (152 . 36,8)/100 = 56 g
Khối lượng mol của S là: \(M_S\) = (152 . 21)/100 = 32 g
Khối lượng mol của O là: \(M_O\) = (152 . 42,2)/100 = 64 g
Gọi công thức hóa học của hợp chất là \(Fe_xS_yO_z\), ta có:
\(56.x=56\Rightarrow x=1\)
\(32.y=32\Rightarrow y=1\)
\(16.z=64\Rightarrow z=4\)
Vậy hợp chât có công thức hóa học là \(FeSO_4\)
Đúng 0
Bình luận (0)
bài 1: Hãy tìm CTHH của một hợp chất có chứa 36,8% Fe;16,5 S và còn lại là O . Biết khối lượng mol của hợp chất là 152 g/mol
Sửa đề:bài 1: Hãy tìm CTHH của một hợp chất có chứa 36,8% Fe;21% S và còn lại là O . Biết khối lượng mol của hợp chất là 152 g/mol
Gọi CTHH của HC là FexSyOz
x=\(\dfrac{152.36,8\%}{56}=1\)
y=\(\dfrac{152.16,5\%}{32}=1\)
z=\(\dfrac{152-56-32}{16}=4\)
Vậy CTHH của HC là FeSO4
Đúng 0
Bình luận (1)
Biết một hợp chất có khối lượng mol là 400 g/mol và có thành phần theo khối lượng của các nguyên tố như sau: 28% Fe; 24% S còn lại là O. Xác định công thức hóa học của hợp chất trên.
\(m_{Fe}=\%Fe.M_X=28\%.400=112\left(g\right)\\ m_S=\%S.M_X=24\%.400=96\left(g\right)\\ m_O=m_X-m_{Fe}-m_S=400-112-96=192\left(g\right)\)
\(\Rightarrow n_{Fe}=\dfrac{m}{M}=\dfrac{112}{56}=2\left(mol\right)\)
\(m_S=\dfrac{m}{M}=\dfrac{96}{32}=3\left(mol\right)\)
\(m_O=\dfrac{m}{M}=\dfrac{192}{16}=12\left(mol\right)\)
\(CTHH:Fe_2\left(SO_4\right)_3\)
Đúng 1
Bình luận (2)
\(m_{Fe}=\dfrac{28.400}{100}=112g\\ m_S=\dfrac{24.400}{100}=96g\\ m_O=400-112-96=192g\\ \Rightarrow n_{Fe}=\dfrac{112}{56}=2mol\\ n_S=\dfrac{96}{32}=3mol\\ n_O=\dfrac{192}{16}=12\\ CTHH:Fe_2S_3O_{12}\)
Đúng 1
Bình luận (4)
Xác định CTHH của hợp chất A, biết:
- Khối lượng mol của A là 64 g/mol.
- Thành phần % về khối lượng của từng nguyên tố trong hợp chất: S chiếm 50% khối lượng, còn lại là O.
Đang cần gấp ạ
Cảm ơn mọi người
\(m_S=\dfrac{64.50}{100}=32\left(g\right)=>n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(m_O=64-32=32\left(g\right)=>n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> CTHH: SO2
Đúng 1
Bình luận (0)
Tìm CTHH của các hợp chất sau, biết thành phần phần trăm các nguyên tố là:
a) 52,174%C; 13,043% H và 34,783%O. Biết khối lượng mol của hợp chất A là 46 g/mol
b) 28,7%Mg, 14,2%C, còn lại là oxygen. Biết khối lượng mol của hợp chất A là 84 g/mol
\(\%C=\dfrac{12x}{46}.100\%=52,174\%\)
⇒ \(x=2\)
\(\%H=\dfrac{1.y}{46}.100\%=13,043\%\)
⇒ \(y=6\)
\(\%O=\dfrac{16z}{46}.100\%=34,783\%\)
⇒ \(x=1\)
⇒ \(CTHH:C_2H_6O\)
Đúng 1
Bình luận (0)





























