cho 2.3g Na t/d hoàn toàn vs nước
a/viết phương trình phản ứng
b/Tính khối lượng NaOH tạo thành tính thể tích H2 tạo thành (ở đck)
ai bt giúp tui với
cho 2,3 g Na tác dụng hết vs H2O tạo thành NaOH và khí H2
a, Viết PTPỨ xảy ra
b, Tính thể tích khí H2 sinh ra ( ở đktc)
c, Tính khối lượng nước cần dùng cho phản ứng
d, Tính khối lượng dung dịch NaOH tạo thành sau phản ứng
e , viết tóm tắt
a)PTHH: Na+H2O---> NaOH+H2
b)nNa= \(\dfrac{m}{M}=\dfrac{2,3}{23}=0,1\left(mol\right)\)
=>nNa=nH2=0,1 (mol)
=>VH2=n.22,4=0,1.22,4=2,24(l)
c)nNa=nH2O=nNaOH=0,1 (mol)
=>mH2O=0,1.18=1,8(g)
d)mNaOH=0,1.(23+16+1)=4(g)
Học tốt !
a, \(2Na+2H_2O\rightarrow2NaOH+H_2\)
b, \(n_{Na}=\dfrac{2,3}{23}=0,1\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{1}{2}n_{Na}=0,05\left(mol\right)\Rightarrow V_{H_2}=0,05.22,4=1,12\left(l\right)\)
c, \(n_{H_2O}=n_{Na}=0,1\left(mol\right)\Rightarrow m_{H_2O}=0,1.18=1,8\left(g\right)\)
d, \(n_{NaOH}=n_{Na}=0,1\left(mol\right)\Rightarrow m_{NaOH}=0,1.40=4\left(g\right)\)
Cho Natri phản ứng hoàn toàn cới H2O thu được NaOH và 11.2(l)khí H2 (dktc)
a, Viết và cân bằng phương trình phản ứng
b, Tính khối lượng Na phản ứng
c,Tính khối lượn NaOH tạo thành
a) 2Na + 2H2O -------> 2NaOH + H2
b)
nH2 = 11,2 : 22,4 = 0,5 (mol)
Ta có phương trình sau : 2Na + 2H2O -------> 2NaOH + H2
Theo phương trình : ( 2 ) ( 2 ) ( 2 ) ( 1 ) (mol)
Theo đ.b : ( 1 ) ( 1 ) ( 1 ) (0,5) (mol)
=> mNa = 1.23 = 23 (g)
c) mNaOH = 1.(23 + 16 + 1) = 40 (g)
Hòa tan hoàn toàn 4,6g Natri vào nước thu được 300ml dd NaOH
a. Viết phương trình của phản ứng
b. Tính thể tích khí hidro tạo thành ở đktc
c. Tính nồng độ % của dd NaOH thu đc sau phản ứng
\(n_{Na}=\dfrac{4,6}{23}=0,2mol\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
0,2 0,2 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
\(m_{NaOH}=0,2\cdot40=8g\)
\(m_{ddNaOH}=4,6+0,2\cdot18-0,1\cdot2=8g\)
\(\Rightarrow C\%=\dfrac{m_{NaOH}}{m_{ddNaOH}}\cdot100\%=\dfrac{8}{8}\cdot100\%=100\%???\)
Sửa đề: Tính nồng độ mol của dung dịch NaOH???
\(C_{M_{NaOH}}=\dfrac{0,2}{0,3}=\dfrac{2}{3}M\)
vì đề không cho \(D_{NaOH}=???\) nên không tính được dung dịch NaOH
Cho 9,2g Na vào nước dư thì thu được dung dịch NaOH và khí H2.
a. Viết phương trình hoá học
b. Tính thể tích khí H2 (đktc) thoát ra và khối lượng NaOH tạo thành ?
c. Nếu dùng toàn bộ lượng H2 bay ra ở trên đem khử 12 gam bột CuO ở nhiệt độ cao thì chất nào còn dư bao nhiêu gam ? ( Zn = 65 ; Cl = 35,5 ; Cu = 64 ; O = 16 ; H= 1 )
\(a.2Na+2H_2O\rightarrow2NaOH+H_2\\ b.n_{Na}=\dfrac{9,2}{23}=0,4\left(mol\right)\\ n_{H_2}=\dfrac{1}{2}n_{Na}=0,2\left(mol\right)\\ \Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\\ n_{NaOH}=n_{Na}=0,4\left(mol\right)\\ \Rightarrow m_{NaOH}=0,4.40=16\left(g\right)\\ c.H_2+CuO-^{t^o}\rightarrow Cu+H_2O\\ n_{CuO}=\dfrac{12}{80}=0,15\left(mol\right)\\ LTL:\dfrac{0,2}{1}>\dfrac{0,15}{1}\Rightarrow H_2dưsauphảnứng\\ n_{H_2\left(pứ\right)}=n_{CuO}=0,15\left(mol\right)\\ \Rightarrow n_{H_2\left(dư\right)}=0,2-0,15=0,05\left(mol\right)\\ \Rightarrow m_{H_2\left(Dư\right)}=0,05.2=0,1\left(g\right)\)
Cho 28g sắt (Fe) tác dụng với axit clohric (HCL) sau phản ứng thu được muối sắt (II)clorua (FeCl2) và khí hiđro(H2)
a. Viết phương trình phản ứng
b. Tính khối lượng muối sắt (II) clorua(HCl²) tạo thành sau phản ứng
c. Tính thể tích khí hidro ở điều kiện tiêu chuẩn Giúp em với ạ
\(n_{Fe}=\dfrac{m}{M}=\dfrac{28}{56}=0,5\left(mol\right)\\ PTHH:Fe+2HCl->FeCl_2+H_2\)
ti le 1 : 2 : 1 : 1
n(mol) 0,5-->1--------->0,5------>0,5
\(m_{FeCl_2}=n\cdot M=0,5\cdot\left(56+35,5\cdot2\right)=63,5\left(g\right)\\ V_{H_2\left(dktc\right)}=n\cdot22,4=0,5\cdot22,4=11,2\left(l\right)\)
Đốt cháy hoàn toàn lưu huỳnh trong không khí, sau phản ứng thu được 12,8g lưu huỳnh đioxit.
a. Viết phương trình phản ứng
b. Tính khối lượng của cacbonđioxit tạo thành sau phản ứng
c. Tính thể tích không khí, biết oxi chiếm 1/5 thể tích không khí.
nSO2 = 12,8 : 64=0,2 (mol)
pthh : S+ O2 -t->SO2
0,2<--0,2<------0,2(mol)
=> mS= 0,2.32=6,4 (g)
=> VO2= 0,2.22,4=4,48 (l)
ta có
VO2 = 1/5 Vkk <=> Vkk = VO2 : 1/5 = 4,48:1/5 = 22.4 (l)
hòa tan hoàn toàn 11,2 gam fe vào 200 ml dd h2so4 loãng.
a) viết các pt hóa học phản ứng
b) tính thể tích khí h2 thoát ra ở đktc
c) tính nồng độ mol của dd axit đã dùng
d) tính khối lượng muối tạo thành.
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
a) PTHH : \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Theo Pt : \(n_{Fe}=n_{H2SO4}=n_{FeSO4}=n_{H2}=0,2\left(mol\right)\)
b) \(V_{H2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
c) \(C_{MddH2SO4}=\dfrac{0,2}{0,2}=1\left(M\right)\)
d) \(m_{muối}=m_{FeSO4}=0,2.152=30,4\left(g\right)\)
Cho 3,2g oxi hoàn toàn với khí hiđrô,sau phản ứng thu được sản phẩm là nước
a,viết phương trình hoá học B,tính thể tích khí hiđrô cần dùng
C,tỉ khối lượng nước tạo thành sau phản ứng
d,cho khí oxi tác dụng với 3,6 khí hiđrô sau pu chất nào còn dư , dư bao nhiêu MOL
a. PTHH: \(2H_2+O_2\rightarrow2H_2O\)
b. \(n_{O_2}=\dfrac{3,2}{32}=0,1\left(mol\right)\)
Theo PTHH: \(n_{H_2}=n_{O_2}\cdot\dfrac{2}{1}=0,1\cdot\dfrac{2}{1}=0,2\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c. Chưa hiểu đề bài lắm :))
d. Ta có: \(n_{O_2}=0,1\left(mol\right);n_{H_2}=\dfrac{3,6}{22,4}\approx0,16\left(mol\right)\)
Do \(0,1< 0,16\) nên \(H_2\) dư \(0,16-0,1=0,06\left(mol\right)\)
Ở nhiệt độ phòng, hỗn hợp khí X gồm hiđrocacbon A và lượng dư hiđro có tỉ khối so với H2 là 3,375. Khi cho X qua Ni đun nóng cho đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Y có tỉ khối so với H2 là 4,5.
a) Xác định công thức phân tử của A.
b) Tính thành phần phần trăm theo thể tích của các chất có trong X.
Nếu cho X qua Pd/BaSO4 đun nóng cho đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Z. Trong Z chỉ có hai chất khí là B và hiđro.
c) Viết phương trình phản ứng tạo thành B trên. Tính tỉ khối của Z so với hiđro.
d) B có thể cho phản ứng polime hóa. Viết phương trình phản ứng này.
Hợp chất B cho phản ứng với Cl2 ở 500 tạo thành C (có chứa 46,4% khối lượng Cl). C phản ứng với dung dịch NaOH loãng thu được D. Cho D phản ứng với nước và Cl2 thu được E (có chứa 32,1% khối lượng Cl). Sau cùng E phản ứng với dung dịch NaOH loãng thu được F.
e) Viết công thức cấu tạo của các chất từ B đến F và viết các phương trình hóa học xảy ra
a.
BTKL ta có mX = mY => nX . MX = nY . mY
MX / My = nY / mY =0.75
Đặt nX = 1 mol => nY = 0,75 mol => nH2 phản ứng = 1 – 0,75 = 0,25mol
* TH hidrocacbon là anken: n anken = n H2 = 0,25 mol => n H2 trong X = 0,75 => M = (6,75 – 0,75 . 2)/0,25 = 21 (loại) * TH là ankin: => n akin = 0,25/2 = 0,125 => n H2 trong X = 0,875 mol => M = (6,75 – 0,875 . 2)/0,125 = 40 =>C3H4
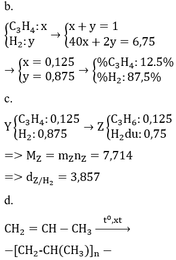

Tính khối lượng của H2 và khối lượng NaOH tạo thành khi cho 2mol Na tác dụng với H2O,biết phương trình phản ứng
Na+H2O -> NaOH + H2
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(\dfrac{2}{2}\) = \(\dfrac{2}{2}\) ( mol )
2 2 2 2 ( mol )
( Cả 2 chất đều không dư )
\(m_{H_2}=1.2=2g\)
\(m_{NaOH}=2.40=80g\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
2 2 1 ( mol )
\(m_{H_2}=1.2=2g\)
\(m_{NaOH}=2.40=80g\)