Dùng khí CO để khử 32g một oxit Sắt ở t\(^o\) cao , sau phản ứng thu được 22,4 g Fe và khí CO\(_2\) . Xác định CTHH của Oxit Sắt đó

Những câu hỏi liên quan
Dùng khí H2 để khử hoàn toàn 4,64g một oxit sắt chưa rõ công thức ở nhiệt độ cao, sau phản ứng thu được 3,36g Fe. Xác định CTHH của oxit sắt
\(m_O=4.64-3.36=1.28\left(g\right)\)
\(n_{Fe}=\dfrac{3.36}{56}=0.06\left(mol\right)\)
\(n_O=\dfrac{1.28}{16}=0.08\left(mol\right)\)
\(n_{Fe}:n_O=0.06:0.08=3:4\)
\(CT:Fe_3O_4\)
Đúng 1
Bình luận (0)
dùng khí h2 vừa đủ để khử hoàn toàn 34,8g một oxit sắt ở nhiệt độ cao. Sau khi phản ứng kết thúc thu được 25,2g sắt, làm lạnh hơi nước thu được sau phản ứng. a. tính thể tích khí H2 đã phản ứng ở đktc b. xác định CTHH của oxit sắt đó c. tính thể tích nước thu đc ở thể lỏng ( giải thích các bước làm )
a) \(n_O=\dfrac{34,8-25,2}{16}=0,6\left(mol\right)\)
=> \(n_{H_2O}=0,6\left(mol\right)\) (bảo toàn O)
=> \(n_{H_2}=0,6\left(mol\right)\) (bảo toàn H)
=> \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
b) \(n_{Fe}=\dfrac{25,2}{56}=0,45\left(mol\right)\)
nFe : nO = 0,45 : 0,6 = 3 : 4
=> CTHH: Fe3O4
c) \(m_{H_2O}=0,6.18=10,8\left(g\right)\)
Mà \(d_{H_2O}=1\left(g/ml\right)\)
=> \(V_{H_2O}=10,8\left(ml\right)\)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 2,32 (g) oxit sắt FexOy cần dùng 104,28ml dd HCl 10% ( d= 1,05g/ml)
a/ Xác định CTHH của oxit sắt
b/ Cho khí CO (đktc) qua ống sứ đựng oxit sắt đốt nóng ( giả sử chỉ xảy ra phản ứng khử). Sau phản ứng thu được hỗn hợp khí A đi ra có tỉ khối so với H2 bằng 17. Tính phần % thể tích các khí có trong hỗn hợp
a)
\(n_{HCl} = \dfrac{104,28.1,05.10\%}{36,5} = 0,3(mol)\)
FexOy + 2yHCl → xFeCl2y/x + yH2O
\(\dfrac{0,15}{y}\)........0,3..........................................(mol)
Suy ra: \(\dfrac{0,15}{y}\).(56x + 16y) = 2,32 ⇒ \(\dfrac{x}{y}=-9,5.10^{-3}\)(Sai đề)
Đúng 1
Bình luận (0)
khử hoàn toàn 16g một oxit sắt nguyên chất bằng khí CO ở nhiệt độ cao. Sau đó dẫn toàn bộ khí thu được qua bình đựng nước vôi trong dư, kết thúc phản ứng thu được 10g kết tủa. Xác định công thức oxit sắt
Khử hoàn toàn một oxit sắt X ở nhiệt độ cao cần vừa đủ V lít khí CO (ở đktc), sau phản ứng thu được 0,84 gam Fe và 0,02 mol khí CO2. Oxit sắt X và giá trị của V lần lượt là: A. Fe3O4 và 0,224 B. Fe3O4 và 0,448 C. FeO và 0,224 D. Fe2O3 và 0,448
Đọc tiếp
Khử hoàn toàn một oxit sắt X ở nhiệt độ cao cần vừa đủ V lít khí CO (ở đktc), sau phản ứng thu được 0,84 gam Fe và 0,02 mol khí CO2. Oxit sắt X và giá trị của V lần lượt là:
A. Fe3O4 và 0,224
B. Fe3O4 và 0,448
C. FeO và 0,224
D. Fe2O3 và 0,448
Đáp án B
Đặt công thức oxit sắt là FexOy
FexOy+ yCO → xFe + yCO2
nFe= 0,84/56= 0,015 mol
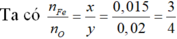
→Công thức oxit là Fe3O4
Ta có: nCO= nCO2= 0,02 mol
→ V= 0,02.22,4= 0,448 lít
Đúng 0
Bình luận (0)
Khử hoàn toàn 16g bột oxit sắt bằng CO ở nhiệt độ cao. Sau phản ứng kết thúc thấy khối lượng chất rắn giảm 4,8g.a) Xác định CTHH của oxit sắt trên?b) Dẫn chất khí thu được qua dung dịch Ca(OH)2 dư. Tính khối lượng kết tủa tạo thành c) Tính thể tích CO cần dùng cho phản ứng trên biết rằng phải dùng CO dư 10% so với lí thuyết và thể tích các chất khí đo ở ĐKTC
Đọc tiếp
Khử hoàn toàn 16g bột oxit sắt bằng CO ở nhiệt độ cao. Sau phản ứng kết thúc thấy khối lượng chất rắn giảm 4,8g.
a) Xác định CTHH của oxit sắt trên?
b) Dẫn chất khí thu được qua dung dịch Ca(OH)2 dư. Tính khối lượng kết tủa tạo thành
c) Tính thể tích CO cần dùng cho phản ứng trên biết rằng phải dùng CO dư 10% so với lí thuyết và thể tích các chất khí đo ở ĐKTC
a. áp dụng định luật bảo toàn nguyên tố
=> 4,8 g là khối lượng O trong oxit sắt
=> nO = 0,3 ; nFe = 0,2
CT oxit sắt là Fe2O3
b. Fe2O3 + 3CO ---> 2Fe + 3CO2
nCO = 0,3 mol
dùng dư 10% => nCO = 0,3 x 110% = 0,33 mol
CÂU C BN TỰ LM NHA, LƯỜI WÁ![]()
Đúng 0
Bình luận (0)
Gọi công thức oxit sắt:Fex0y.
Fex0y+yCO=>xFe+yC02
0.2/x------------>0.2(mol)
_Sau pư khối lượng chất rắn giảm 4.8 g so với ban đầu:
=>mFe=16-4.8=11.2(g)
=>nFe=11.2/56=0.2(mol)
=>n(Fex0y)=0.2/x(mol)
Mà nFex0y=16/(56x+16y) (mol)
=>16x=0.2(56x+16y)
<=>4.8x=3.2y
<=>x/y=2/3
Vậy công thức oxit sắt là Fe203.
_Khí sinh ra là C02 cho tác dụng với dd NaOH:
nC02=0.2*3=0.6(mol)
_Khối lượng dd tăng cũng chính là khối lượng C02 tham gia:
C02+2NaOH=>Na2S03+H20
0.6--->1.2-------->0.6(mol)
=>mC02=0.6*44=26.4(g)
Đúng 1
Bình luận (2)
khử 16g sắt lll Oxit=khí Hiđrô :a) viết pt b) Tính khối lượng sắt thu được c) tinh the tích khí hiđrô ở (dktc)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Khử 23,2 gam một oxit sắt bằng CO , sau phản ứng thu được 16,8 (g) sắt
a) Tính thể tích khí CO2 thoát ra (đktc)
b) Xác định công thức hóa học của oxit ấy
Gọi số mol CO=mol CO2= a mol
Bảo toàn klg=>23,2+28a=44a+16,8
=>a=0,4 mol
=>VCO2=0,4.22,4=8,96 lit
Gọi CT oxit là Fe2On
Bảo toàn Fe: nFe tạo thành=nFe trong oxit ban đầu=16,8/56=0,3 mol
=>n oxit sắt=0,15 mol
=>M oxit sắt=23,2/0,15=464/3 =>n=8/3 CT oxit sắt là Fe3O4
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Khử hoàn toàn 11,6g một oxit sắt (FexOy) bằng khí H2 ở to cao thu được 8,4g sắt kim loại. Xác định CTHH của oxit sắt và tính VH2 (đktc) đã dùng
chỉ mik với các bn
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\\ n_O=\dfrac{11,6-0,15}{16}=0,2\left(mol\right)\)
CTHH: FexOy
\(\rightarrow x:y=n_{Fe}:n_O=0,15:0,2=3:4\)
CTHH: Fe3O4
PTHH: Fe3O4 + 4H2 --to--> 3Fe + 4H2O
0,2 0,15
=> VH2 = 0,2.22,4 = 4,48 (l)
Đúng 3
Bình luận (1)
\(n_{Fe}=\dfrac{8,4}{56}=0,15mol\)
\(n_{Fe_xO_y}=\dfrac{11,6}{56x+16y}\) mol
\(Fe_xO_y+yH_2\rightarrow\left(t^p\right)xFe+yH_2O\)
\(\dfrac{11,6}{56x+16y}\) \(\dfrac{11,6x}{56x+16y}\) ( mol )
\(\Rightarrow\dfrac{11,6x}{56x+16y}=0,15\)
\(\Leftrightarrow11,6x=8,4x+2,4y\)
\(\Leftrightarrow3,2x=2,4y\)
\(\Leftrightarrow4x=3y\)
\(\Leftrightarrow x=3;y=4\)
\(\Rightarrow CTHH:Fe_3O_4\)
\(\Rightarrow n_{H_2}=0,15.4:3=0,2mol\)
\(V_{H_2}=0,2.22,4=4,48l\)
Đúng 2
Bình luận (1)
trong phòng thí nghiệm, ngta dùng khí H2 để khử sắt (III) oxit (Fe2O3) và thu đc 22,4 g sắt (Fe) và nước (H2O)
a) tính khối lượng sắt (III) oxit đã phản ứng?
b) tính thể tích khí hidro đã sử dụng
c) để điều chế lượng khí hidro trên, người ta dùng kim loại kẽm (Zn) cho phản ứng với dung dịch axit sunfuric (H2SO4) . tính khối lượng kim loại kẽm cần dùng
PTHH: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
a+b) \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe_2O_3}=0,2\left(mol\right)\\n_{H_2}=0,6\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe_2O_3}=0,2\cdot160=32\left(g\right)\\V_{H_2}=0,6\cdot22,4=13,44\left(l\right)\end{matrix}\right.\)
c) PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
Theo PTHH: \(n_{Zn}=n_{H_2}=0,6\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,6\cdot65=39\left(g\right)\)
Đúng 3
Bình luận (0)
a,
nFe = 22,4/56 = 0,4 (mol)
PTHH
Fe2O3 + 3H2 ---to----) 2Fe + 3H2O (1)
theo phương trình (1) ,ta có:
nFe2O3 = 0,4 x 2 / 1 = 0,8 (mol)
mFe2O3 = 160 x 0,8 = 128 (g)
b,
theo pt (1)
nH2 = (0,4 x 3)/2 = 0,6 (mol)
=) VH2 = 0,6 x 22,4 = 13,44 (L)
c,
PTHH
Zn + H2SO4 -------------) ZnSO4 + H2 (2)
Số mol H2 cần dùng là 0,6 (mol)
Theo PT (2) :
nZn = nH2 ==) nZn = 0,6 x 65 = 39 (g)
Đúng 0
Bình luận (1)
































