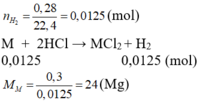cho 4,8g 1 kim loại hóa trị 2 tác dụng với dung dịch HCl sau phản ứng thu đc 4,48 lít H2(đktc).kim loại đó là

Những câu hỏi liên quan
1a, Cho 4,8g một kim loại hóa trị 2 phản ứng hết với dung dịch HCL dư, thu được 2,688lits H2(đktc). Xác định tên kim loại và khối lượng muối thu được sau phản ứng
1b, Cho 2,4g kim loại Mg tác dụng hết với đ HCL dư được V lít H2 ở đktc. Tính giá tri của V và khối lượng muối thu được sau phản ứng
1a)
nH2 = 2.688/22.4 = 0.12 (mol)
M + 2HCl => MCl2 + H2
0.12..............0.12......0.12
MM = 4.8/0.12 = 40
=> M là : Ca
mCaCl2 = 0.12 * 111 = 13.32 (g)
Đúng 1
Bình luận (0)
1b)
nMg = 2.4/24 = 0.1 (mol)
Mg + 2HCl => MgCl2 + H2
0.1....................0.1.........0.1
VH2 = 0.1*22.4 = 2.24 (l)
mMgCl2 = 0.1*95 = 9.5 (g)
Đúng 1
Bình luận (0)
1b)
nMg=0,2(mol)
PTHH: Mg + 2 HCl -> MgCl2 + H2
nH2=nMgCl2=nMg=0,2(mol)
=> nHCl=2.0,2=0,4(mol)
=> V=V(H2,đktc)=0,2.22,4=4,48(l)
mMgCl2=95. 0,2=19(g)
Đúng 0
Bình luận (2)
hòa tan 4,8g một kim loại hóa trị II bằng dung dịch HCL sau phản ứng ta thu được 4,48 lít khí hidro ở đktc. Kim loại hóa trị II đó là gì ?
Gọi KL cần tìm là A.
PT: \(A+2HCl\rightarrow ACl_2+H_2\)
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT: \(n_A=n_{H_2}=0,2\left(mol\right)\Rightarrow M_A=\dfrac{4,8}{0,2}=24\left(g/mol\right)\)
Vậy: KL cần tìm là Mg.
Đúng 2
Bình luận (0)
\(\text{Gọi M là kim loại hóa trị II}\)
\(M+2HCl\rightarrow MCl_2+H_2\)
\(1mol\) \(1mol\)
\(0,2mol\) \(0,2mol\)
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(M_M=\dfrac{m}{n}=\dfrac{4,8}{0,2}=24\)
\(\text{Vậy kim loại hóa trị II là Magie(Mg)}\)
Đúng 0
Bình luận (0)
Cho 4,8 gam một kim loại hóa trị II phản ứng hết với dung dịch HCl dư, thu được 4,48 lít H2 (đktc). Kim loại đó là ?
A. Ba
B. Ca
C. Mg
D. Sr
Đáp án C
Gọi kim loại là R.
![]() = 0,2 (mol)
= 0,2 (mol)
R + 2HCl → RCl2 + H2
0,2 ← 0,2 (mol)
![]() = 24(Mg)
= 24(Mg)
Đúng 0
Bình luận (0)
cho 2,4g kim loại hóa trị II tác dụng với dung dịch HCl lấy dư, sau khi phản ứng kết thức thu được 2,24 lít khí H2 (ở đktc) xác định tên kim loại?
cho 2,7g kim loại hóa trị III tác dụng với dung dịch H2SO4 lấy dư, sau khi phản ứng kết thúc thu được 3,36 lí khia H2 (ở đktc) xác định tenn kim loại?
Bài 1 :
$R + 2HCl \to RCl_2 + H_2$
n R = n H2 = 2,24/22,4 = 0,1(mol)
M R = 2,4/0,1 = 24(Mg) - Magie
Bài 2 :
$2R + 6HCl \to 2RCl_3 + 3H_2$
n H2 = 3,36/22,4 = 0,15(mol)
n R = 2/3 n H2 = 0,1(mol)
M R = 2,7/0,1 = 27(Al) - Nhôm
Đúng 3
Bình luận (0)
Cho 2,4 gam kim loại hóa trị II tác dụng với dung dịch HCl lấy dư , sau khi phản ứng kết thúc thu được 2,24 lít H2 (đktc) . Xác định kim loại ?
PTHH: \(R+2HCl\rightarrow RCl_2+H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)=n_R\)
\(\Rightarrow M_R=\dfrac{2,4}{0,1}=24\) (Magie)
Đúng 5
Bình luận (1)
cho 4,8 gam kim loại m tác dụng hết với dung dịch axit HCL Sau phản ứng thu được 4,48 lít khí H2 (đktc). xác định kim loại M và tính khối lượng muối thu được sau phản ứng
Giả sử KL có hóa trị n.
PT: \(2M+2nHCl\rightarrow2MCl_n+nH_2\)
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT: \(n_M=\dfrac{2}{n}nH_2=\dfrac{0,4}{n}\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{4,8}{\dfrac{0,4}{n}}=12n\left(g/mol\right)\)
Với n = 2 thì MM = 24 (g/mol) là tm
Vậy: M là Mg.
Ta có: \(n_{MgCl_2}=n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
\(\Rightarrow m_{MgCl_2}=0,2.95=19\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 16,2 gam kim loại M (hóa trị không đổi) tác dụng với 0,15 mol oxi. Chất rắn sau phản ứng cho hòa tan hoàn toàn vào dung dịch HCL dư, thu được 13,44 lít H2 (đktc). Biết các phản ứng xảy ra hoàn toàn. Kim loại M là A. Ca B. Zn C. Al D. Mg
Đọc tiếp
Cho 16,2 gam kim loại M (hóa trị không đổi) tác dụng với 0,15 mol oxi. Chất rắn sau phản ứng cho hòa tan hoàn toàn vào dung dịch HCL dư, thu được 13,44 lít H2 (đktc). Biết các phản ứng xảy ra hoàn toàn. Kim loại M là
A. Ca
B. Zn
C. Al
D. Mg
Đáp án C
Các phương trình phản ứng :
M tác dụng với O2: 4 M + 2 n O 2 → t 0 2 M n O n
Chất rắn sau phản ứng tác dụng với dung dịch HCl thu được khí H2, chứng tỏ chất rắn sau có M dư nên O2 hết - chất rắn sau gồm M dư và M2On :
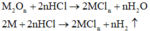
Tính toán:
Số mol H2 thu được là: n H 2 = 13 , 44 22 , 4 = 0 , 6 m o l
Sơ đồ phản ứng:
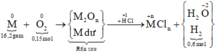
Các quá trình nhường, nhận electron cho cả quá trình:
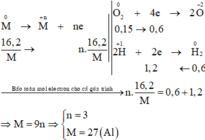
Đúng 0
Bình luận (0)
Cho 0,3gam một kim loại hóa trị II phản ứng hết với dung dịch HCl dư, thu được 0,28 lít H2 (đktc). Kim loại đó là?
A. Ba
B. Ca
C. Mg
D. Sr
Cho 13 g kim loại hóa trị 2 tác dụng với dung dịch H2 SO4 thu được 4,48 lít khí (đktc) .xác định kim loại
Đặt KL là R
\(R+H_2SO_4\to RSO_4+H_2\\ \Rightarrow n_R=n_{H_2}=\dfrac{4,48}{22,4}=0,2(mol)\\ \Rightarrow M_R=\dfrac{13}{0,2}=65(g/mol)\)
Vậy KL là kẽm (Zn)
Đúng 2
Bình luận (0)