Tìm công thức của muối sắt clorua biết rằng khi hòa tan 3,25g muối này vào dung dịch bạc nitrat dư thì thu được 8,61g kết tủa.
Giúp e nhanh vs ạ !
Gọi công thức tổng quát của muối sắt đó là FeClx
mFeClx=3.25(g)
FeClx+xAgNO3->Fe(NO3)x+xAgCl
nAgCl=0.06(mol)
->nFeClx(tính theo AgCl)=0.06/x
->mFeClx=(56+35.5x)*\(\frac{0.06}{x}\)
Ta có mFeClx=3.25(g)
->(56+35.5x)*\(\frac{0.06}{x}\)=3.25
\(\frac{3.36+2.13x}{x}\)=3.25
<->3.36+2.13x=3.25x
<->3.36=1.12x
->x=3
->Công thức của muối sắt đó là FeCl3
Tìm CTHH của muối sắt clorua, biết rằng khi hòa tan 3,25g muối này vào dung dịch AgNO3 dư thì thu được 8,61g kết tủa
gọi công thúc hóa học của muối sắt clorua là FeClx với x là hóa trị của sắt trong muối săt clorua này ta có khi cho muối sắt clorua pư với dd AgNO3 ta có pthh:
FeClx+xAgNO3\(\rightarrow\)Fe(NO3)x+xAgCl(1)
theo pthh(1) và đề bài ta có: nAgCl=8,61:143,5=0,06(mol)
và theo pthh(1) ta lại có:\(\dfrac{3,25}{35,5\times x+56}\)=\(\dfrac{0,06}{x}\)
\(\Rightarrow\)3,25\(\times\)x=2,13\(\times\)x+3,36
hay x=3,36:(3,25-2,13)=3
vậy cthh của muối sắt clorua là FeCl3
\(n_{\downarrow}=0,06\left(mol\right)\)
\(FeCl_x+xAgNO_3->Fe\left(NO_3\right)_x+xAgCl\)
0,06/x........................................................0,06
\(M_{FeCl_x}=\dfrac{3,25}{\dfrac{0,06}{x}}=56+35,5x\)
=> x=3
CTHH FeCl3
Cho 10g dung dịch muối sắt clorua 32,5% tác dụng với dung dịch bạc nitrat dư thì tạo thành 8,61g kết tủa.
a)Hãy tìm công thức hóa học của muối sắt đã dùng ?
b)Cần bao nhiêu ml dung dịch natri hidroxit chứa 0.02 gam NaOH trong 1ml dung dịch để chuyển 1.25gam FeCl3.6H2O thành Fe(OH)3
ai đó giúp mình vớii, mình đang cần gấp:")
Gọi CTHH của muối sắt clorua là \(FeCl_x\) (x là hóa trị của Fe)
\(m_{FeCl_x}=\dfrac{10.32,5\%}{100\%}=3,25\left(g\right)\)
\(FeCl_x+xAgNO_3\rightarrow Fe\left(NO_3\right)_x+xAgCl\)
3,25 (g) 8,61 (g)
Ta có:
\(8,61\left(56+35,5x\right)=3,25\left(108x+35,5x\right)\)
\(\Rightarrow x=3\)
a. CTHH của muối sắt đã dùng là \(FeCl_3\)
b. Trong \(1,25\left(g\right)FeCl_3.6H_2O\) có:
\(n_{FeCl_3.6H_2O}=\dfrac{1,25}{270,5}=\dfrac{5}{1082}\left(mol\right)\)
\(FeCl_3.6H_2O+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl+6H_2O\)
\(\dfrac{5}{1082}\)---------->\(\dfrac{3.5}{1082}\)
\(m_{NaOH}=\dfrac{3.5}{1082}.40=\dfrac{300}{541}\left(g\right)\)
\(V_{NaOH}=\dfrac{300}{541}:0,02=27,73\left(ml\right)\)
Bài 17. Cho 10 gam dung dịch muối sắt clorua 32,5% tác dụng với dung dịch bạc nitrat dư thì tạo thành 8,61 gam chất kết tủa. Hãy tìm công thức hóa học của muối sắt đã dùng.
\(m_{FeCl_x}=\dfrac{10.32,5}{100}=3,25\left(g\right)\)
PTHH: FeClx + 3AgNO3 --> Fe(NO3)3 + xAgCl + (3-x)Ag
_______a------------------------------->ax--------->(3-x)a
=> 143,5ax + 108(3-x)a = 8,61
=> a(35,5x + 324) = 8,61
=> \(a=\dfrac{8,61}{35,5x+324}\)
=> \(M_{FeCl_x}=56+35,5x=\dfrac{3,25}{\dfrac{8,61}{35,5x+324}}\)
=> x = 3
=> CTHH: FeCl3
Cho 10g dung dịch muối sắt clorua 32,5% tác dụng với dung dịch bạc nitrat dư thì tạo thành 8,61g kết tủa. Hãy tìm công thức hóa học của muối sắt đã dùng.
PTHH: FeCla + aAgNO3 --> Fe(NO3)a + aAgCl
Ta có: mFeClamFeCla = 10.32,5% = 3,25g
nAgClnAgCl = 8,61143,58,61143,5 = 0,06 mol
Cứ 1 mol FeCla --> a mol AgCl
56 + 35,5a (g) --> a mol
3,25 (g) --> 0,06 mol
=> 0,06. ( 56 + 35,5a ) = 3,25a
=> 3,36 + 2,13a = 3,25a
=> 1,12a = 3,36 => a = 3
=> CTHH của muối sắt là FeCl3
Cho 10g dung dịch muối sắt clorua 32,5% tác dụng với dung dịch bạc nitrat dư thì tạo thành 8,61g kết tủa. Hãy tìm công thức hóa học của muối sắt đã dùng.
Gọi CTHH của muối sắt là FeCln
FeCln + nAgNO3 → Fe(NO3)n + nAgCl↓
\(m_{FeCl_n}=10\times32,5\%=3,25\left(g\right)\)
\(n_{AgCl}=\dfrac{8,61}{143,5}=0,06\left(mol\right)\)
Theo PT: \(n_{FeCl_n}=\dfrac{1}{n}n_{AgCl}=\dfrac{1}{n}\times0,06=\dfrac{0,06}{n}\left(mol\right)\)
\(\Rightarrow M_{FeCl_n}=3,25\div\dfrac{0,06}{n}=\dfrac{325}{6}n\left(g\right)\)
\(\Leftrightarrow56+35,5n=\dfrac{325}{6}n\)
\(\Leftrightarrow56=\dfrac{56}{3}n\)
\(\Leftrightarrow n=3\)
Vậy CTHH của muối sắt đã dùng là FeCl3
Xác định công thức hóa học và gọi tên muối sắt clorua. Biết khi cho 9,75g muối này tác dụng hết với dung dịch AgNO3 dư thì thu được 25,83g kết tủa.
n AgCl = \(\dfrac{25,83}{143,5}=0,18\) ( mol )
FeCly + AgNO3 → Fe(NO3)y + AgCl ↓
( mol ) \(\dfrac{0,18}{y}\) ← 0,18
m FeCly = \(\dfrac{0,18}{y}+\left(56+35,5y\right)=9,75\)
\(\Leftrightarrow\dfrac{10,08}{y}+6,39=9,75\)
\(\Leftrightarrow\dfrac{10,08}{y}=3,36\)
\(\Leftrightarrow10,08=3,36y\)
\(\Leftrightarrow\dfrac{10,08}{3,36}=3\)
Cồn thức hóa học của muối sắt là: FeCl3
Hoà tan trong nước 0,325g một hỗn hợp gồm 2 muối Natriclorua và Kaliclorua. Thêm vào dung dịch này một dung dịch bạc Nitrat lấy dư - Kết tủa bạc clorua thu được có khối lượng là 0,717g. Tính thành phần phần trăm của mỗi chất trong hỗn hợp.
n NaCl = a(mol) ; n KCl = b(mol)
=> 58,5a + 74,5b = 0,325(1)
NaCl + AgNO3 → AgCl + NaNO3
KCl + AgNO3 → AgCl + KNO3
=> n AgCl = a + b = 0,717/143,5 (2)
Từ (1)(2) suy ra a = 0,003 ; b = 0,002
Suy ra
%m NaCl = 0,003.58,5/0,325 .100% = 54%
%m KCl = 100% -54% = 46%
Sửa đề: 0,717 thành 0,7175 cho số đẹp bạn nhé!
PT: \(NaCl+AgNO_3\rightarrow NaNO_3+AgCl_{\downarrow}\)
\(KCl+AgNO_3\rightarrow KNO_3+AgCl_{\downarrow}\)
Giả sử: \(\left\{{}\begin{matrix}n_{NaCl}=x\left(mol\right)\\n_{KCl}=y\left(mol\right)\end{matrix}\right.\)
⇒ 58,5x + 74,5y = 0,325 (1)
Ta có: \(n_{AgCl}=\dfrac{0,7175}{143,5}=0,005\left(mol\right)\)
Theo PT: \(n_{AgCl}=n_{NaCl}+n_{KCl}=x+y\left(mol\right)\)
⇒ x + y = 0,005 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=\dfrac{19}{6400}\left(mol\right)\\y=\dfrac{13}{6400}\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{NaCl}=\dfrac{\dfrac{19}{6400}.58,5}{0,325}.100\%\approx53,4\%\\\%m_{KCl}\approx46,6\%\end{matrix}\right.\)
Bạn tham khảo nhé!
Hoà tan trong nước 0,325g một hỗn hợp gồm 2 muối Natriclorua và Kaliclorua. Thêm vào dung dịch này một dung dịch bạc Nitrat lấy dư - Kết tủa bạc clorua thu được có khối lượng là 0,717g. Tính thành phần phần trăm của mỗi chất trong hỗn hợp.
PTHH: NaCl + AgNO3 -> AgCl ¯ + NaNO3
KCl + AgNO3 -> AgCl ¯ + KNO3
Dựa vào 2 PTHH ta tìm được khối lượng của AgCl trong mỗi phản ứng:
m'AgCl = x .= x . = x . 2,444
mAgCl = y .= y . = y . 1,919
=> mAgCl = 2,444x + 1,919y = 0,717 (2)
Từ (1) và (2) => hệ phương trình
Giải hệ phương trình ta được: x = 0,178
y = 0,147
=> % NaCl = .100% = 54,76%
% KCl = 100% - % NaCl = 100% - 54,76% = 45,24%.
Vậy trong hỗn hợp: NaCl chiếm 54,76%, KCl chiếm 45,24%
ọi MNaCl là x và mKcl là y ta có phương trình đại số:
x + y = 0,35 (1)
PTHH: NaCl + AgNO3 -> AgCl ¯ + NaNO3
KCl + AgNO3 -> AgCl ¯ + KNO3
Dựa vào 2 PTHH ta tìm được khối lượng của AgCl trong mỗi phản ứng:
m'AgCl = x .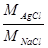 = x .
= x .  = x . 2,444
= x . 2,444
mAgCl = y .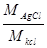 = y .
= y . 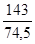 = y . 1,919
= y . 1,919
=> mAgCl = 2,444x + 1,919y = 0,717 (2)
Từ (1) và (2) => hệ phương trình 
Giải hệ phương trình ta được: x = 0,178
y = 0,147
=> % NaCl = 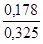 .100% = 54,76%
.100% = 54,76%
% KCl = 100% - % NaCl = 100% - 54,76% = 45,24%.
Vậy trong hỗn hợp: NaCl chiếm 54,76%, KCl chiếm 45,24%