Rót 100ml dung dịch HCl 2M vào 250ml dung dịch Ca(OH)2 0,5M.Tính nồng độ mol của dung dịch sau phản ứng

Những câu hỏi liên quan
cho 100ml dung dịch NaOH 2M tác dụng với 100ml dung dịch HCl, sau phản ứng thu được dung dịch chứa 10,775 gam chất tan. Nồng độ mol của dung dịch HCL là?
hòa tan hoàn toàn 6,5g Zn vào 100ml dung dịch HCl
a) tính thể tích khí hiđro thoát ra (đktc)
b) tính nồng độ mol dung dịch HCl đã phản ứng
c) nếu dùng 50ml dung dịch HCl trên trung hòa V ml dung dịch Ca(OH)2 2M tính V?
Trung hòa 100ml dung dịch KOH 2M bằng V ml dung dịch HCl 2M. a) Viết phương trình phản ứng ? b) Tính V ? c) Tính nồng độ mol của dung dịch thu được sau phản ứng ?
\(a,PTHH:KOH+HCl\rightarrow KCl+H_2O\\ b,n_{KOH}=n_{HCl}=2\cdot0,1=0,2\left(mol\right)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,2}{2}=0,1\left(l\right)\\ c,C_{M_{KCl}}=\dfrac{0,2}{0,1+0,1}=1M\)
Đúng 2
Bình luận (1)
Đổi 100ml = 0,1 lít
Ta có: \(n_{KOH}=2.0,1=0,2\left(mol\right)\)
a. PTHH: \(KOH+HCl--->KCl+H_2O\)
b. Theo PT: \(n_{HCl}=n_{KOH}=0,2\left(mol\right)\)
\(\Rightarrow V_{dd_{HCl}}=\dfrac{0,2}{2}=0,1\left(lít\right)=100\left(ml\right)\)
c. Ta có: \(V_{dd_{KCl}}=V_{dd_{HCl}}=0,1\left(lít\right)\)
Theo PT: \(n_{KCl}=n_{HCl}=0,2\left(mol\right)\)
\(\Rightarrow C_{M_{KCl}}=\dfrac{0,2}{0,1}=2M\)
Đúng 0
Bình luận (2)
Giải giúp mình 2 câu nhé:
1) Tính nồng độ mol/lit của các ion trong dung dịch
a)Ion K+ và SO4 2- trong dung dịch K2SO4 0,05M
b)Ion Ba 2+ và OH- trong dung dịch Ba(OH)2 0,02M
c)Ion H+ và NO3 - trong 100ml dung dịch HNO3 nồng độ 10% (D=1,054g/ml)
2) Cho 150 ml dung dịch KOH 2M vào 250ml dung dịch HCl 3M. Tính nông độ mol/lit của các ion trong dung dịch sau phản ứng
2)
nKOH = 0.15*2=0.3 mol
nHCl = 0.25*3=0.75 mol
KOH + HCl --> KCl + H2O
Bđ: 0.3____0.45
Pư : 0.3____0.3____0.3
Kt: 0______0.15___0.3
DD sau phản ứng : 0.15 mol HCl dư , 0.3 mol KCl
CM H+= 0.15/0.25=0.6M
CM Cl- = 0.15/0.25=0.6 M
CM K+= 0.3/(0.15+0.25)=0.75M
CM Cl-= 0.3/(0.15+0.25)= 0.75M
Đúng 0
Bình luận (2)
Cho 100ml dung dịch HCl 1M tác dụng với v ml dung dịch Ca(OH)2 1M. Tính
a/ v ml dung dịch Ca(OH)2 cần dùng
b/ nồng độ mol dung dịch sau phản ứng
c/ nếu cô cạn dung dịch sau phản ứng thì được bao nhiêu gam muôi khan.
nHCl=0,1(mol)
PT: 2HCl + Ca(OH)2 -> CaCl2 + 2H2O
vậy: 0,1-------->0,05--------->0,05(mol)
=> VCa(OH)2=n/CM=0,05/1=0,05(lít)=50 ml
b) Vd d sau phản ứng=0,1+0,05=0,15(lít)
=> CM CaCl2=n/V=0,05/0,15=0,33(M)
c) mCaCl2=n.M=0,05.111=5,55(g)
Đúng 0
Bình luận (0)
Ca(OH)2 + 2HCl -> CaCl2 + 2H2O
nHCl=0,1(mol)
Theo PTHH ta có:
nCa(OH)2=\(\dfrac{1}{2}\)nHCl=0,05(mol)
nCaCl2=nCa(OH)2=0,05(mol)
Vdd Ca(OH)2=\(\dfrac{0,05}{1}=0,05\left(lít\right)\)
mCaCl2=111.0,05=5,55(g)
CM dd CaCl2=\(\dfrac{0,05}{0,15}=\dfrac{1}{3}M\)
Đúng 0
Bình luận (0)
a) nHCl=0.1*1=0.1(mol)
Ta có phương trình sau
2 HCl + Ca(OH)2 ➞ CaCl2 + 2 H2O
....0.1........0.05............0.1..........................(mol)
V=0.05/1=0.05(l)=50ml
b)CM (CaCl2)=0.1/(0.1+0.05)=2/3(M)
c)mCaCl2=111*0.1=11.1(g)
Đúng 0
Bình luận (0)
Nhỏ 200ml dung dịch NaOH 2M vào 100ml dung dịch HCl 1M. Tính nồng độ mol/lít của dung dịch sau phản ứng.
X là dung dịch HCl nồng độ x mol/lít. Y là dung dịch Na2CO3 nồng độ y mol/lít. Nhỏ từ từ 100ml dung dịch X vào 100ml Y, sau các phản ứng thu được V1 lít CO2 (đktc). Nhỏ từ từ 100ml dung dịch Y vào 100ml dung dịch X, sau phản ứng thu được V2 lít CO2 (đktc). Biết tỉ lệ V1 : V2 4 : 7. Tỉ lệ x : y bằng A. 11 : 4 B. 11 : 7 C. 7 : 5 D. 7 : 3
Đọc tiếp
X là dung dịch HCl nồng độ x mol/lít. Y là dung dịch Na2CO3 nồng độ y mol/lít. Nhỏ từ từ 100ml dung dịch X vào 100ml Y, sau các phản ứng thu được V1 lít CO2 (đktc). Nhỏ từ từ 100ml dung dịch Y vào 100ml dung dịch X, sau phản ứng thu được V2 lít CO2 (đktc). Biết tỉ lệ V1 : V2 = 4 : 7. Tỉ lệ x : y bằng
A. 11 : 4
B. 11 : 7
C. 7 : 5
D. 7 : 3
Đáp án C
Trường hợp 1: Khi nhỏ từ từ axit vào dung dịch muối cacbonat, phản ứng xảy ra theo trình từ
H+ + CO32- → HCO3-
Sau đó H+còn dư + HCO3- → CO2 + H2O
=> nCO2 = nH+ – nCO32- = 0,1(x – y)
Trường hợp 2: Khi nhỏ từ từ muối cacbonat vào axit thì phản ứng tạo ra ngay CO2:
2H+ + CO32- → CO2 + H2O
nCO2 = ½ nH+ = 0,05x
Do V1 : V2 = 4 : 7
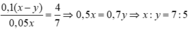
Đúng 0
Bình luận (0)
X là dung dịch HCl nồng độ x mol/lít. Y là dung dịch Na2CO3 nồng độ y mol/lít. Nhỏ từ từ 100ml dung dịch X vào 100ml Y, sau các phản ứng thu được V1 lít CO2 (đktc). Nhỏ từ từ 100ml dung dịch Y vào 100ml dung dịch X, sau phản ứng thu được V2 lít CO2 (đktc). Biết tỉ lệ V1 : V2 4 : 7. Tỉ lệ x : y bằng A. 11 : 4. B. 11 : 7. C. 7 : 5. D. 7 : 3.
Đọc tiếp
X là dung dịch HCl nồng độ x mol/lít. Y là dung dịch Na2CO3 nồng độ y mol/lít. Nhỏ từ từ 100ml dung dịch X vào 100ml Y, sau các phản ứng thu được V1 lít CO2 (đktc). Nhỏ từ từ 100ml dung dịch Y vào 100ml dung dịch X, sau phản ứng thu được V2 lít CO2 (đktc). Biết tỉ lệ V1 : V2 = 4 : 7. Tỉ lệ x : y bằng
A. 11 : 4.
B. 11 : 7.
C. 7 : 5.
D. 7 : 3.
Trường hợp 1: Khi nhỏ từ từ axit vào dung dịch muối cacbonat, phản ứng xảy ra theo trình từ
H+ + CO32- → HCO3-
Sau đó H+còn dư + HCO3- → CO2 + H2O
→ nCO2 = nH+ – nCO32- = 0,1(x – y)
Trường hợp 2: Khi nhỏ từ từ muối cacbonat vào axit thì phản ứng tạo ra ngay CO2:
2H+ + CO32- → CO2 + H2O
nCO2 = ½ nH+ = 0,05x
Do V1 : V2 = 4 : 7
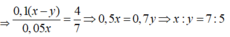
Đáp án C
Đúng 0
Bình luận (0)
Cho 300ml dung dịch HNO3 1M vào 100ml dung dịch Ba(OH)2 1M. Sau phản ứng hoàn toàn thu được dung dịch X.
a) Tính nồng độ các chất trong X
b) Cho rất từ từ đến hết 250ml dung dịch Na2CO3 0,5M vào X. Sau khi các phản ứng xảy ra hoàn toàn, thu được V lít khí CO2 (đktc) và m gam kết tủa. Tính V, m =)) ét ô étttttttt
a, \(n_{HNO_3}=0,3.1=0,3\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0,1.1=0,1\left(mol\right)\)
PT: \(2HNO_3+Ba\left(OH\right)_2\rightarrow Ba\left(NO_3\right)_2+2H_2O\)
Xét tỉ lệ: \(\dfrac{0,3}{2}>\dfrac{0,1}{1}\), ta được HNO3 dư.
Theo PT: \(\left\{{}\begin{matrix}n_{Ba\left(NO_3\right)_2}=n_{Ba\left(OH\right)_2}=0,1\left(mol\right)\\n_{HNO_3\left(pư\right)}=2n_{Ba\left(OH\right)_2}=0,2\left(mol\right)\end{matrix}\right.\)
⇒ nHNO3 (dư) = 0,3 - 0,2 = 0,1 (mol)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{Ba\left(NO_3\right)_2}}=\dfrac{0,1}{0,3+0,1}=0,25\left(M\right)\\C_{M_{HNO_3\left(dư\right)}}=\dfrac{0,1}{0,3+0,1}=0,25\left(M\right)\end{matrix}\right.\)
b, Ta có: \(n_{Na_2CO_3}=0,25.0,5=0,125\left(mol\right)\)
PT: \(Na_2CO_3+2HNO_3\rightarrow2NaNO_3+CO_2+H_2O\)
______0,05______0,1_______________0,05 (mol)
⇒ VCO2 = 0,05.22,4 = 1,12 (l)
\(Na_2CO_3+Ba\left(NO_3\right)_2\rightarrow2NaNO_3+BaCO_{3\downarrow}\)
0,075________0,075_______________0,075 (mol)
⇒ mBaCO3 = 0,075.197 = 14,775 (g)
Đúng 1
Bình luận (0)
Cho 2.4 gam M vào 250ml dung dịch HCl 1M. Tính nồng độ mol/l của các ion trong dung dịch sau phản ứng.

























