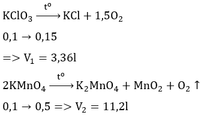Phân hủy 30,8g KMnO4.Tính thể tích oxi thu được ở đktc,biết hiệu suất phản ứng phân hủy là 90%

Những câu hỏi liên quan
Phân hủy 3,6g KMnO4 thu được V lít khí oxi(đktc)
a) viết PTHH xảy ra
b) tính V. Biết hiệu suất phản ứng là 100%
c) nếu hiệu suất của phản ứng là 80% thì sau phản ứng thu được bao nhiêu lít oxi (đktc)
Xem chi tiết
a. PTHH: \(KMnO_4\rightarrow^{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
b. \(H=100\%\)
\(n_{KMnO_4}=\frac{3,6}{158}=0,023mol\)
Theo phương trình \(n_{O_2}=0,5n_{KMnO_4}=0,046mol\)
\(\rightarrow V_{O_2}=0,0115.22,4.100\%=0,2576l\)
c. H = 80%
\(\rightarrow V_{O_2}=0,0115.22,4.80\%=0,20608l\)
Khi phân hủy có xúc tác 122,5g Kaliclorat (KClO3) thể tích khí oxi (đktc) thu được là :
A. 48 lít
B. 24,5 lít
C. 67,2 lít
D. 33,6 lít
Nhiệt phân hoàn toàn 31,6 gam KMnO4, thu được V lít O2 (đktc), biết hiệu suất phản ứng 80% . Giá trị của V là
A. 2,24
B. 1,792
C. 10,08
D. 8,96
Xem thêm câu trả lời
Tính khối lượng KMnO4 cần dùng để điều chế được lượng oxi là 11,2 lít , biết hiệu suất phản ứng phân hủy đạt 80% (các chất khí đo ở đktc)
\(n_{O_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
1<------------------------------------0,5
=> \(m_{KMnO_4\left(pthh\right)}=1.158=158\left(g\right)\)
=> \(m_{KMnO_4\left(tt\right)}=\dfrac{158.100}{80}=197,5\left(g\right)\)
Đúng 2
Bình luận (0)
Phân hủy 49 gam kali clorat ở nhiệt độ cao sau phản ứng thu được V lít oxi (ở đktc).a/ Tính V biết hiệu suất phản ứng bằng 75%.b/ Cho oxi thu được ở trên tác dụng với Mg sau phản ứng thu được magie oxit.- Tính khối lượng magie phản ứng biết phản ứng xảy ra với hiệu suất 70%- Tính khối lượng magie oxit tạo thành bằng nhiều cách.
Đọc tiếp
Phân hủy 49 gam kali clorat ở nhiệt độ cao sau phản ứng thu được V lít oxi (ở đktc).
a/ Tính V biết hiệu suất phản ứng bằng 75%.
b/ Cho oxi thu được ở trên tác dụng với Mg sau phản ứng thu được magie oxit.
- Tính khối lượng magie phản ứng biết phản ứng xảy ra với hiệu suất 70%
- Tính khối lượng magie oxit tạo thành bằng nhiều cách.
để điều chế được 6,72 lít khí oxi cần phân hủy bao nhiêu gam KMnO4 biết hiệu suất phân hủy là 90%
2KMnO4-to>K2MnO4+MnO2+O2
0,6------------------------------------0,3 mol
n O2=\(\dfrac{6,72}{22,4}\)=0,3 mol
=>m KMnO4pứ=0,6.158.\(\dfrac{100}{90}\)=105,33g
Đúng 9
Bình luận (0)
nhiệt phân 15 gam KClO3 tính thể tích khí oxi thu được ở đktc biết hiệu suất phản ứng đạt 90%
\(m_{KClO_3\left(pư\right)}=\dfrac{15.90}{100}=13,5\left(g\right)\)
=> \(n_{KClO_3\left(pư\right)}=\dfrac{13,5}{122,5}=\dfrac{27}{245}\left(mol\right)\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
\(\dfrac{27}{245}\)----------------->\(\dfrac{81}{490}\)
=> \(V_{O_2}=\dfrac{81}{490}.22,4=\dfrac{648}{175}\left(l\right)\)
Đúng 2
Bình luận (0)
\(n_{KClO_3}=\dfrac{m_{KClO_3}}{M_{KClO_3}}=\dfrac{15}{122,5}=\dfrac{6}{49}mol\)
\(n_{KClO_3}=\dfrac{6}{49}:90\%=\dfrac{20}{147}mol\)
\(2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\)
20/147 10/49 ( mol )
\(V_{O_2}=n_{O_2}.22,4=\dfrac{10}{49}.22,4=4,5714l\)
Đúng 1
Bình luận (1)
Trong phòng thí nghiệm có thể dùng muối KClO3 hoặc KMnO4 để điều chế oxi bằng phản ứng phân hủy. Viết phương trình hóa học của các phản ứng và tính thể tích khí oxi thu được (đktc) khi nhiệt phân hoàn toàn 0,1 mol mỗi chất trên.
C1: trong phòng thí nghiệm, ng ta điều chế oxi bằng cách phân hủy hoàn toàn 15.8g KMnO4 a) Viết Phương trình phản ứng B) tính thể tích oxi điều chế đc(đktc)? C) tính khối lượng sắt cần dùng để phản ứng hết vs thể tích khí oxi thu đc hết ở trên
a) $2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
b) n KMnO4 = 15,8/158 = 0,1(mol)
Theo PTHH : n O2 = 1/2 n KMnO4 = 0,05(mol)
=> V O2 = 0,05.22,4 = 1,12(lít)
c)
$3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$
Theo PTHH : n Fe = 3/2 nO2 = 0,075(mol)
=> m Fe = 0,075.56 = 4,2(gam)
Đúng 2
Bình luận (0)
Theo gt ta có: $n_{KMnO_4}=0,1(mol)$
a, $2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2$
b, Ta có: $n_{O_2}=0,05(mol)\Rightarrow V_{O_2}=1,12(mol)$
c, $3Fe+2O_2\rightarrow Fe_3O_4$
Ta có: $n_{Fe}=0,075(mol)\Rightarrow m_{Fe}=4,2(g)$
Đúng 1
Bình luận (0)
Đung nóng 15,8g kali pemanganat(thuốc tím) K M n O 4 trong ống nghiệm để điều chế khí oxi. Biết rằng, chất rắn còn lại trong ống nghiệm có khối lượng 12,6g; khối lượng khí oxi thu được là 2,8g. Tính hiệu suất của phản ứng phân hủy.
Theo định luật bảo toàn khối lượng ta có: m O 2 = 15,8 – 12,6 = 3,2(g)
Hiệu suất của phản ứng phân hủy: H = 2,8/3,2 x 100 = 87,5%
Đúng 0
Bình luận (0)