cho 6,5g kim loại R(hóa trị 2) tác dụng với hcl sinh ra 2,24l khí(đktc) xác định tên kim loại đó

Những câu hỏi liên quan
Cho 10,8g kim loại R có hóa trị III tác dụng với dung dịch HCl thấy tạo thành 53,4g muối.
a) Xác định tên loại R đó.
b) Cho 13,5g kim loại R trên tan hoàn toàn trong dung dịch axit HCl 0,5M. Tính: thể tích khí H2 thoát ra(đktc); thế tích dung dịch HCl cần dùng ?
*trình bày chi tiết giúp mình với ạ
\(PTHH:2R+6HCl\rightarrow2RCl_3+3H_2\)
\(TheoPTHH:n_R=n_M=\dfrac{10,8}{R}=\dfrac{53,4}{R+35,5.3}\)
\(\Rightarrow R=27\)
=> Kim loại đó là Nhôm
b, \(TheoPTHH:n_{HCl}=3n_R=1,5mol\)
\(\Rightarrow V_{HCl}=3l\)
Theo PTHH : \(n_{H2}=\dfrac{3}{2}n_{Al}=0,75mol\)
\(\Rightarrow V=n.22,4=16,8l\)
Đúng 1
Bình luận (1)
\(2M+6HCl\rightarrow2MCl_3+3H_2\)
\(2M...........2\cdot\left(M+106.5\right)\)
\(10.8..................53.4\)
\(53.4\cdot2M=10.8\cdot\cdot2\left(M+106.5\right)\)
\(\Rightarrow M=27\)
\(M:Nhôm\)
\(n_{Al}=\dfrac{13.5}{27}=0.5\left(mol\right)\)
\(V_{H_2}=0.5\cdot\dfrac{3}{2}\cdot22.4=16.8\left(l\right)\)
\(V_{dd_{HCl}}=\dfrac{0.5\cdot6}{2\cdot0.5}=3\left(l\right)\)
Đúng 2
Bình luận (1)
cho 7,8 gam kim loại a(có hóa trị 1) tác dụng hoàn toàn với nc sau phản ứng thu đc 2,24l khí hidro(ở đktc) xác định tên và kí hiệu hóa học của kim loại trên
`2A + 2H_2 O -> 2AOH + H_2`
`0,2` `0,1` `(mol)`
`n_[H_2] = [ 2,24 ] / [ 22,4 ] = 0,1 (mol)`
`=> M_A = [ 7,8 ] / [ 0,2 ] = 39 ( g // mol )`
`=> A` là `K`
Đúng 2
Bình luận (0)
cho 4g 1 kim loại chưa biết hóa trị phản ứng với 400g dd HCL 3.65%? Sau phản ứng đem toàn bộ axit dư tác dụng với Fe thì thấy có 2.24l khí H2 (Đktc) được sinh ra. Xác định tên kim loại?
Bài 1: Cho 5.52g một kim loại kiềm tác dụng với nước tạo ra 2.688 lít khí H2 (đktc). Xác định tên kim loại đó.
Bài 2: Cho 1.84g một kim loại kiềm tác dụng với nước tạo ra 896ml khí H2 (đktc). Xác định tên kim loại đó.
Bài 1:
Gọi kim loại kiềm là R
\(n_{H_2}=\dfrac{2,688}{22,4}=0,12\left(mol\right)\)
Giả sử R hóa trị I:
\(R+H_2O\rightarrow ROH+\dfrac{1}{2}H_2\\ \Rightarrow n_R=0,12.2=0,24\left(mol\right)\\ \Rightarrow M_R=\dfrac{5,52}{0,24}=23\left(đvC\right)\)
Giả sử đúng, tên kim loại đó là sodium (Na)
Bài 2: Tự làm tương tự bài 1 nhé=0
Đúng 2
Bình luận (0)
cho 1,2g kim loại R có hóa trị II tác dụng với dd HCl dư, sau phản ứng thu đc 1,12lit H2(đktc).Xác định tên kim loại R?
\(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: R + 2HCl --> RCl2 + H2
0,05<---------------0,05
=> \(M_R=\dfrac{1,2}{0,05}=24\left(g/mol\right)\)
=> R là Mg (Magie)
Đúng 4
Bình luận (1)
cho 2,5g kim loại R ( hóa trị II) tác dụng với dung dịch H2SO4 loãng thấy giải phóng 2,24l ở đktc và tạo ra muối ( RSO4). Hãy xác định kim loại R
Tính được : \(n_{H2}=0,1\left(mol\right)\)
PTHH :
\(R+H_2SO_4\rightarrow RSO_4+H_2\)
\(1..1...........1........1\)
\(0,1......0,1..........0,1.........0,1\)
\(M_R=\frac{M_R}{M_R}=\frac{2,5}{0,1}=25\) ( g/mol )
Vậy \(R=25\)
Đúng 0
Bình luận (0)
R + H2SO4 ---> RSO4 + H2
nH2 = \(\dfrac{2,24}{22,4}\) = 0,1 mol
TPT : nR = nH2
=> nR = 0,1 mol
=> \(M_R\) = \(\dfrac{2,5}{0,1}\) = 25 đvC
Hình như sai đề bài
Đúng 0
Bình luận (0)
PƯHH:R+H2SO4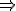 RSO4+H2
RSO4+H2
Ta có:nH2=2,24:22,4=0,1(mol)
Ta lại có:
1 mol R tạo thành 1 mol H2
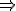 x mol R tạo thành 0,1 mol H2
x mol R tạo thành 0,1 mol H2
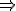 x=0,1(mol)
x=0,1(mol)
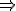 MR=mR:nR=2,5:0,1=25g
MR=mR:nR=2,5:0,1=25g
 không xác định
không xác định
Đúng 0
Bình luận (0)
1. Cho 0,6g một kim loại hóa trị II tác dụng với nước tạo ra 0,336 l khí H2(đktc). Tìm tên kim loại.
2. Cho 4.48g một oxit kim loại hóa trị II, tác dụng hết với 100ml dung dịch H2SO4 0,8M. Xác định tên kim loại.
*trình bày chi tiết giúp mình với ạ
\(n_{H_2}=\dfrac{0.336}{22.4}=0.015\left(mol\right)\)
\(M+2HCl\rightarrow MCl_2+H_2\)
\(0.015........................0.015\)
\(M_M=\dfrac{0.6}{0.015}=40\left(\dfrac{g}{mol}\right)\)
\(M:Canxi\left(Ca\right)\)
Đúng 4
Bình luận (1)
\(n_{H_2SO_4}=0.1\cdot0.8=0.08\left(mol\right)\)
\(M+H_2SO_4\rightarrow MSO_4+H_2\)
\(0.08.....0.08\)
\(M_M=\dfrac{4.48}{0.08}=56\left(\dfrac{g}{mol}\right)\)
\(M:Sắt\left(Fe\right)\)
Đúng 3
Bình luận (1)
1/
nH2=0,336/22,4=0,015(mol)
gọi KL là M.
PTHH:M+2H2O-->M(OH)2+H2(1)
0,015 0,015 (mol)
Từ pt(1)-->nM=0,015(mol)
-->MM=0,6/0,015=40(g/mol)
-->M là Canxi(Ca)
2/
nH2SO4=0,1.0,8=0,08(mol)
gọi KL là R
PTHH:R+H2SO4-->RSO4+H2(2)
0,08 0,08 (mol)
từ pt (2)-->nR=0,08(mol)
-->MR=4,48/0,08=56(g/mol)
-->R là Sắt(Fe)
nhớ tích đúng cho mình nha!
Đúng 12
Bình luận (1)
Câu 1: Cho 13,7 gam một kim loại R có hóa trị 2 khi tác dụng vừa đủ 200ml dung dịch HCl thu được 2,24 lít khí H2 ở (ĐKTC) và dung dịch A. Xác định tên kim loại R và nồng độ HCl đã dùng?
\(n_{H_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(R+2HCl\rightarrow RCl_2+H_2\)
\(0.1........0.2................0.1\)
\(M_R=\dfrac{13.7}{0.1}=137\left(\dfrac{g}{mol}\right)\)
\(R:Ba\)
\(200\left(ml\right)=0.2\left(l\right)\)
\(C_{M_{HCl}}=\dfrac{0.2}{0.2}=1\left(M\right)\)
Đúng 2
Bình luận (0)
Cho 9,6g hỗn hợp MgO và kim loại A hóa trị II tác dụn với dung dịch HCl 10% vừa đủ. Sau phản ứng thu được 2,24l khí (đktc) và 22,2g hỗn hợp muối.
a. Xác định tên kim loại.
b. Tính m dung dịch axit cần dùng.




























