Tính được : \(n_{H2}=0,1\left(mol\right)\)
PTHH :
\(R+H_2SO_4\rightarrow RSO_4+H_2\)
\(1..1...........1........1\)
\(0,1......0,1..........0,1.........0,1\)
\(M_R=\frac{M_R}{M_R}=\frac{2,5}{0,1}=25\) ( g/mol )
Vậy \(R=25\)
R + H2SO4 ---> RSO4 + H2
nH2 = \(\dfrac{2,24}{22,4}\) = 0,1 mol
TPT : nR = nH2
=> nR = 0,1 mol
=> \(M_R\) = \(\dfrac{2,5}{0,1}\) = 25 đvC
Hình như sai đề bài
PƯHH:R+H2SO4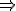 RSO4+H2
RSO4+H2
Ta có:nH2=2,24:22,4=0,1(mol)
Ta lại có:
1 mol R tạo thành 1 mol H2
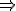 x mol R tạo thành 0,1 mol H2
x mol R tạo thành 0,1 mol H2
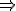 x=0,1(mol)
x=0,1(mol)
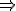 MR=mR:nR=2,5:0,1=25g
MR=mR:nR=2,5:0,1=25g
 không xác định
không xác định













