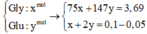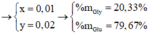Hỗn hợp gồm ZnO và MgO nặng 0,3g cho tan trong 17 ml HCl 1M. Phản ứng trung hòa lượng axit dư cần 8 ml NaOH 0,5M. Tính phần trăm theo khối lượng mỗi axit

Những câu hỏi liên quan
Hỗn hợp X gồm ZnO và MgO nặng 0,3g đem hòa tan hết trong 17ml HCL 1M sau phản ứng để trung hòa HCl còn dư cần dùng 8ml NaOH 0,5M tính khối lượng mỗi chất trong hỗn hợp ban đầu
nHCl = 0,017 mol
nNaOH = 0,004 mol
NaOH (0,004) + HCldư (0,004) ------> NaCl + H2O (1)
- Theo PTHH(1): = > nHCl dư = 0,004 mol
=> nHCl phản ứng = 0,017 - 0,004 = 0,013 mol
Gọi nZnO là x thì nMgO là y
=> 81x + 40y = 0,3 (I)
ZnO (x) + 2HCl (2x) -------> ZnCl2 + H2O (2)
MgO (y) + 2HCl (2y) -------> MgCl2 + H2O (3)
-Theo PTHH(1,2) => nHCl = 2x +2y = 0,013 (II)
- Giải hệ PT(I,II) => \(\left\{{}\begin{matrix}x=\dfrac{1}{1025}\left(mol\right)\\y=\dfrac{453}{82000}\left(mol\right)\end{matrix}\right.\)
=> mZnO = \(\dfrac{1}{1025}.81=\dfrac{81}{1025}\left(gam\right)\)
=> mMgO = \(\dfrac{453}{82000}.40=\dfrac{453}{2050}\left(gam\right)\)
Đúng 1
Bình luận (0)
PT: \(ZnO+2HCl\rightarrow ZnCl_2+H_2O\) (1)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\) (2)
\(HCl+NaOH\rightarrow NaCl+H_2O\) (3)
Số mol NaOH cần dùng để trung hòa HCl dư là:
\(n_{NaOH}=0,008.0,5=0,004\left(mol\right)\)
Theo pt (3): \(n_{NaOH}=n_{HCl}=0,004\left(mol\right)\)
Hay: \(n_{HCl_{dư}}=0,004\left(mol\right)\)
Số mol HCl tham gia pư là :
\(n_{HCl}=0,017.1=0,017\left(mol\right)\)
\(\Rightarrow n_{HCl_{1+2}}=0,017-0,004=0,013\left(mol\right)\)
Giả sử: Số mol ZnO là x(mol)
Số mol MgO là y (mol)
(x,y>0)
\(\Rightarrow m_{ZnO}=81x\left(g\right)\)
\(m_{MgO}=40y\left(g\right)\)
\(\Rightarrow81x+40y=0,3\) (*)
Theo pt (1) : \(n_{HCl_1}=2.n_{ZnO}=2x\left(mol\right)\)
(2) :\(n_{HCl_2}=2.n_{MgO}=2y\left(mol\right)\)
Mà: \(n_{HCl_{1+2}}=0,013\left(mol\right)\)
\(\Rightarrow2x+2y=0,013\) (**)
Từ (*) và (**),ta có hệ phương trình:
\(\left\{{}\begin{matrix}81x+40y=0,3\\2x+2y=0,013\end{matrix}\right.\)
Giải hệ phương trình,ta đc:
\(\left\{{}\begin{matrix}x=\dfrac{1}{1025}\left(mol\right)=n_{ZnO}\\y=\dfrac{453}{82000}\left(mol\right)=n_{MgO}\end{matrix}\right.\)
\(\Rightarrow m_{ZnO}=\dfrac{1}{1025}.81=\dfrac{81}{1025}\left(g\right)\)
\(m_{MgO}=\dfrac{453}{82000}.40=\dfrac{453}{2050}\left(g\right)\)
=.= hok tốt!!
Đúng 1
Bình luận (0)
Hòa tan 12,1 g hỗn hợp gồm Fe và Zn trong 500 ml dung dịch HCl 1M được dung dịch A .Để trung hòa hết lượng axit còn dư trong A cần 50ml dung dịch NaOH 2M .Tính thành phần phần trăm theo khối lượng mỗi kim loại
$NaOH + HCl \to NaCl + H_2O$
$n_{HCl\ dư} = n_{NaOH} = 0,05.2 = 0,1(mol)$
Gọi $n_{Fe} = a ; n_{Zn} = b \Rightarrow 56a + 65b = 12,1(1)$
$Fe + 2HCl \to FeCl_2 + H_2$
$Zn + 2HCl \to ZnCl_2 + H_2$
$n_{HCl} = 2a + 2b = 0,5 -0,1 = 0,4(2)$
Từ (1)(2) suy ra a = b = 0,1
$\%m_{Fe} = \dfrac{0,1.56}{12,1}.100\% = 46,28\%$
$\%m_{Zn} = 100\% -46,28\% = 53,72\%$
Đúng 2
Bình luận (0)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(HCl_{dư}+NaOH\rightarrow NaCl+H_2O\)
Gọi x, y lần lượt là số mol Fe, Zn, theo đề ta có:
\(\left\{{}\begin{matrix}56x+65y=12,1\\2x+2y=0,5.1-0,05.2\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
=> \(\%m_{Fe}=\dfrac{0,1.56}{12,1}=46,28\%\)
=> \(\%m_{Zn}=100-46,28=53,72\%\)
Đúng 3
Bình luận (0)
Hỗn hợp G gồm glyxin và axit glutamic. Cho 3,69 gam hỗn hợp G vào 100 ml dung dịch HCl 0,5M được dung dịch Z. Dung dịch Z phản ứng vừa đủ với 100 ml dung dịch KOH 1M. Thành phần phần trăm theo khối lượng của glyxin và axit glutamic trong hỗn hợp G lần lượt là:
A. 40,65% và 59,35%.
B. 30,49% và 69,51%.
C. 60,17% và 39,83%.
D. 20,33% và 79,67%.
Hoà tan hoàn toàn 8 gam hỗn hợp gồm CuO,Fe2O3, MgO, ZnO trong 400 ml axit H2SO4 0,5M (vừa đủ). Sau phản ứng, hỗn hợp muối sunfat khan thu được khi cô cạn dung dịch có khối lượng là
\(n_{H_2SO_4}=0,4.0,5=0,2\left(mol\right)\)
=> \(n_{H_2O}=0,2\left(mol\right)\)
Theo ĐLBTKL: moxit + mH2SO4 = mmuối + mH2O
=> mmuối = 8 + 0,2.98 - 0,2.18 = 24 (g)
Đúng 2
Bình luận (0)
n H2SO4=0,5.0,4=0,2 mol
=> m muối =8+0,2.96=27,2g
Đúng 3
Bình luận (10)
Trung hòa hoàn toàn 10,6 gam hỗn hợp X gồm axit axetic và axit fomic cần 200 ml dung dịch NaOH 1M. Tính khối lượng mỗi axit trong hỗn hợp ban đầu và tính khối lượng muối thu được.
\(HCOOH+NaOH\rightarrow HCOONa+H_2O\)
\(CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)
\(n_{HCOOH}=a\left(mol\right),n_{CH_3COOH}=b\left(mol\right)\)
\(m_X=46a+60b=10.6\left(g\right)\left(1\right)\)
\(n_{NaOH}=a+b=0.2\left(mol\right)\left(2\right)\)
\(\Rightarrow a=b=0.1\)
\(m_{HCOOH}=0.1\cdot46=4.6\left(g\right)\)
\(m_{CH_3COOH}=6\left(g\right)\)
\(n_{H_2O}=0.2\left(mol\right)\)
\(BTKL:\)
\(m_{Muối}=10.6+0.2\cdot40-0.2\cdot18=15\left(g\right)\)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 2.81 gam hỗn hợp gồm Fe2O3, MgO, ZnO trong 500 ml axit H2SO4 0.1 M (vừa đủ) . Tính khối lượng hỗn hợp muối sunfat thu được sau phản ứng.
Dung` DL BTKL: moxit + mH2SO4 = mmuoi' + mH2O
voi' nH2O = nH2SO4 = 0.5*0.1 = 0.05
--> mmuoi' = 2.81 + 0.05*98 - 0.05*18 = 6.81g
Cach' #: (Fe2O3, MgO, ZnO) ----> (Fe2(SO4)3; MgSO4, ZnSO4)
--> nO = nSO4(2-) = nH2SO4 = 0.05
--> m(Fe, Mg, Zn) = 2.81 - mO = 2.81 - 0.05*16 = 2.01g
mmuoi' = mKL + mSO4(2-) = 2.01 + 0.05*96 = 6.81g
Đúng 0
Bình luận (2)
500 ml = 0,5 l
Ta có nH2SO4 = 0,5 . 0,1 = 0,05 (mol)
Fe2O3 + 3H2SO4 \(\rightarrow\) Fe2(SO4)3 + 3H2O (1)
x \(\rightarrow\) 3x \(\rightarrow\) x \(\rightarrow\) 3x
H2SO4 + MgO \(\rightarrow\) MgSO4 + H2O (2)
y \(\rightarrow\) y \(\rightarrow\) y \(\rightarrow\) y
H2SO4 + ZnO \(\rightarrow\) ZnSO4 + H2O (3)
z \(\rightarrow\) z \(\rightarrow\) z \(\rightarrow\) z
từ các phương trình (1)(2)(3) => nH2 = nH2SO4 = 0,05
Theo định luật bảo toàn khối lượng
=> Mmuối = Mkim loại + Maxít - MH2
= 2,81 + 0,05 . 98 - 0,05 . 2
= 7,61 ( gam )
Đúng 0
Bình luận (1)
m muối = m oxit + 80*n h2so4
= 2.81 + 80*0.05= 6.81g
đơn giản dễ hiểu
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Hòa tan hoàn toàn 21,1 gam hỗn hợp A gồm Zn và ZnO cần dùng 200 ml dung dịch axit axetic. Sau phản ứng thu được 4,48 lít khí H2 (đktc).
a. Tính % khối lượng mỗi chất trong hỗn hợp A.
b. Tính nồng độ mol của axit axetic đã dùng.
$a\big)$
$Zn+2CH_3COOH\to (CH_3COO)_2Zn+H_2$
$ZnO+2CH_3COOH\to (CH_2COO)_2Zn+H_2O$
Theo PT: $n_{Zn}=n_{H_2}=\frac{4,48}{22,4}=0,2(mol)$
$\to \%m_{Zn}=\frac{0,2.65}{21,1}.100\%\approx 61,61\%$
$\to \%m_{ZnO}=100-61,61=38,39\%$
$b\big)$
$n_{ZnO}=\frac{21,1-0,2.65}{81}=0,1(mol)$
Theo PT: $\sum n_{CH_3COOH}=2n_{Zn}+2n_{ZnO}=0,6(mol)$
$\to C_{M_{CH_3COOH}}=\dfrac{0,6}{\frac{200}{1000}}=3M$
Đúng 4
Bình luận (0)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(Zn+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Zn+H_2\)
0,2 0,2 ( mol )
\(m_{Zn}=0,2.65=13g\)
\(\%m_{Zn}=\dfrac{13}{21,1}.100=61,61\%\)
\(\%m_{ZnO}=100\%-61,61\%=38,39\%\)
\(Zn+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Zn+H_2\)
0,2 0,4 ( mol )
\(n_{ZnO}=\dfrac{21,1-13}{81}=0,1mol\)
\(ZnO+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Zn+H_2O\)
0,1 0,2 ( mol )
\(C_{M\left(CH_3COOH\right)}=\dfrac{0,4+0,2}{0,2}=3M\)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 2,81 gam hỗn hợp gồm
Fe
2
O
3
, MgO, ZnO trong 500 ml axit
H
2
SO
4
0,1M (vừa đủ). Sau phản ứng cô cạn dung dịch hỗn hợp muối sunfat khan thu được có khối lượng là A. 6,81 gam B. 4,81 gam C. 3,81 gam D. 5,81 gam
Đọc tiếp
Hòa tan hoàn toàn 2,81 gam hỗn hợp gồm Fe 2 O 3 , MgO, ZnO trong 500 ml axit H 2 SO 4 0,1M (vừa đủ). Sau phản ứng cô cạn dung dịch hỗn hợp muối sunfat khan thu được có khối lượng là
A. 6,81 gam
B. 4,81 gam
C. 3,81 gam
D. 5,81 gam
Bài 1 Hòa tan 10 gam hỗn hợp gồm hai kim loại đồng và kẽm cần dùng hết V ml dung dịch axit HCl 0,2 mol thấy thoát ra 2,24 l khí ( đo ở dktc )a. Tính phần trăm theo khối lượng của mỗi kim loại có trong hỗn hợp đầu.b. Tính V của dd axit HCl cần dùng. Bài 2 Cho 20g hỗn hợp muối Na2CO3 và Na2SO4 tác dụng vừa đủ với dd HCl 20% thu được 2,24 dm^3 khí ở dktca. Tính phần trăm theo khối lượng của các chất có trong hỗn hợp b. Tính khối lượng Hcl đã dùng
Đọc tiếp
Bài 1
Hòa tan 10 gam hỗn hợp gồm hai kim loại đồng và kẽm cần dùng hết V ml dung dịch axit HCl 0,2 mol thấy thoát ra 2,24 l khí ( đo ở dktc )
a. Tính phần trăm theo khối lượng của mỗi kim loại có trong hỗn hợp đầu.
b. Tính V của dd axit HCl cần dùng.
Bài 2 Cho 20g hỗn hợp muối Na2CO3 và Na2SO4 tác dụng vừa đủ với dd HCl 20% thu được 2,24 dm^3 khí ở dktc
a. Tính phần trăm theo khối lượng của các chất có trong hỗn hợp
b. Tính khối lượng Hcl đã dùng