Cho 17,76 g hỗn hợp gồm CaO và Fe2O3 kết hợp với 200 ml HCl 3,3M \
a) Lập PT
b) Tính % m mỗi oxit có trong hỗn hợp
Cho 16 gam hỗn hợp gồm 2 oxit CuO và Fe2O3 hoàn tan vừa đủ trong 500 ml dung dịch HCl 1M. a) Tính khối lượng mỗi oxit trong hỗn hợp. b) Tính thành phần % khối lượng mỗi oxit trong hỗn hợp.
a,\(n_{HCl}=0,5.1=0,5\left(mol\right)\)
PTHH: CuO + 2HCl → CuCl2 + H2O
Mol: x 2x
PTHH: Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Mol: y 6y
Ta có: \(\left\{{}\begin{matrix}80x+160y=16\\2x+6y=0,5\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
PTHH: CuO + 2HCl → CuCl2 + H2O
Mol: 0,1 0,2
PTHH: Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Mol: 0,05 0,3
\(\Rightarrow m_{CuO}=0,1.80=8\left(g\right);m_{Fe_2O_3}=16-8=8\left(g\right)\)
b,\(\%m_{CuO}=\dfrac{8.100\%}{16}=50\%;\%m_{Fe_2O_3}=100-50=50\%\)
200(ml) dung dịch HCL có nồng độ 3,5M hòa tan vừa hết 20(g) hỗn hợp hai oxit CuO và Fe2O3. Tính khối lượng của mỗi oxit trong hỗn hợp ban đầu
Đổi 200ml = 0,2 lít
Ta có: \(n_{HCl}=3,5.0,2=0,7\left(mol\right)\)
Gọi x, y lần lượt là số mol của CuO và Fe2O3
PTHH:
CuO + 2HCl ----> CuCl2 + H2O (1)
Fe2O3 + 6HCl ---> 2FeCl3 + 3H2O (2)
Theo PT(1): \(n_{HCl}=2.n_{CuO}=2x\left(mol\right)\)
Theo PT(2): \(n_{HCl}=6.n_{Fe_2O_3}=6y\left(mol\right)\)
=> 2x + 6y = 0,7 (*)
Theo đề, ta có: 80x + 160y = 20 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}2x+6y=0,7\\80x+160y=20\end{matrix}\right.\)
=> x = 0,05, y = 0,1
=> \(m_{CuO}=80.0,05=4\left(g\right)\)
\(m_{Fe_2O_3}=20-4=16\left(g\right)\)
đổi 200ml = 0.2 l
nhcl = 0.2*3.5 = 0.7 ( mol)
gọi số mol của CuO là x
số mol của Fe2O3 là y
PTHH:
CuO + 2HCl ➜ CuCl2 + H2O
x 2x
Fe2O3 + 6HCl ➜ 2FeCl3 + 3H2O
y 6y
ta có hệ phương trình
\(\left\{{}\begin{matrix}80x+160y=20\\2x+6y=0,7\end{matrix}\right.\)
⇒ x= 0.05
y=0.1
mCuO= 0.05*80=4 (g)
mFe2O3= 0.1*160=16(g)
Phương trình hóa học:
CuO + 2HCl → CuCl2 + H2O (1)
Fe2O3 + 6HCl → 2FeCl3 + 3H2O (2)
Khối lượng của mỗi oxit trong hỗn hợp: x + y = 20
nHCl= 3,5 . 0,2 = 0,7 mol
Gọi khối lượng của CuO trong hỗn hợp là x và Fe2O3 là y (gam).
Từ (1) và (2) ta có:
{x+y=20x40+3y80=0,7{x+y=20x40+3y80=0,7
Giải hệ phương trình ta được x = 4 gam và y = 16 gam.
cho 16g hỗn hợp gồm 2 oxit CuO và Fe2O3 hòa tan vừa đủ trong 500 ml dung dịch HCl 1M
a) tính khối lượng mỗi oxit trong hỗn hợp
b)tình thành phần phần trăm khối lượng mỗi oxit trong hỗn hợp
\(n_{HCl}=0,5.1=0,5\left(mol\right)\)
a)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
x------->2x
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
y--------->6y
Có hệ: \(\left\{{}\begin{matrix}2x+6y=0,5\\80x+160y=16\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
\(m_{CuO}=0,1.80=8\left(g\right)\\ m_{Fe_2O_3}=0,05.160=8\left(g\right)\)
b
\(\%m_{CuO}=\dfrac{0,1.80.100\%}{16}=50\%\\ \%m_{Fe_2O_3}=\dfrac{0,05.160.100\%}{16}=50\%\)
200 ml dung dịch HCl có nồng độ 3,5M hòa tan vừa hết với 200g hỗn hợp hai oxit CuO VÀ Fe2O3.
a) viết các phương trình hóa học.
b) tính khối lượng của mỗi oxit có trong hỗn hợp ban đầu.
a) 2HCl + CuO ----> CuCl2 + H2O
6HCl + Fe2O3 ----> 2FeCl3 + 3H2O
b) nHCl= 3.5 x 0.2 = 0.7
Đặt x, y lần lượt là số mọl của HCl ở pt 1, pt2
2HCl + CuO ----> CuCl2 + H2O
2x-------------x-----------x--------- x
6HCl + Fe2O3-----> 2FeCl3 + 3H2O
6y---------------y----------------2y--... 3y
ta có hệ phương trình hai ẩn x, y
2x+ 6y = 0.7
80x+160y=20
===> x=0.05;y = 0.1
m CuO= 0.05 x 80=4 g
m Fe2O3= 0.1 x 160 =16 g
Hòa tan hoàn toàn 53,4(g) hổn hợp bột ZnO và Fe2O3 cần dùng 200(ml) dung dịch HCL 6,9M
a)tính khối lượng mỗi oxit trong hỗn hợp ban đầu
b) tính thể tích dung dịch H2SO4 0,315M để hòa tan hoàn toàn hỗn hợp oxit trên
a)
$n_{ZnO} = a(mol) ; n_{Fe_2O_3} = b(mol) \Rightarrow 81a + 160b = 53,4(1)$
\(ZnO+2HCl\text{→}ZnCl_2+H_2O\)
a 2a (mol)
\(Fe_2O_3+6HCl\text{→}2FeCl_3+3H_2O\)
b 6b (mol)
$n_{HCl} = 2a + 6b = 0,2.6,9 = 1,38(2)$
Từ (1)(2) suy ra a = 0,6; b = 0,03
$m_{ZnO} = 0,6.81 = 48,6(gam) ; m_{Fe_2O_3} = 0,03.160 = 4,8(gam)$
b)
\(ZnO+H_2SO_4\text{→}ZnSO_4+H_2O\)
0,6 0,6 (mol)
\(Fe_2O_3+3H_2SO_4\text{→}Fe_2\left(SO_4\right)_3+3H_2O\)
0,03 0,09 (mol)
$V_{dd\ H_2SO_4} = \dfrac{0,6 + 0,09}{0,315} = 2,19M$
Cho 200 ml dd H2SO4 2M hòa tan vừa hết với 24g hỗn hợp CUO và Fe2O3.
Tính khối lượng mỗi oxit trong hỗn hợp
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
Ta có: 80nCuO + 160nFe2O3 = 24 (1)
\(n_{H_2SO_4}=0,2.2=0,4\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n_{CuO}+3n_{Fe_2O_3}=0,4\left(2\right)\)
Từ (1) và (2) ⇒ nCuO = nFe2O3 = 0,1 (mol)
⇒ mCuO = 0,1.80 = 8 (g)
mFe2O3 = 0,1.160 = 16 (g)
\(n_{CuO}=a\left(mol\right);n_{Fe_2O_3}=b\left(mol\right)\left(a,b>0\right)\\ CuO+H_2SO_4\rightarrow CuSO_4+H_2O\\ Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\\ \Rightarrow\left\{{}\begin{matrix}80a+160b=24\\a+3b=2.0,2=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\\ \%m_{CuO}=\dfrac{0,1.80}{24}.100\%\approx33,333\%;\%m_{Fe_2O_3}=\dfrac{160.0,1}{24}.100\%\approx66,667\%\)
đổi `200ml=0,2l`
`=>n_(H_2 SO_4)=C_M *V=2*0,2=0,4(mol)`
gọi: \(\left\{{}\begin{matrix}n_{CuO}=a\left(mol\right)\\n_{Fe_2O_3}=b\left(mol\right)\end{matrix}\right.\)
\(PTHH:CuO+H_2SO_4->CuSO_4+H_2O\)
tỉ lệ 1 : 1 : 1 : 1
n(mol) a----------->a---------->a------------>a
\(PTHH:Fe_2O_3+3H_2SO_4->Fe_2\left(SO_4\right)_3+3H_2O\)
tỉ lệ 1 ; 3 : 1 : 3
n(mol) b--------->3b------------>b-------------->3b
Ta có hệ phương trình sau
\(\left\{{}\begin{matrix}80a+160b=24\\a+3b=0,4\end{matrix}\right.\\ < =>\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\\ =>\left\{{}\begin{matrix}n_{CuO}=0,1\left(mol\right)\\n_{Fe_2O_3}=0,1\left(mol\right)\end{matrix}\right.\\ =>\left\{{}\begin{matrix}m_{CuO}=n\cdot M=0,1\cdot80=8\left(g\right)\\m_{Fe_2O_3}=n\cdot M=0,1\cdot160=16\left(g\right)\end{matrix}\right.\)
Hòa tan vừa hết 20 gam hỗn hợp CuO và F e 2 O 3 trong 200 ml dung dịch HCl 3,5M . Khối lượng mỗi oxit trong hỗn hợp là:
A. 4 g và 16 g
B. 10 g và 10 g
C. 8 g và 12 g
D. 14 g và 6 g
Chọn A
gọi x, y lần lượt là số mol của CuO và F e 2 O 3
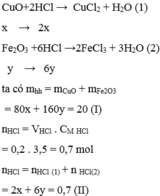
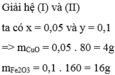
huhu ai có tâm giúp em với, e cần gấp T.T
1. Cho 17,76 gam hỗn hợp CaO và Fe2O3 hòa tan hoàn toàn cần 200ml dung dịch HCl 3,3M. Tính thành phần phần trăm trong các oxit của hỗn hợp
2. hóa tan toàn bộ 12gam hỗn hợp Mg và MgO bằng dung dịch HCl. dung dịch thu được cho tác dụng với một lượng NaOh dư. lọc kết tủa rửa sạch rồi nung ở nhiệt độ cao cho đến khi khối lượng k đổi thu đ 14gam chất rắn. tính % khối lượng hỗn hợp ban đầu đã dùng
3. cho 3,87 gam hỗn hợp kim loại gồm Al và Mg tác dụng vs 500ml dung dịch HCl 1M thu được 4, 368l H2 (đktc) hãy tính %số mol các chất ban đầu trong hỗn hợp
Ai làm hộ e nhanh nhất e lấy cả 3 nick e tick đúng cho ạ
Giả sử dd axit phản ứng hết
--> nH2 = 0.5nH+ = 0.5(0.25*1+0.25*0.5*2)=0.25mol
--> VH2 = 5.6l > 4.368l
--> axit còn dư, KL hết
Gọi nAl = a, nMg = b
--> 27a+24b = 3.87
1.5a + b = 0.195
--> a = 0.09, b= 0.06
nH+ dư = 0.5 - 0.39 = 0.11
nOH- = 0.01V + 0.01*2*V = 0.03V
H+ + OH- --> H2O
0.11 0.11
nAl3+ = nAl = 0.09
Al3+ + 3OH- --> Al(OH)3
0.09 0.27 0.09
Al(OH)3 + OH- --> AlO2(-) + 2H2O
0.09 0.09
--> 0.03V = 0.47
--> V = 15.67l
chịu thôi
Hòa tan vừa hết 28g hỗn hợp MgO và Fe2O3.vào 200 g dung dịch HCl có nồng độ 21,9%. Tính % khối lượng mỗi oxit trong hỗn hợp ban đầu
Giả sử :
\(n_{MgO}=a\left(mol\right),n_{Fe_2O_3}=b\left(mol\right)\)
\(\Rightarrow m_{hh}=40a+160b=28\left(g\right)\left(1\right)\)
\(n_{HCl}=\dfrac{200\cdot21.9\%}{36.5}=1.2\left(mol\right)\)
\(PTHH:\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
Từ PTHH :
\(n_{HCl}=2a+6b=1.2\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.3,b=0.1\)
\(\%m_{MgO}=\dfrac{0.3\cdot40}{28}\cdot100\%=42.85\%\)
\(\%m_{Fe_2O_3}=100-42.85=57.15\%\)