Cho 16g oxide của kim loại A hóa trị 3 tác dụng hết với dung dịch HCl. Sau phản ứng thu được 325g dung dịch muối Chloride 10%
Mọi người giúp em với ạ
cho 18,6g oxide của kim loại R hóa trị I tác dụng vừa đủ với dung dịch HCl thu được dung dịch có chứa 35,1 g muối chloride. Xác định công thức hóa học của oxide trên.
\(n_{R_2O}=\dfrac{18,6}{2M_R+16}\left(mol\right);n_{RCl}=\dfrac{35,1}{M_R+35,5}\left(mol\right)\)
PTHH: R2O + 2HCl ---> 2RCl + H2O
Theo PT: \(2n_{R_2O}=n_{RCl}\)
=> \(\dfrac{2.18,6}{2M_R+16}=\dfrac{35,1}{M_R+35,5}\)
=> MR = 23 (g/mol)
=> R là Natri (Na)
=> Oxide là Na2O
\(R_2O+2HCl\rightarrow2RCl+H_2O\\ n_{Cl}=n_{HCl}=\dfrac{35,1-18,6}{71-16}=0,3\left(mol\right)\\ n_{oxit}=\dfrac{n_{HCl}}{2}=\dfrac{0,3}{2}=0,15\left(mol\right)\\ M_{oxit}=\dfrac{18,6}{0,15}=124\left(\dfrac{g}{mol}\right)=2M_R+M_O\\ \Leftrightarrow2M_R+16=124\\ \Leftrightarrow M_R=54\left(\dfrac{g}{mol}\right)\)
Em xem lại đề
cho 8g 1 oxide kim loại tác dụng hết với dung dịch HCl, sau phản ứng thu được 13,5g muối khan. Tìm công thức oxide
Gọi CTHH của oxide là \(R_2O_y\)
\(n_R=\dfrac{8}{2R+16y}mol\\ n_{RCl_y}=\dfrac{13,5}{R+35,5y}mol\\ R_2O_y+2yHCl\rightarrow2RCl_y+yH_2O\\ \Rightarrow n_R=n_{RCl_y}:2\\ \Leftrightarrow\dfrac{8}{2R+16y}=\dfrac{13,5}{R+35,5y}:2\\ \Leftrightarrow R=32y\)
Với y = 2 thì R =64, Cu(TM)
Vậy CTHH oxide là CuO
cho 5,4g kim loại A chưa biết hóa trị tác dụng với dung dịch H2SO4.Sau phản ứng thu được 342g dung dịch muối 10%
a) Tìm tên kim loại
a) Gọi hóa trị của kim loại A là n(n>0,n∈Z)
\(n_A=\dfrac{5,4}{A}mol\\ n_{A_2\left(SO_4\right)_n}=\dfrac{342.10\%}{100\%.\left(2A+96n\right)}mol\\ 2A+nH_2SO_4\rightarrow A_2\left(SO_4\right)_n+nH_2\\ \Rightarrow n_A:2=n_{A_2\left(SO_4\right)_n}\\ \Leftrightarrow\dfrac{5,4}{A}:2=\dfrac{342.10\%}{100\%\left(2A+96n\right)}\\ \Leftrightarrow A=9n\)
Với n = 3 thì A = 27(TM)
Vậy kim loại A là Nhôm
Cho 7,0 gam hỗn hợp hai muối cacbonat của kim loại hóa trị II tác dụng hết với dung dịch HCl thấy thoát ra V lít khí ở đktc. Cô cạn dung dịch sau phản ứng thu được 9,2 gam muối khan. Giá trị của V là:
A. 1,12 lít
B. 2,24 lít
C. 3,36 lít
D. 4,48 lít
Đáp án D
Đặt công thức của hai muối là RCO3: x mol
RCO3+ 2HCl → RCl2+ CO2+ H2O
x 2x x x mol
Theo định luật bảo toàn khối lượng:
mmuối cacbonat+ mHCl= m muối clorua+ mCO2+ mH2O
→ 7,0 + 2x. 36,5=9,2+ 44x+18x → x= 0,2 mol→ VCO2= 0,2.22,4= 4,48 lít
cho 2,4g kim loại hóa trị II tác dụng với dung dịch HCl lấy dư, sau khi phản ứng kết thức thu được 2,24 lít khí H2 (ở đktc) xác định tên kim loại?
cho 2,7g kim loại hóa trị III tác dụng với dung dịch H2SO4 lấy dư, sau khi phản ứng kết thúc thu được 3,36 lí khia H2 (ở đktc) xác định tenn kim loại?
Bài 1 :
$R + 2HCl \to RCl_2 + H_2$
n R = n H2 = 2,24/22,4 = 0,1(mol)
M R = 2,4/0,1 = 24(Mg) - Magie
Bài 2 :
$2R + 6HCl \to 2RCl_3 + 3H_2$
n H2 = 3,36/22,4 = 0,15(mol)
n R = 2/3 n H2 = 0,1(mol)
M R = 2,7/0,1 = 27(Al) - Nhôm
Cho kim loại X (hóa trị III) tác dụng với dung dịch HCl vừa đủ rồi cô cạn dung dịch sau phản ứng, thu được a gam muối khan. Nếu lấy cùng lượng X như trên cho tác dụng với dd H2SO4 loãng vừa đủ rồi cô cạn dung dịch, thì thu được b gam muối khan. Lập biểu thức tính số mol X theo a, b.
\(n_{XCl_3}=\dfrac{a}{M_X+106,5}\left(mol\right)\)
PTHH: 2X + 6HCl --> 2XCl3 + 3H2
=> \(n_X=\dfrac{a}{M_X+106,5}\left(mol\right)\)
\(n_{X_2\left(SO_4\right)_3}=\dfrac{b}{2.M_X+288}\left(mol\right)\)
PTHH: 2X + 3H2SO4 --> X2(SO4)3 + 3H2
=> \(n_X=\dfrac{b}{M_X+144}\left(mol\right)\)
1a, Cho 4,8g một kim loại hóa trị 2 phản ứng hết với dung dịch HCL dư, thu được 2,688lits H2(đktc). Xác định tên kim loại và khối lượng muối thu được sau phản ứng
1b, Cho 2,4g kim loại Mg tác dụng hết với đ HCL dư được V lít H2 ở đktc. Tính giá tri của V và khối lượng muối thu được sau phản ứng
1a)
nH2 = 2.688/22.4 = 0.12 (mol)
M + 2HCl => MCl2 + H2
0.12..............0.12......0.12
MM = 4.8/0.12 = 40
=> M là : Ca
mCaCl2 = 0.12 * 111 = 13.32 (g)
1b)
nMg = 2.4/24 = 0.1 (mol)
Mg + 2HCl => MgCl2 + H2
0.1....................0.1.........0.1
VH2 = 0.1*22.4 = 2.24 (l)
mMgCl2 = 0.1*95 = 9.5 (g)
1b)
nMg=0,2(mol)
PTHH: Mg + 2 HCl -> MgCl2 + H2
nH2=nMgCl2=nMg=0,2(mol)
=> nHCl=2.0,2=0,4(mol)
=> V=V(H2,đktc)=0,2.22,4=4,48(l)
mMgCl2=95. 0,2=19(g)
: Hòa tan 13g một kim loại hóa trị 2 tác dụng với dung dịch HCL , sau phản ứng thu được 27,2g muối khan , xác định kim loại
Đặt kim loại cần tìm là R
\(n_R=\dfrac{13}{M_R}\left(mol\right);n_{RCl_2}=\dfrac{27,2}{M_R+71}\left(mol\right)\)
PTHH: R + 2HCl ---> RCl2 + H2
Theo PT: \(n_R=n_{RCl_2}\)
\(\Rightarrow\dfrac{13}{M_R}=\dfrac{27,2}{M_R+71}\Leftrightarrow M_R=65\left(g/mol\right)\)
Vậy R là kim loại kẽm
Cho 6,2 gam oxit của kim loại hóa trị I tác dụng với nước dư thu được dung dịch A có tính kiềm. Chia A thành 2 phần bằng nhau:
Phần 1 tác dụng với 95ml dung dịch HCl 1M thấy dung dịch sau phản ứng làm xanh quỳ tím.
Phần 2 tác dụng với 55ml dung dịch HCl 2M thấy dung dịch sau phản ứng làm đỏ quỳ tím.
Công thức oxit kim loại đã dùng là:
A.Li2O.
B. Na2O.
C.K2O.
D.Rb2O.
Gọi n M 2 O = a thì nMOH = 2a, mỗi phần có nMOH = a
Khi nHCl = 0,095 thì dung dịch sau phản ứng làm quỳ tím hóa xanh nên MOH dư => a > 0,095
Khi nHCl = 0,11 thì dung dịch sau phản ứng làm quỳ tím hóa đỏ nên HCl dư => a < 0,11
Có 0,095 < a < 0,11
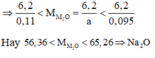
Đáp án B