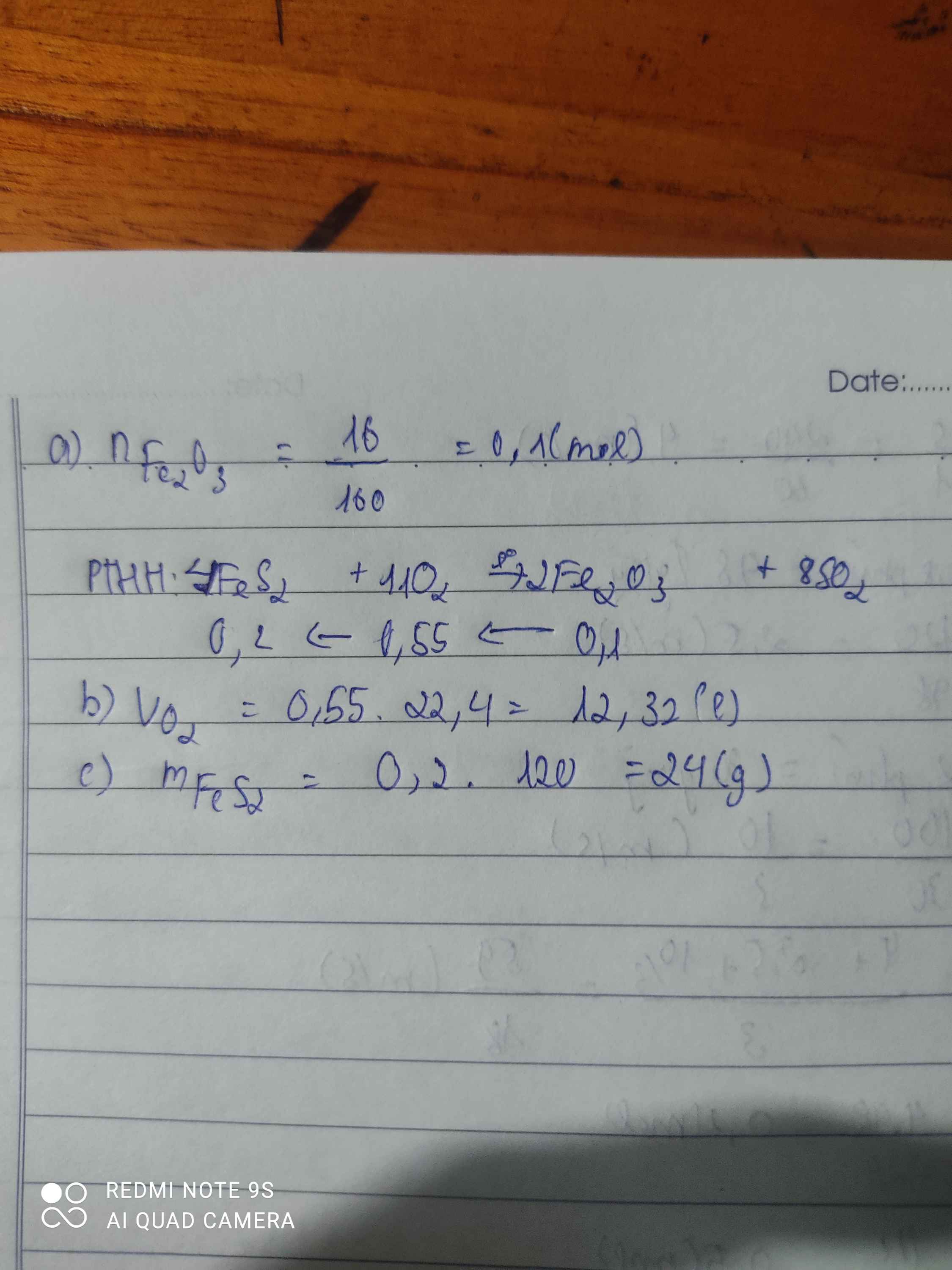Câu 6: Phân loại và gọi tên các oxit sau: Fe\(_2\)O\(_3\), SO\(_3\), N\(_2\)O\(_5\), Na\(_2\)O, P\(_2\)Os, FeO, CO\(_2\),
CuO, Mn\(_2\)0\(_7\), SO\(_2\), HgO, PbO, Ag\(_2\)0.

Những câu hỏi liên quan
Cho các chất sau :NO,Al_2O_3 ,SO_2 ,CuO,Fe_2O_3 ,P_2O_5 ,MgO,PbO,Na_2O,SO_3 ,CaO,FeO,CO_2 .
Viết PT phản ứng với H_2 ,H_2O,dung dịch HCl,Ba(OH)_2
Đọc tiếp
Cho các chất sau :NO,Al\(_2\)O\(_3\) ,SO\(_2\) ,CuO,Fe\(_2\)O\(_3\) ,P\(_2\)O\(_5\) ,MgO,PbO,Na\(_2\)O,SO\(_3\) ,CaO,FeO,CO\(_2\) .
Viết PT phản ứng với H\(_2\) ,H\(_2\)O,dung dịch HCl,Ba(OH)\(_2\)
tác dụng với H2
+) 3H2 + Al2O3 \(\underrightarrow{to}\) 2Al + 3H2O
+) H2 + CuO \(\underrightarrow{to}\) Cu + H2O
+) 3H2 + Fe2O3 \(\underrightarrow{to}\) 2Fe + 3H2O
+) H2 + MgO \(\underrightarrow{to}\) Mg + H2O
+) H2 + FeO \(\underrightarrow{to}\) Fe + H2O
tác dụng với H2O :
+) H2O + SO2 -> H2SO3
+) 3H2O + P2O5 -> 2H3PO4
+) H2O + Na2O -> 2NaOH
+) H2O + SO3 -> H2SO4
+) H2O + CaO -> Ca(OH)2
+) H2O + CO2 -> H2CO3
Tác dụng với HCl
+) Al2O3 + 6HCl -> 2AlCl3 + 3H2O
+) Fe2O3 + 6HCl -> 2FeCl3 + 3H2O
+) MgO + 2HCl -> MgCl2 + H2O
+) PbO + 2HCl -> PbCl2 + H2O
+) Na2O + 2HCl -> 2NaCl + H2O
+)CaO + 2HCl -> CaCl2 + H2O
+) FeO + 2HCl -> FeCl2 + H2O
tác dụng với Ba(OH)2 :
+) Ba(OH)2 + SO2 -> BaSO3 + H2O
+) 3Ba(OH)2 + P2O5 -> Ba3(PO4)2 + 3H2O
+) Ba(OH)2 + SO3 -> BaSO4 + H2O
+) Ba(OH)2 + CO2 -> BaCO3 + H2O
Đúng 0
Bình luận (2)
- H2
CuO + H2 -to-> Cu + H2O
Fe2O3 + 3H2 -to-> 2Fe + 3H2O
PbO + H2 -to-> Pb + H2O
FeO + H2 -to-> Fe + H2O
- H2O
SO2 + H2O --> H2SO3
P2O5 + 3H2O --> 2H3PO4
Na2O + H2O --> 2NaOH
SO3 + H2O --> H2SO4
CaO + H2O --> Ca(OH)2
CO2 + H2O <--> H2CO3
- Ba(OH)2 :
Ba(OH)2 + SO2 --> BaSO3 + H2O
Ba(OH)2 + P2O5 --> Ba3(PO4)2 +H2O
Ba(OH)2 + SO3 --> BaSO4 + H2O
Ba(OH)2 + CO2 --> BaCO3 + H2O
PTHH tự cân bằng nhé
Đúng 0
Bình luận (1)
Đóc tên và phân loại các loại oxit sau :
1. Na\(_2\)O 2. Fe\(_2\)O\(_3\) 3. SO\(_3\) 4. Cu\(_2\)O
5. PbO 6. NO 7. Ag\(_2\)O 8. N\(_2\)O\(_3\)
1) Natri oxit (oxit kim kim)
2) Sắt (III) oxit (oxit kim loại)
3) Lưu huỳnh trioxit (oxit phi kim)
4) Đồng (I) oxit ( oxit kim loại)
5) Chì (II) oxit (oxit kim loại)
6) Nito monoxit (oxit phi loại)
7) Bạc oxit (oxit kim loại)
8) Đinitơ trioxit (oxit phi loại)
Đúng 0
Bình luận (0)
Câu 1 : Phản ứng nào sau đây là phản ứng thế :
A. 2KClO_3rightarrow 2KCl + O_2 B. Fe_2O_3 + 6HCl rightarrow 2FeCl_3 + 3H_2O
C. SO_3+ H_2O rightarrowH_2SO_4 D. Fe_3O_4 + 4H_2rightarrow 3Fe + 4H_2O
Câu 2 : Kim loại nào sau đây phản ứng được với axit H_2SO_4 loãng sinh khí hidro :
A. Đồng B. Thủy ngân C. Magie D. Bạc
Câu 3 : Hỗn hợp hidro và oxi nổ mạnh nhất khi tỉ lệ thể tích khí oxi và hidro bằng :
A. 1...
Đọc tiếp
Câu 1 : Phản ứng nào sau đây là phản ứng thế :
A. 2KClO\(_3\)\(\rightarrow\) 2KCl + O\(_2\) B. Fe\(_2\)O\(_3\) + 6HCl \(\rightarrow\) 2FeCl\(_3\) + 3H\(_2\)O
C. SO\(_3\)+ H\(_2\)O \(\rightarrow\)H\(_2\)SO\(_4\) D. Fe\(_3\)O\(_4\) + 4H\(_2\)\(\rightarrow\) 3Fe + 4H\(_2\)O
Câu 2 : Kim loại nào sau đây phản ứng được với axit H\(_2\)SO\(_4\) loãng sinh khí hidro :
A. Đồng B. Thủy ngân C. Magie D. Bạc
Câu 3 : Hỗn hợp hidro và oxi nổ mạnh nhất khi tỉ lệ thể tích khí oxi và hidro bằng :
A. 1 : 2 B. 2 : 1 C. 1 : 1 D. 3 : 1
Câu 4 : Dãy oxit bazo nào dưới đây tác dụng được với nước tạo thành dung dịch bazo :
A. Na\(_2\)O , K\(_2\)O , CaO B. Na\(_2\)O , CuO , FeO
C. SO\(_2\) , SO\(_3\), NO D. BaO , MgO , Al\(_2\)O\(_3\)
Câu 5 : Dãy oxit kim loại nào sau đây tác dụng được với hidro :
A. CaO , ZnO , FeO B. Na\(_2\)O , Al\(_2\)O\(_3\) , ZnO
C. PbO , ZnO , Fe\(_2\)O\(_3\) D. CuO , PbO , MgO
Câu 1 : Phản ứng nào sau đây là phản ứng thế :
A. 2KClO3→→ 2KCl + O22
B. Fe2O3 + 6HCl →→ 2FeCl3 + 3H2O
C. SO3+ H22O →→H2SO4
D. Fe3O4 + 4H22→→ 3Fe + 4H22O
Câu 2 : Kim loại nào sau đây phản ứng được với axit H22SO4 loãng sinh khí hidro :
A. Đồng B. Thủy ngân C. Magie D. Bạc
Câu 3 : Hỗn hợp hidro và oxi nổ mạnh nhất khi tỉ lệ thể tích khí oxi và hidro bằng :
A. 1 : 2 B. 2 : 1 C. 1 : 1 D. 3 : 1
Câu 4 : Dãy oxit bazo nào dưới đây tác dụng được với nước tạo thành dung dịch bazo :
A. Na2O , K2O , CaO B. Na22O , CuO , FeO
C. SO22 , SO33, NO D. BaO , MgO , Al22O33
Câu 5 : Dãy oxit kim loại nào sau đây tác dụng được với hidro :
A. CaO , ZnO , FeO B. Na22O , Al22O33 , ZnO
C. PbO , ZnO , Fe22O33 D. CuO , PbO , MgO
Câu 1 : Phản ứng nào sau đây là phản ứng thế :
A. 2KClO3→ 2KCl + 3O2
B. Fe2O3+ 6HCl →→ 2FeCl3 + 3H2O
C. SO3+ H2O →→H2SO4
D. Fe3O4 + 4H2→→ 3Fe + 4H2O
Phản ứng B,D là pư thế
Câu 2 : Kim loại nào sau đây phản ứng được với axit H22SO44 loãng sinh khí hidro :
A. Đồng B. Thủy ngân C. Magie D. Bạc
Câu 3 : Hỗn hợp hidro và oxi nổ mạnh nhất khi tỉ lệ thể tích khí oxi và hidro bằng :
A. 1 : 2 B. 2 : 1 C. 1 : 1 D. 3 : 1
Câu 4 : Dãy oxit bazo nào dưới đây tác dụng được với nước tạo thành dung dịch bazo :
A. Na22O , K22O , CaO B. Na22O , CuO , FeO
C. SO22 , SO33, NO D. BaO , MgO , Al22O33
Câu 5 : Dãy oxit kim loại nào sau đây tác dụng được với hidro :
A. CaO , ZnO , FeO B. Na22O , Al22O33 , ZnO
C. PbO , ZnO , Fe22O33 D. CuO , PbO , MgO
Pthh nào sau đây viết đúng:1.A.4Al+O_2➜2Al_2O_3B.Al+O_2➜AlO_2C.2Al+3O_2➜2Al_2O_3_{ }D.4Al+3O_2➜2Al_2O_32.A.2Zn+O_2➜2ZnOB.Zn+O➜ZnOC.Zn+O_2➜ZnOD.Zn+O_2➜2ZnO3.A.2P+5O_2➜2P^2O_5B.2P+O_2➜P_2O_5C.2P+5O➜P_2O_5D.4P+5O_2➜2P^2O_5Ở điều kiện tiêu chuẩn, thể tích mol của chất khí :1.A. 1,12 lítB. 2,24 lítC. 11,2 lítD. 22,4 lít2.A. 44,8 lítB. 22,4 lítC. 32 lítD. 2,24 lítSố ntử Na có trong 1,5 moi ntử Na là:A. 1,5 NB. 6,023.10^{23}C. 1 ND. 12,046.10^{23}
Đọc tiếp
Pthh nào sau đây viết đúng:
1.
A.4Al+O\(_2\)➜2Al\(_2\)O\(_3\)
B.Al+O\(_2\)➜AlO\(_2\)
C.2Al+3O\(_2\)➜2Al\(_2\)O\(_3\)\(_{ }\)
D.4Al+3O\(_2\)➜2Al\(_2\)O\(_3\)
2.
A.2Zn+O\(_2\)➜2ZnO
B.Zn+O➜ZnO
C.Zn+O\(_2\)➜ZnO
D.Zn+O\(_2\)➜2ZnO
3.
A.2P+5O\(_2\)➜2P\(^2\)O\(_5\)
B.2P+O\(_2\)➜P\(_2\)O\(_5\)
C.2P+5O➜P\(_2\)O\(_5\)
D.4P+5O\(_2\)➜2P\(^2\)O\(_5\)
Ở điều kiện tiêu chuẩn, thể tích mol của chất khí = :
1.
A. 1,12 lít
B. 2,24 lít
C. 11,2 lít
D. 22,4 lít
2.
A. 44,8 lít
B. 22,4 lít
C. 32 lít
D. 2,24 lít
Số ntử Na có trong 1,5 moi ntử Na là:
A. 1,5 N
B. 6,023.10\(^{23}\)
C. 1 N
D. 12,046.10\(^{23}\)
tất cả phương trình hóa học đều sai vì thiếu điều kiện là nhiệt độ
Đúng 1
Bình luận (5)
Xem thêm câu trả lời
Bài 1 : Viết CTHH của các oxit tạo bởi các nguyên tố : K, Al, Fe, Cu, Mg, Na, Zn, C, S, P với nguyên tố Oxi. Tính phân tử khối và gọi tên các chất đó.
Bài 2 : Cho các hợp chất oxit sau : CO_2 , SO_2 , P_2O_5 , Al_2O_3 , Fe_3O_4 , H_2O, CuO, K_2O. Viết PTHH điều chế các oxit trên.
Bài 3 : Có một số CTHH được viết như sau : KO, AlO, FeO, CaO_2, Zn_2O, MgO, N_2O, PO, S_2O, CO_3. Hãy chỉ ra các CTHH viết sai và sửa lại cho đúng.
Đọc tiếp
Bài 1 : Viết CTHH của các oxit tạo bởi các nguyên tố : K, Al, Fe, Cu, Mg, Na, Zn, C, S, P với nguyên tố Oxi. Tính phân tử khối và gọi tên các chất đó.
Bài 2 : Cho các hợp chất oxit sau : CO\(_2\) , SO\(_2\) , P\(_2\)O\(_5\) , Al\(_2\)O\(_3\) , Fe\(_3\)O\(_4\) , H\(_2\)O, CuO, K\(_2\)O. Viết PTHH điều chế các oxit trên.
Bài 3 : Có một số CTHH được viết như sau : KO, AlO, FeO, CaO\(_2\), Zn\(_2\)O, MgO, N\(_2\)O, PO, S\(_2\)O, CO\(_3\). Hãy chỉ ra các CTHH viết sai và sửa lại cho đúng.
Bài 1: CTHH:
Các hợp chất: K2O, Al2O3, FeO, Fe2O3, Fe3O4, CuO, Cu2O, MgO, Na2O, ZnO, CO, CO2, SO2, SO3, P2O3 , P2O5
\(PTK_{K_2O}=2.39+16=94\left(đ.v.C\right)\)
\(PTK_{Al_2O_3}=2.27+3.16=102\left(đ.v.C\right)\)
\(PTK_{FeO}=56+16=72\left(đ.v.C\right)\\ PTK_{Fe_2O_3}=2.56+3.16=160\left(đ.v.C\right)\\ PTK_{Fe_3O_4}=3.56+4.16=232\left(đ.v.C\right)\)
\(PTK_{CuO}=64+16=80\left(đ.v.C\right)\\ PTK_{Cu_2O}=2.64+16=144\left(đ.v.C\right)\\ PTK_{MgO}=24+16=40\left(đ.v.C\right)\\ PTK_{Na_2O}=2.23+16=62\left(đ.v.C\right)\\ PTK_{ZnO}=65+16=81\left(đ.v.C\right)\\ PTK_{CO}=12+16=28\left(đ.v.C\right)\\ PTK_{CO_2}=12+2.16=44\left(đ.v.C\right)\\ PTK_{SO_2}=32+2.16=64\left(đ.v.C\right)\\ PTK_{SO_3}=32+3.16=80\left(đ.v.C\right)\\ \)
\(PTK_{P_2O_3}=2.31+3.16=110\left(đ.v.C\right)\\ PTK_{P_2O_5}=2.31+5.16=142\left(đ.v.C\right)\)
Đúng 0
Bình luận (0)
Bài 2:
PTHH điều chế các oxit trên:
(1) CO2
PTHH: C + O2 -to-> CO2
hoặc Fe2O3 + 3 CO -to-> 2 Fe + 3 CO2
(2) SO2
PTHH: S + O2 -to-> SO2
hoặc Cu +2 H2SO4(đ) -to-> CuSO4 + 2 H2O + SO2
(3) P2O5
PTHH: 4 P + 5 O2 -to-> 2 P2O5
(4) Al2O3
PTHH: 4Al + 3 O2 -to-> 2 Al2O3
(5) Fe3O4
PTHH: 3 Fe +2 O2 -to-> Fe3O4
(6) H2O
PTHH: 2 H2 + O2 -to-> 2 H2O
(7) CuO
PTHH: 2 Cu + O2 -to-> 2 CuO
(8) K2O
PTHH: 4 K + O2 -to-> 2 K2O
Đúng 0
Bình luận (0)
Bài 3:
| CTHH viết sai | CTHH sửa lại đúng |
| KO | K2O |
| AlO | Al2O3 |
| CaO2 | CaO |
| Zn2O | ZnO |
| PO | P2O3 hoặc P2O5 |
| CO3 | CO hoặc CO2 |
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Lập các phương trình hóa học sau:
1. Mg + O_2 --- MgO
2. P_2O_5 + H_2O --- H_3PO_4
3. Fe + O2 ---- Fe3O4
4. A1 + O_2 --- Al_2O_3
5. H_2O --- H_2 + O_2
6. Cu + O_2 --- CuO
7. Fe + HC1 --- FeC1_2+H_2
8. Zn + C1_2 --- ZnC1_2
9. CaO + HNO_3 --- Ca(NO_3)_2 + H_2O
10. BaC1_2 + Na_2SO_4 + NaC1
11. A1_2O_3 + H_2SO_4--- A1_2(SO_4)_3 + H_2O
Đọc tiếp
Lập các phương trình hóa học sau:
1. Mg + O\(_2\) ---> MgO
2. P\(_2\)O\(_5\) + H\(_2\)O ---> H\(_3\)PO\(_4\)
3. Fe + O2 ----> Fe3O4
4. A1 + O\(_2\) ---> Al\(_2\)O\(_3\)
5. H\(_2\)O ---> H\(_2\) + O\(_2\)
6. Cu + O\(_2\) ---> CuO
7. Fe + HC1 ---> FeC1\(_2\)+H\(_2\)
8. Zn + C1\(_2\) ---> ZnC1\(_2\)
9. CaO + HNO\(_3\) ---> Ca(NO\(_3\))\(_2\) + H\(_2\)O
10. BaC1\(_2\) + Na\(_2\)SO\(_4\) + NaC1
11. A1\(_2\)O\(_3\) + H\(_2\)SO\(_4\)---> A1\(_2\)(SO\(_4\))\(_3\) + H\(_2\)O
Viết PTPƯ thực hiện dãy chuyển hóa sau. Phân loại mỗi PƯHH đóa/ KMnO_4 - O_2 - Fe_3O_4 - Fe - FeSO_4b/ Ba - BaO - Ba(OH)_2c/ S - SO_2 - SO_3 - H2SO_4
Đọc tiếp
Viết PTPƯ thực hiện dãy chuyển hóa sau. Phân loại mỗi PƯHH đó
a/ KMnO\(_4\) -> O\(_2\) -> Fe\(_3\)O\(_4\) -> Fe -> FeSO\(_4\)
b/ Ba -> BaO -> Ba(OH)\(_2\)
c/ S -> SO\(_2\) -> SO\(_3\) -> H2SO\(_4\)
TK :
https://sachgiaibaitap.com/sach_giai/giai-sach-bai-tap-hoa-lop-8-bai-38-luyen-tap-chuong-5/#gsc.tab=0
Đúng 1
Bình luận (4)
a) KMnO4 (to) → K2MnO4 + MnO2 + O2 (phản ứng phân huỷ)
Fe + O2 (to) → Fe3O4 (phản ứng hoá hợp)
Fe3O4 + H2 (to) → Fe + H2O (phản ứng thế)
Fe + H2SO4 → FeSO4 + H2 (phản ứng thế)
b) Ba + O2 (to) → BaO (phản ứng hoá hợp)
BaO + H2O → Ba(OH)2 (phản ứng hoá hợp)
c) S + O2 (to) → SO2 (phản ứng hoá hợp)
SO2 + O2 (to) → SO3 (phản ứng hoá hợp)
SO3 + H2O → H2SO4 (phản ứng hoá hợp)
(các phương trình trên chưa cân bằng)
Đúng 3
Bình luận (0)
Cho FeS_2 tác dụng với O_2 thì thu được Fe_2O_3 và SO_2 sau p.ưa, Viết PTHH của p.ư trên?b, Tìm thể tích oxi ở (đktc) cần sử dụng biết sau p.ư thu được 16g Fe_2O_3?c, Xác định khối lượng FeS_2 đã sử dụng
Đọc tiếp
Cho FeS\(_2\) tác dụng với O\(_2\) thì thu được Fe\(_2\)O\(_3\) và SO\(_2\) sau p.ư
a, Viết PTHH của p.ư trên?
b, Tìm thể tích oxi ở (đktc) cần sử dụng biết sau p.ư thu được 16g Fe\(_2\)O\(_3\)?
c, Xác định khối lượng FeS\(_2\) đã sử dụng
4FeS+7O2-to>2Fe2O3+4SO2
0,2----0,35------0,1 mol
n Fe2O3=\(\dfrac{16}{160}\)=0,1 mol
=>VO2=0,35.22,4=7,84l
=>m FeS2=0,2.120=24g
Đúng 1
Bình luận (1)
1.a) Na + ... underrightarrow{t^0} Na_2Ob) Zn + ... rightarrow ZnCl_2 + H_2c) Cao + ... rightarrow Ca(OH)_2d) SO_3 + ... rightarrow H_2SO_42.a) Ba + ... underrightarrow{t^0} BaOb) CuO + ... underrightarrow{t^0} Cu + H20c) K + ... rightarrow KOH + H_2d) CO_2 + ... rightarrow H_2CO_3
Đọc tiếp
1.
a) Na + ... \(\underrightarrow{t^0}\) Na\(_2\)O
b) Zn + ... \(\rightarrow\) ZnCl\(_2\) + H\(_2\)
c) Cao + ... \(\rightarrow\) Ca(OH)\(_2\)
d) SO\(_3\) + ... \(\rightarrow\) H\(_2\)SO\(_4\)
2.
a) Ba + ... \(\underrightarrow{t^0}\) BaO
b) CuO + ... \(\underrightarrow{t^0}\) Cu + H20
c) K + ... \(\rightarrow\) KOH + H\(_2\)
d) CO\(_2\) + ... \(\rightarrow\) H\(_2\)CO\(_3\)
\(1)\\ a) 4Na + O_2 \xrightarrow{t^o} 2Na_2O\\ b) Zn + 2HCl \to ZnCl_2 + H_2\\ c) CaO + H_2O \to Ca(OH)_2\\ d) SO_3 + H_2O \to H_2SO_4\\ 2)\\ a) 2Ba + O_2 \xrightarrow{t^o} 2BaO\\ b) CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ c) K + H_2O \to KOH + \dfrac{1}{2}H_2\\ d) CO_2 + H_2O \to H_2CO_3\)
Đúng 2
Bình luận (0)