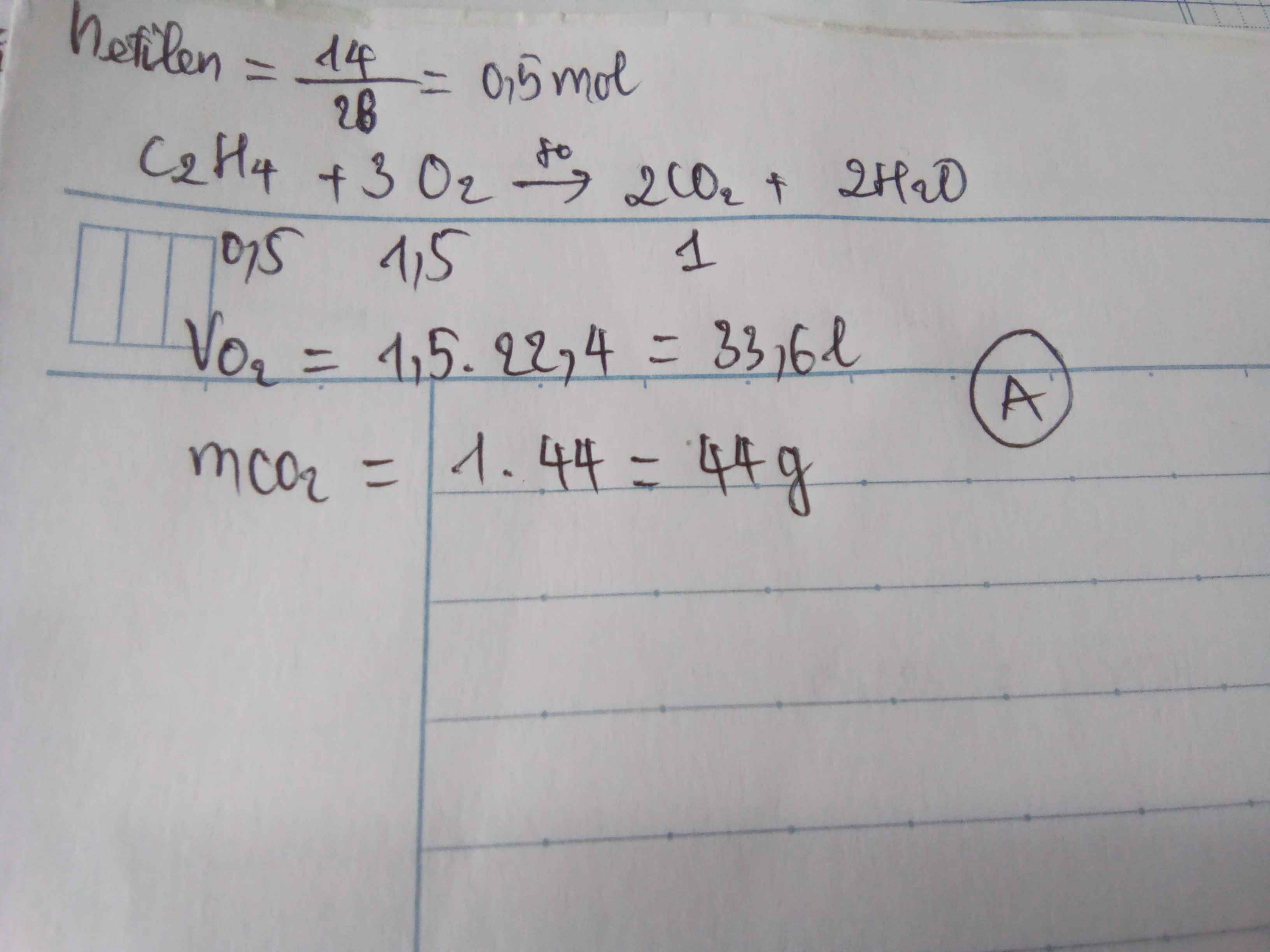Câu 19: Đốt cháy hoàn toàn khí etilen, thu được 5,6 lít khí CO2. Thể tích khí etilen và oxi cần dùng là (Các khí đo ở đktc) A. 5,6 lít; 16,8 lít. B. 2,8 lít; 8,4 lít. C. 28 lít; 84 lít. D. 2,8 lít; 5,6 lít.

Những câu hỏi liên quan
đốt cháy hoàn toàn 5,6 lít khí etilen(đktc)thu được khí co2 và nước. a)Hãy viết các phương trình hóa học xảy ra? b)Tính thể tích không khí cần dùng cho phản ứng cháy biết oxi chiếm 20% c)Tính khối lượng khí co2 thu được
Đọc tiếp
đốt cháy hoàn toàn 5,6 lít khí etilen(đktc)thu được khí co2 và nước. a)Hãy viết các phương trình hóa học xảy ra? b)Tính thể tích không khí cần dùng cho phản ứng cháy biết oxi chiếm 20% c)Tính khối lượng khí co2 thu được
\(n_{C_2H_4}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(C_2H_4+3O_2\underrightarrow{^{t^0}}2CO_2+2H_2O\)
\(0.25.....0.75.......0.5\)
\(V_{kk}=5V_{O_2}=5\cdot0.75\cdot22.4=84\left(l\right)\)
\(m_{CO_2}=0.5\cdot44=22\left(g\right)\)
Đúng 1
Bình luận (0)
Câu 17: Đốt cháy hoàn toàn 14 gam khí etilen. Thể tích khí oxi cần dùng ở đktc và khối lượng khí CO2 sinh ra là A. 33,6 lít; 44 gam. B. 22,4 lít; 33 gam. C. 11,2 lít; 22 gam. D. 5,6 lít; 11 gam.
PTHH: C2H4 (0,5 mol) + 3O2 (1,5 mol) \(\underrightarrow{t^o}\) 2CO2 (1 mol) + 2H2O.
Thể tích khí oxi cần dùng ở đktc: Vkhí oxi=1,5.22,4=33,6 (lít).
Khối lượng khí CO2 sinh ra là: mkhí cacbonic=1.44=44 (g).
Chọn A.
Đúng 1
Bình luận (0)
Câu 17: Đốt cháy hoàn toàn 14 gam khí etilen. Thể tích khí oxi cần dùng ở đktc và khối lượng khí CO2 sinh ra là A. 33,6 lít; 44 gam. B. 22,4 lít; 33 gam. C. 11,2 lít; 22 gam. D. 5,6 lít; 11 gam.
\(n_{C_2H_4}=\dfrac{14}{28}=0,5mol\)
\(C_2H_4+5O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\)
0,5 2,5 1 ( mol )
\(V_{O_2}=2,5.22,4=56l\)
\(m_{CO_2}=1.44=44g\)
( ko có câu đúng :< )
Đúng 1
Bình luận (0)
Câu 29:
Đốt cháy hoàn toàn 14 gam khí etilen. Thể tích khí oxi cần dùng ở đktc và khối lượng khí CO2 sinh ra là
A. 33,6 lít; 44 gam.
B. 22,4 lít; 33 gam.
C. 11,2 lít; 22 gam.
D. 5,6 lít; 11 gam
Để đốt cháy 5,6 lít khí etilen cần phải dùng:
a) Bao nhiêu lít oxi?
b) Bao nhiêu lít không khí chứa 1/5 thể tích oxi? Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
Hỗn hợp A gồm CH4 và C2H4. Đốt cháy hoàn toàn 3,36 lít hỗn hợp A (đktc) thì thu được 8,8g khí cacbonic. Hãy tính thành phần % thể tích của mỗi khí trong hỗn hợp.
Câu 1:
\(a,PTHH:C_2H_4+5O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(n_{C_2H_4}=\dfrac{V_{\left(đktc\right)}}{22,4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(Theo.PTHH:n_{O_2}=5.n_{C_2H_4}=5.0,25=1,25\left(mol\right)\\ V_{O_2\left(đktc\right)}=n.22,4=1,25.22,4=28\left(l\right)\)
\(b,\Rightarrow V_{kk\left(đktc\right)}=5.V_{O_2\left(đktc\right)}=5.28=140\left(l\right)\)
Đúng 0
Bình luận (1)
B1:
\(C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\)
Vì số mol tỉ lệ thuận với thể tích, đồng thời nhìn PTHH, ta sẽ được:
\(a,V_{O_2\left(đktc\right)}=3.V_{C_2H_4\left(đktc\right)}=3.5,6=16,8\left(l\right)\)
\(b,V_{kk}=5.V_{O_2\left(đktc\right)}=16,8.5=84\left(l\right)\)
B2:
Đặt số mol metan, etylen lần lượt là a,b (mol) (a,b>0)
\(n_{hh}=n_{CH_4}+n_{C_2H_4}=a+b=\dfrac{3,36}{22,4}=0,15\left(1\right)\)
PTHH: CH4 +2 O2 -to-> CO2 +2 H2O
C2H4 +3 O2 -to-> 2CO2 + 2H2O
\(n_{CO_2\left(tổng\right)}=a+2b=\dfrac{8,8}{44}=0,2\left(mol\right)\left(2\right)\)
(1), (2) =>a=0,1; b=0,05
Số mol tỉ lệ tương ứng với thể tích. Nên:
\(\%V_{CH_4}=\%n_{CH_4}=\dfrac{0,1}{0,15}.100\approx66,667\%\\ \Rightarrow\%V_{C_2H_4}\approx33,333\%\)
Đúng 4
Bình luận (2)
Câu 29:
Đốt cháy hoàn toàn 14 gam khí etilen. Thể tích khí oxi cần dùng ở đktc và khối lượng khí CO2 sinh ra là
A. 33,6 lít; 44 gam.
B. 22,4 lít; 33 gam.
C. 11,2 lít; 22 gam.
D. 5,6 lít; 11 gam.
PTHH : \(C_2H_4\rightarrow2H_2O+2CO_2\)
\(n_{C_2H_4}=\frac{14}{28}=0,5\left(mol\right)\)
Theo phương trình :
\(n_{O_2}=3n_{C_2H_4}=3.0,5=1,5\left(mol\right)\)
\(\Rightarrow V_{O_2}=1,5.22,4=33,6\left(l\right)\)
\(n_{CO_2}=2n_{C_2H_4}=2.0,5=1\left(mol\right)\)
\(\Rightarrow m_{CO_2}=1.44=44\left(gam\right)\)
PTHH: C2H4 (0,5 mol) + 3O2 (1,5 mol) to→ 2CO2 (1 mol) + 2H2O.
Thể tích khí oxi cần dùng ở đktc: Vkhí oxi=1,5x22,4=33,6 (lít).
Khối lượng khí CO2 sinh ra là: mkhí cacbonic=1x44=44 (gam).
Chọn A.
BT2: Đốt cháy hoàn toàn 5,6 lít hh 2 khí CO và CH4 cần dùng 4,48 lít khí oxi. Tính % theo thể tích mỗi khí trong hh. Các thể tích khí đo ở đktc.
Gọi số mol CO, CH4 là a, b (mol)
=> \(a+b=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: 2CO + O2 --to--> 2CO2
a--->0,5a
CH4 + 2O2 --to--> CO2 + 2H2O
b--->2b
=> 0,5a + 2b = 0,2
=> a = 0,2 (mol); b = 0,05 (mol)
=> \(\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,2}{0,25}.100\%=80\%\\\%V_{CH_4}=\dfrac{0,05}{0,25}.100\%=20\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
\(n_{hh}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ 2CO+O_2\rightarrow\left(t^o\right)2CO_2\\ CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\\ Đặt:n_{CO}=a\left(mol\right);n_{CH_4}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}a+b=0,25\\0,5a+2b=0,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,05\end{matrix}\right.\\ \Rightarrow\%V_{\dfrac{CO}{hh}}=\%n_{\dfrac{CO}{hh}}=\dfrac{a}{a+b}.100\%=\dfrac{0,2}{0,25}.100=80\%;\%V_{CH_4}=100\%-80\%=20\%\)
Đúng 1
Bình luận (0)
Câu 1Trong nhóm hidrocacbon sau, nhóm hidrocacbon nào có phản ứng đặc trưng là phản ứng cộng?AC2H4, CH4 .BC2H4, C2H2 .CCH4, C2H2 .DC2H2, C2H6 .Câu 2Đốt cháy hoàn toàn 5,6 lít khí etilen ở đktc. Thể tích khí oxi và thể tích không khí cần dùng ở đktc là ( biết rằng khí oxi chiếm 20% thể tích không khí)A5,6 lít; 28 lít.B16,8 lít; 84 lít.C16,8 lít; 336 lít.D5,6 lít; 112 lít.Câu 3Chất tham gia phản ứng thế với Cl2 trong diều kiện ánh sang có CTCT là:ACH2CH2BCHCHCCH2CCH2DCH3–CH2–CH3Câu 4Dẫn khí etilen...
Đọc tiếp
Câu 1
Trong nhóm hidrocacbon sau, nhóm hidrocacbon nào có phản ứng đặc trưng là phản ứng cộng?
A
C2H4, CH4 .
B
C2H4, C2H2 .
C
CH4, C2H2 .
D
C2H2, C2H6 .
Câu 2
Đốt cháy hoàn toàn 5,6 lít khí etilen ở đktc. Thể tích khí oxi và thể tích không khí cần dùng ở đktc là ( biết rằng khí oxi chiếm 20% thể tích không khí)
A
5,6 lít; 28 lít.
B
16,8 lít; 84 lít.
C
16,8 lít; 336 lít.
D
5,6 lít; 112 lít.
Câu 3
Chất tham gia phản ứng thế với Cl2 trong diều kiện ánh sang có CTCT là:
A
CH2=CH2
B
CHCH
C
CH2=C=CH2
D
CH3–CH2–CH3
Câu 4
Dẫn khí etilen qua dung dịch Brom thấy dung dịch Brom mất màu. Phương trình hóa học được viết là:
A
CH2=CH2 + Br2 ® CH3–CHBr2
B
CH2=CH2 + Br2 ® CH2Br–CH2Br
C
CH2=CH2 + Br2 ® CH2=CHBr + HBr
D
CH2=CH2 + Br2 ® CH2–Br–Br–CH2
Câu 5
Tính chất hóa học chung của metan, etilen, axetilen là
A
phản ứng thế.
B
phản ứng cộng.
C
phản ứng cháy.
D
phản ứng trùng hợp.
Câu 6
Các trái cây, trong quá trình chín sẽ thoát ra một lượng nhỏ chất khí là :
A
metan.
B
etan.
C
etilen.
D
axetilen.
Câu 7
Khối lượng khí etilen cần dùng để phản ứng hết 8 gam brom trong dung dịch là:
A
0,7 gam.
B
1,4 gam.
C
2,8 gam.
D
14 gam.
Câu 8
Axetilen thường dùng làm nhiên liệu trong hàn cắt kim loại và trong công nghiệp vì
A
khi cháy tỏa nhiệt nhiều.
B
khi cháy không gây ô nhiễm môi trường.
C
giá thành thấp.
D
là nhiên liệu có sẵn trong tự nhiên
Câu 9
Cần tối đa bao nhiêu ml dung dịch brom 0,1 M để tác dụng tối đa với 0,224 lít axetilen ỏ điều kiện tiêu chuẩn?
A
100 .
B
5000 .
C
200.
D
2 .
Câu 10
Để đốt cháy 4,48 lít khí etilen cần phải dùng bao nhiêu lít không khí chứa 20% thể tích oxi ?Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
A
13,44.
B
6,72 .
C
67,2 .
D
22,4 .
Câu 1
Trong nhóm hidrocacbon sau, nhóm hidrocacbon nào có phản ứng đặc trưng là phản ứng cộng?
A
C2H4, CH4 .
B
C2H4, C2H2 .
C
CH4, C2H2 .
D
C2H2, C2H6 .
Câu 2
Đốt cháy hoàn toàn 5,6 lít khí etilen ở đktc. Thể tích khí oxi và thể tích không khí cần dùng ở đktc là ( biết rằng khí oxi chiếm 20% thể tích không khí)
A
5,6 lít; 28 lít.
B
16,8 lít; 84 lít.
C
16,8 lít; 336 lít.
D
5,6 lít; 112 lít.
Câu 3
Chất tham gia phản ứng thế với Cl2 trong diều kiện ánh sang có CTCT là:
A
CH2=CH2
B
CHCH
C
CH2=C=CH2
D
CH3–CH2–CH3
Câu 4
Dẫn khí etilen qua dung dịch Brom thấy dung dịch Brom mất màu. Phương trình hóa học được viết là:
A
CH2=CH2 + Br2 ® CH3–CHBr2
B
CH2=CH2 + Br2 ® CH2Br–CH2Br
C
CH2=CH2 + Br2 ® CH2=CHBr + HBr
D
CH2=CH2 + Br2 ® CH2–Br–Br–CH2
Câu 5
Tính chất hóa học chung của metan, etilen, axetilen là
A
phản ứng thế.
B
phản ứng cộng.
C
phản ứng cháy.
D
phản ứng trùng hợp.
Câu 6
Các trái cây, trong quá trình chín sẽ thoát ra một lượng nhỏ chất khí là :
A
metan.
B
etan.
C
etilen.
D
axetilen.
Câu 7
Khối lượng khí etilen cần dùng để phản ứng hết 8 gam brom trong dung dịch là:
A
0,7 gam.
B
1,4 gam.
C
2,8 gam.
D
14 gam.
Câu 8
Axetilen thường dùng làm nhiên liệu trong hàn cắt kim loại và trong công nghiệp vì
A
khi cháy tỏa nhiệt nhiều.
B
khi cháy không gây ô nhiễm môi trường.
C
giá thành thấp.
D
là nhiên liệu có sẵn trong tự nhiên
Câu 9
Cần tối đa bao nhiêu ml dung dịch brom 0,1 M để tác dụng tối đa với 0,224 lít axetilen ỏ điều kiện tiêu chuẩn?
A
100 .
B
5000 .
C
200.
D
2 .
Câu 10
Để đốt cháy 4,48 lít khí etilen cần phải dùng bao nhiêu lít không khí chứa 20% thể tích oxi ?Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
A
13,44.
B
6,72 .
C
67,2 .
D
22,4 .
Đúng 3
Bình luận (1)
Câu 1. B Câu 2. BCâu 3. DCâu 4. BCâu 5. CCâu 6. CCâu 7. BCâu 8. ACâu 9. ACâu 10. C
Đúng 0
Bình luận (1)
Câu 5. Đốt cháy hoàn toàn 5,6 lit hỗn hợp khí metan và etilen cần phải dùng vừa đủ 13,44 lit khí oxi.
a) Tính phần trăm thể tích mỗi khí trong hỗn hợp.
b) Tính thể tích khí CO2 sinh ra.
(Cho biết: C = 12, H = 1. Các thể tích khí đo ở đktc).
CH4+2O2-to>CO2+2H2O
x------2x---------x
C2H4+3O2-to>2CO2+2H2O
y----------3y--------2y
=>\(\left\{{}\begin{matrix}x+y=\dfrac{5,6}{22,4}\\2x+3y=\dfrac{13,44}{22,4}\end{matrix}\right.\)
=>x=0,15 mol , y=0,1 mol
=>%VCH4=\(\dfrac{0,15.22,4}{5,6}\).100=60%
=>%VC2H4=100-60=40%
b)
VCO2=(0,15+0,1.2).22,4=7,84l
Đúng 4
Bình luận (2)
mhh khí = 5,6/22,4 = 0,25 (mol)
nO2 = 13,44/22,4 = 0,6 (mol)
Gọi nC2H4 = a (mol); nCH4 = b (mol)
a + b = 0,25 (1)
PTHH:
C2H4 + 3O2 -> (t°) 2CO2 + 2H2O
Mol: a ---> 3a ---> 2a
CH4 + 2O2 -> (t°) CO2 + 2H2O
Mol: b ---> 2b ---> b
3a + 2b = 0,6 (2)
(1)(2) => a = 0,1 (mol); b = 0,15 (mol)
%VC2H4 = 0,1/0,25 = 40%
%VCH4 = 100% - 40% = 60%
VCO2 = (0,1 . 2 + 0,15) . 22,4 = 7,84 (l)
Đúng 1
Bình luận (0)