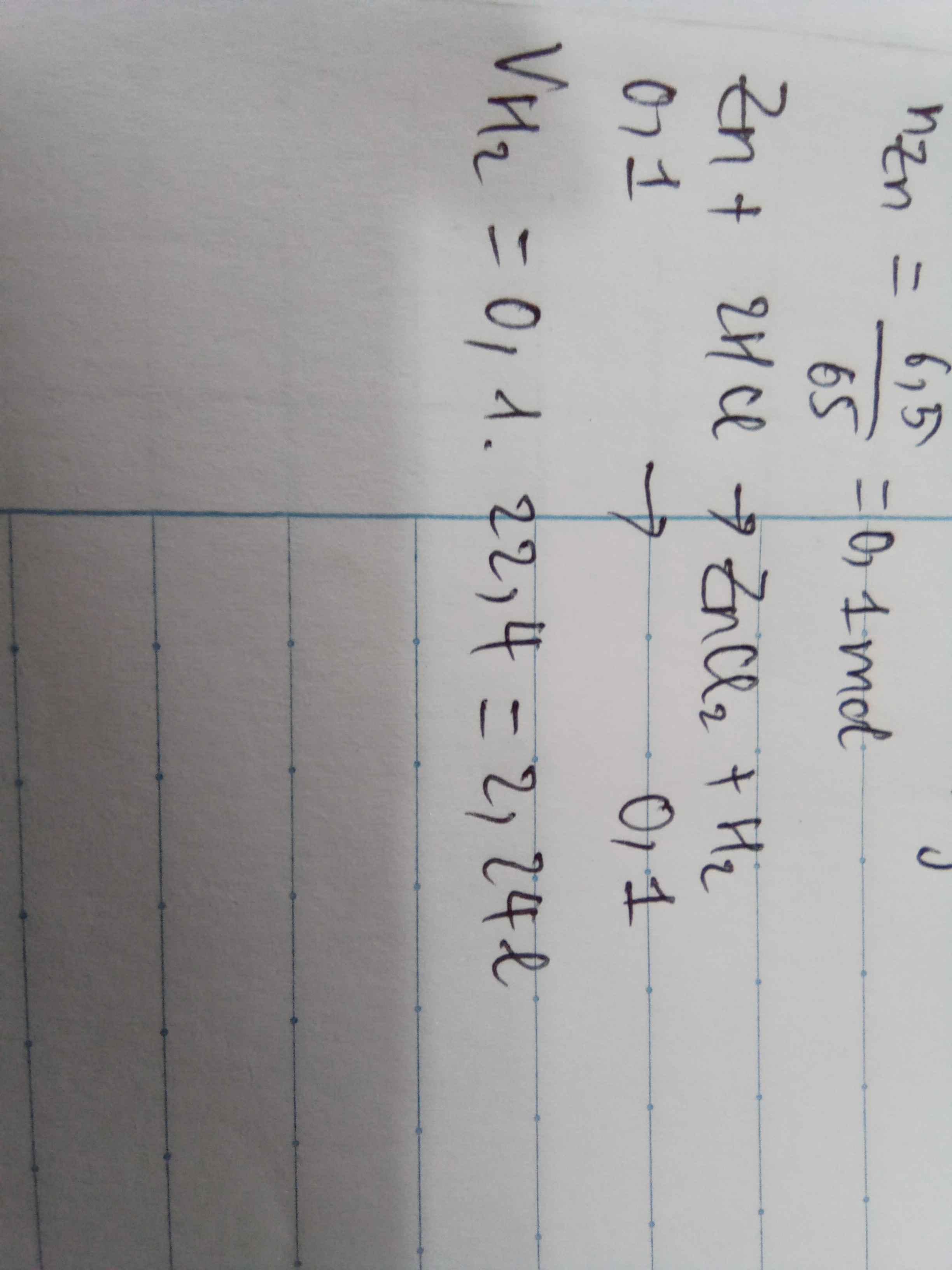Cho a gam Zn vào dung dịch axit chứa 5,48 gam HCl a, Tính a? b, Tính thể tích H2 (đktc)

Những câu hỏi liên quan
Cho 6.5 gam kẽm vào 200g dung dịch axit clohidric(HCl) thu được kẽm clorua(ZnCl2) và khí Hidro(H2)
a. TÍnh thể tích khí hidro(H2) thu được (ở đktc)
b Tính nồng độ phần trăm của dung dịch axit clohidric HCl đã dùng
Biết (H=1 ; Zn=65 ; Cl=35.5)
`Zn + 2HCl -> ZnCl_2 + H_2`
`0,1` `0,2` `0,1` `(mol)`
`n_[Zn]=[6,5]/65=0,1(mol)`
`a)V_[H_2]=0,1.22,4=2,24(l)`
`b)C%_[HCl]=[0,2.36,5]/200 . 100 =3,65%`
Đúng 4
Bình luận (3)
`Zn + HCl -> ZnCl_2 + H_2` `\uparrow`
`n_(Zn) = (6,5)/65 = 0,1 mol`.
`n_(H_2) = 0,1 mol`.
`V(H_2) = 0,1 xx 22,4 = 2,24l`.
`C%(HCl) = (0,2.36,5)/200 xx 100 = 36,5%`.
Đúng 3
Bình luận (2)
Cho 3,6 gam magie trên vào dung dịch chứa 14,6 gam axit clohidric (HCl) a. Hỏi sau phản ứng chất nào còn dư, dư bao nhiêu gam? b. Tính thể tích H2 (đktc)?
Đọc tiếp
Cho 3,6 gam magie trên vào dung dịch chứa 14,6 gam axit clohidric (HCl) a. Hỏi sau phản ứng chất nào còn dư, dư bao nhiêu gam? b. Tính thể tích H2 (đktc)?
Theo gt ta có: $n_{Mg}=0,15(mol);n_{HCl}=0,4(mol)$
$Mg+2HCl\rightarrow MgCl_2+H_2$
Do đó sau phản ứng thì HCl dư 0,1(mol)
Đúng 2
Bình luận (0)
PTHH: Mg + 2HCl → MgCl2 + H2
b. nMg = 3,6 : 24 = 0,15 (mol)
nHCl = 14,6 : 36,5 = 0,4 (mol)
Tỉ lệ: nMg/1<nHCl/2 ⇒ Mg hết, HCl dư
m HCl = 0,4 . 14,6 (g)
Vậy ....
Đúng 0
Bình luận (0)
Theo đề ra, ta có:
n\(_{Mg}\)= \(\dfrac{3,6}{24}\)=0,15 (mol)
n\(_{HCl}\)=\(\dfrac{14,6}{36,5}\)=0,4 (mol)
\(\Rightarrow\) PTHH: Mg + 2HCl\(\rightarrow\) MgCl\(_2\) + H\(_2\)
Mol: 0,15 0,4
So sánh: \(\dfrac{0,15}{1}\)<\(\dfrac{0,4}{2}\)\(\Rightarrow\) HCl dư, bài toán tính theo mol Mg.
Mg + 2HCl\(\rightarrow\) MgCl\(_2\) + H\(_2\)
Mol: 0,15\(\rightarrow\)0,3
\(\Rightarrow\)m\(_{HCl}\)\(_{\left(dư\right)}\)= (0,4 - 0,3).36,5 = 3,65 (g)
Đúng 0
Bình luận (0)
Cho 16.25 gam kẽm phản ứng vừa đủ với dung dịch axit clohidric theo sơ đồ sau Zn + HCL---> Zncl2 +H2 a tính khối lượng dung dịch axit clohidic đã phản ứng b tính thể tích khí sinh ra (đktc)?
a) Số mol kẽm tham gia phản ứng : \(n_{Zn}=\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{16,25}{65}=0,25\left(mol\right)\).
PTHH : \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Mol : 1 : 2 : 1 : 1
Mol : 0,25 → 0,5 → 0,25 → 0,5
Suy ra, số mol dung dịch Axit Clohidric \(HCl\) tham gia phản ứng là \(n_{HCl}=0,5\left(mol\right)\).
Khối lượng dung dịch đã dùng : \(m_{HCl}=n_{HCl}.M_{HCl}=\left(0,5\right).\left(36,5\right)=18,25\left(g\right)\).
b) Từ câu a, suy ra số mol khí Hidro sinh ra là \(n_{H_2}=0,25\left(mol\right)\).
Thể tích khí Hydro sinh ra là : \(V_{H_2}=n_{H_2}.22,4=\left(0,25\right).\left(22,4\right)=5,6\left(l\right)\)
Đúng 1
Bình luận (0)
Cho 6,5 gam Zn tác dụng hết với dung dịch axit HCl thu được muối ZnCl2 và thoát ra V lít khí H2 (đktc).
a) Viết phương trình hóa học xảy ra.
b) Tính thể tích khí H2 (đktc)
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
Đúng 2
Bình luận (0)
Cho 6,5 gam Zn tác dụng hết với dung dịch axit HCl thu được muối ZnCl2 và thoát ra V lít khí H2 (đktc).a) Viết phương trình hóa học xảy ra.b) Tính thể tích khí H2 (đktc)
Cho 15,6 g Zn vào dung dịch H2SO4 loãng chứa 39,2 g H2SO4.
a) Tính thể tích H2 thu được (đktc) biết thể tích H2 bị hoa hụt 5%.
b) Còn dư bao nhiêu gam sau phản ứng.
a) 4Al : 4 nguyên tử Nhôm
b) $2Al(OH)_3$ : 2 phân tử Nhôm hidroxit
c) $3O_2$ : 3 phân tử oxi
d) $12C_6H_{12}O_6$ : 12 phân tử glucozo
Đúng 2
Bình luận (0)
Diễn đạt các cách viết sau:
a) 4Al =>4 nguyên tử Al
b) 2 Al(OH)3=>2 nguyên tử nhôm hidroxit
c) 3O2 =>3 nt khí oxi
d) 12C6H12O6 =>12 nt đường sacarozo
Đúng 0
Bình luận (0)
. Hòa tan hoàn toàn 16,25 gam kim loại M (chưa rõ hóa trị) vào dung dịch axit HCl dư. Khi phản ứng kết thúc thu được 5,6 lít H2 (đktc).
a. Xác định kim loại M trong số các kim loại cho sau: Na=23; Cu=64; Zn=65.
b. Tính thể tích dung dịch HCl 0,2M cần dùng để hòa tan hết lượng kim loại này.
a) \(2M+2nHCl\rightarrow2MCl_n+nH_2\)
\(n_M=\dfrac{2}{n}n_{H_2}=\dfrac{0,5}{n}\left(mol\right)\)
Ta có : \(M_M=\dfrac{16,25}{\dfrac{0,5}{n}}=32,5n\)
Chạy nghiệm n
n=1 => M=32,5 (loại)
n=2 => M=65 ( chọn)
n=3 => M=97,5 (loại)
Vậy M là Zn
b) Ta có : \(n_{HCl}=2n_{H_2}=0,5\left(mol\right)\)
=> \(V_{HCl}=\dfrac{0,5}{0,2}=2,5\left(lít\right)\)
Đúng 2
Bình luận (0)
Cho a gam hỗn hợp gồm Zn và Al vào dung dịch axit clohiđric (HCl) dư. Sau phản ứng thu được 3,36 lít H2 ở đktc. Tính a?
\(n_{H_2}=\dfrac{3.36}{22.4}=0,15\left(mol\right)\)
PTHH : Zn + 2HCl -> ZnCl2 + H2 ( 1)
0,15 0,15
PTHH : 2Al + 6HCl -> 2AlCl3 + 3H2 ( 2 )
0,1 0,15
\(m_{Zn}=0,15.65=9,75\left(g\right)\)
\(m_{Al}=27.0,1=2,7\left(g\right)\)
\(m_{hh}=9,75+2,7=12,45\left(g\right)\)
Đúng 3
Bình luận (0)
nH2=3,36:22,4=0,15(mol)
có PTHH:
Zn+2HCl--->ZnCl2+H2
0,15 0,15(mol)
2Al+6HCl--->2AlCl3+3H2
0,1 0,15(mol)
mAl=0,1x27=2,7(g)
mZn=0,15x65=9,75(g)
ma=2,7+9,75=12,45(g)
Đúng 3
Bình luận (4)
Cho 6,5 gam Zn tác dụng hết với dung dịch axit HCl thu được muối ZnCl2 và thoát ra V lít khí H2 (đktc).
a) Viết phương trình hóa học xảy ra.
b) Tính thể tích khí H2 (đktc)
Đánh máy giúm nha
a, \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl ----> ZnCl2 + H2
Mol: 0,1 0,1
b, \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Đúng 1
Bình luận (0)