Tìm khối lượng của : a). 2,5 mol H2O b). 1,68 khí video ở điều kiện tiêu chuẩn

Những câu hỏi liên quan
Tìm khối lượng của : a). 2,5 mol H2O b). 1,68 khí hidro ở điều kiện tiêu chuẩn
a) \(m_{H_2O}=2,5.18=45\left(g\right)\)
b) \(n_{H_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\) => mH2 = 0,075.2 = 0,15(g)
Đúng 2
Bình luận (0)
\(a.m_{H_2O}=2,5.18=45\left(g\right)\)
\(b.n_{H_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
\(m_{H_2}=2.0,075=0,15\left(g\right)\)
Đúng 0
Bình luận (0)
Bài tập
1 tính khối lượng của
a) 0.5 mol Fe2O3
b) 0,15 mol CO2
c) 5,6 lít O2 ( điều kiện tiêu chuẩn )
d) 8,96 lít H2 ( điều kiện tiêu chuẩn)
2 tính thể tích ( điều kiện tiêu chuẩn)
a) 0,125 mol Cl2
b) 2,5 mol CH4
c) 6,4 gam 02
d) 5,6 gam N2
3 tính tỉ khối của khí O2 so với
a) khí N2
b) khí CO
c) không khí
3. a) MO2/MN2 = 32/28 = 8/7
b) MO2/MCO = 32/28 = 8/7
c) MO2/Mkk = 32/29
Đúng 0
Bình luận (0)
1 tính khối lượng của
a) 0.5 mol Fe2O3
\(M_{Fe_2O_3}=2\times56+3\times16=160\) (g/mol)
\(m_{Fe_2O_3}=n_{Fe_2O_3}\times M_{Fe_2O_3}=0,5\times112=56\left(g\right)\)
b) 0,15 mol CO2
\(M_{CO_2}=1\times12+2\times16=44\) (g/mol)
\(m_{CO_2}=n_{CO_2}\times M_{CO_2}=0,15\times44=6,6\left(g\right)\)
c) 5,6 lít O2 ( điều kiện tiêu chuẩn )
\(n_{O_2}=\frac{V_{O_2}}{22,4}=\frac{5,6}{22,4}=0,25\left(mol\right)\)
\(M_{O_2}=2\times16=32\) (g/mol)
\(m_{O_2}=n_{O_2}\times M_{O_2}=0,25\times32=8\left(g\right)\)
d) 8,96 lít H2 ( điều kiện tiêu chuẩn)
\(n_{H_2}=\frac{V_{H_2}}{22,4}=\frac{8,96}{22,4}=0,4\left(mol\right)\)
\(M_{H_2}=2\times1=2\) (g/mol)
\(m_{H_2}=n_{H_2}\times M_{H_2}=0,4\times2=0,8\left(g\right)\)
2 tính thể tích ( điều kiện tiêu chuẩn)
a) 0,125 mol Cl2
\(V_{Cl_2}=22,4\times n_{Cl_2}=22,4\times0,125=2,8\left(l\right)\)
b) 2,5 mol CH4
\(V_{CH_4}=22,4\times n_{CH_4}=22,4\times2,5=56\left(l\right)\)
c) 6,4 gam 02
\(M_{O_2}=2\times16=32\) (g/mol)
\(n_{O_2}=\frac{m_{O_2}}{M_{O_2}}=\frac{6,4}{32}=0,2\left(mol\right)\)
\(V_{O_2}=22,4\times n_{O_2}=22,4\times0,2=4,48\left(l\right)\)
d) 5,6 gam N2
\(M_{N_2}=2\times14=28\) (g/mol)
\(n_{N_2}=\frac{m_{N_2}}{M_{N_2}}=\frac{5,6}{28}=0,2\left(mol\right)\)
\(V_{N_2}=22,4\times n_{N_2}=22,4\times0,2=4,48\left(l\right)\)
3 tính tỉ khối của khí O2 so với
a) khí N2
\(d_{O_2;N_2}=\frac{M_{O_2}}{M_{N_2}}=\frac{2\times16}{2\times14}=\frac{8}{7}\)
b) khí CO
\(d_{O_2;CO}=\frac{M_{O_2}}{M_{CO}}=\frac{2\times16}{1\times12+1\times16}=\frac{8}{7}\)
c) không khí
\(d_{O_2;kk}=\frac{M_{O_2}}{M_{kk}}=\frac{2\times16}{29}=\frac{32}{29}\)
Đúng 0
Bình luận (2)
1. a) mFe2O3 = 0,5.160 = 80 (g)
b) mCO2 = 0,15.44 = 6,6 (g)
c) nO2 = 5,6/22,4 = 0,25 (mol) => mO2 = 0,25.32 = 8 (g)
d) nH2 = 8,96/22,4 = 0,4 (mol) => mH2 = 0,4.2 = 0,8 (g)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
a)Tính khối lượng mol của phân tử SO3
b)Tính khối lượng của 2, 24 lít khí SO3 ở điều kiện tiêu chuẩn
a) đề bài??
b)
\(n_{SO_3\left(dktc\right)}=\dfrac{V}{22,4}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ m_{SO_3}=n\cdot M=0,1\cdot\left(32+16\cdot3\right)=8\left(g\right)\)
Đúng 2
Bình luận (0)
Tính khối lượng của: a)7437 mL khí nitrogen ở điều kiện tiêu chuẩn b)2,479 lít khí chlorine ơ điều kiện tiêu chuẩn
\(a)7437ml=7,437l\\ n_{N_2}=\dfrac{7,437}{24,79}=0,3mol\\ m_{N_2}=0,3.28=8,4g\\ b)n_{Cl_2}=\dfrac{2,479}{24,79}=0,1mol\\ m_{Cl_2}=0,1.71=7,1g\)
Đúng 1
Bình luận (0)
A tính khối lượng của 0,6 mol o2 b tính khối lượng ở điều kiện tiêu chuẩn của 0,5 mol CO2
Xem chi tiết
\(a,m_{O_2}=n.M=0,6.\left(16.2\right)=19,2\left(g\right)\)
Thể tích ở điều kiện tc chứ nhỉ?
\(b,V_{CO_2}=n.22,4=0,5.22,4=11,2\left(g\right)\)
Đúng 0
Bình luận (0)
a) mO2= 0,6.32=19,2(g)
b) mCO2=0,5.44=22(g)
Nhưng sao khối lượng đktc nhỉ? Hay thể tích ta??
Đúng 0
Bình luận (0)
cho 2,5 gam nhôm vào bình chứa 0,5 mol dung dịch axit sunfuric loãng
a,Viết phương trình phản ứng
b,chất nào còn dư sau phản ứng Tính khối lượng chất dư
c,Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn
\(n_{Al}=\dfrac{2,5}{27}=\dfrac{25}{270}=\dfrac{5}{54}\left(mol\right)\\ n_{H_2SO_4}=0,5\left(mol\right)\\ a,2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ b,Vì:\dfrac{\dfrac{5}{54}}{2}< \dfrac{0,5}{4}\Rightarrow H_2SO_4dư\\ b,n_{H_2SO_4\left(dư\right)}=0,5-\dfrac{3}{2}.\dfrac{5}{54}=\dfrac{13}{36}\left(mol\right)\\ \Rightarrow m_{H_2SO_4}=\dfrac{13}{36}.98=\dfrac{637}{18}\left(g\right)\\ c,n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.\dfrac{5}{54}=\dfrac{5}{36}\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=\dfrac{5}{36}.22,4=\dfrac{28}{9}\left(l\right)\)
Đúng 5
Bình luận (2)
Tóm tắt:
mAl= 2,5(g)
\(n_{H_2SO_4}=0,5\left(mol\right)\)
---
a) PTHH?
b) Chất dư? m?
c) Thể tích khí sau phản ứng?
Anh ít tóm tắt lắm nên không biết tóm tắt như ri ổn không, vì em cần nên anh tóm tắt ra thử
Đúng 2
Bình luận (1)
cho 2,5 gam nhôm vào bình chứa 0,25 mol dung dịch axit sunfuric loãng a,Viết phương trình phản ứng b,chất nào còn dư sau phản ứng Tính khối lượng chất dư c,Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn
a: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b: \(n_{Al}=\dfrac{2.5}{27}< \dfrac{1}{4}\)
=>H2SO4 dư, Al đủ
\(m_{H_2SO_4}=0.25\cdot98=24.5\left(g\right)\)
c: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{2.5}{54}=\dfrac{5}{108}\left(mol\right)\)
\(\Leftrightarrow n_{H_2}=\dfrac{5}{36}\left(mol\right)\)
\(V_{H_2}=\dfrac{5}{36}\cdot22.4=\dfrac{28}{9}\left(lít\right)\)
Đúng 1
Bình luận (0)
Mình thấy bạn Thịnh tính lượng dư sai
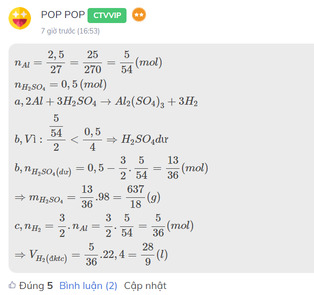
Đây là bài mình từng làm, bạn tham khảo nhé!
Đúng 1
Bình luận (2)
a. Thể tích của 0,8 mol khí NH3 (đktc) b. Thể tích ở đktc của 140 g khí Nitơ ; 96g khí Oxi c. Thể tích của hỗn hợp khí gồm 0,5 mol Cl2 và 0,2 mol N2 ở điều kiện tiêu chuẩn. d. Khối lượng của hỗn hợp 0,25 mol khí NH3 , 28lit khí CO.
\(a.V_{NH_3}=0,8.22,4=17,92\left(l\right)\\ b.n_{N_2}=\dfrac{140}{28}=5\left(mol\right)\\ V_{N_2}=112\left(l\right)\\ n_{O_2}=\dfrac{96}{32}=3\left(mol\right)\\ V_{O_2}=22,4.3=67,2\left(l\right)\)
\(c.n_{hh}=0,5+0,2=0,7\left(mol\right)\\ V_{hh}=0,7.22,4=15,68\left(l\right)\\ d.m_{NH_3}=4,25\left(g\right)\\ n_{CO}=\dfrac{28}{22,4}=1,25\left(mol\right)\\ m_{CO}=1,25.28=35\left(g\right)\\ m_{hh}=4,25+35=39,25\left(g\right)\)
Đúng 0
Bình luận (0)
a. Thể tích của 0,8 mol khí NH3 (đktc)
=>VNH3=0,8.22,4=17,92l
b. Thể tích ở đktc của 140 g khí Nitơ ; 96g khí Oxi
nN2=140\14.2=5 mol
nO2=96\32=3 mol
=>Vhh=(5+3).22,4=179,2l
c. Thể tích của hỗn hợp khí gồm 0,5 mol Cl2 và 0,2 mol N2 ở điều kiện tiêu chuẩn.
=>Vhh=(0,5+0,2).22,4=15,68l
d. Khối lượng của hỗn hợp 0,25 mol khí NH3 , 28lit khí CO.
n CO=28\22,4=1,25 mol
=>mhh=0,25.17+1,25.28=39,25g
Đúng 1
Bình luận (0)
đốt cháy một lượng khí A thu được 105,6 gam CO2 và 57,6 gam H2O. tìm công thức phân tử của khí A biết tỉ khối của khí A so với CH4 bằng 2,75
trộn khí A với N2 theo tỉ lệ 8:2 về khối lượng thu được hỗn hợp khí D. tính thể ở điều kiện tiêu chuẩn của 13,408 gam hỗn D