Giả chi tiết dễ hiểu giúp mình nha , cám ơnnnnnnnnnnnn!
Nhiệt phân hoàn toàn 15,8g KMnO2 để điều chế Oxi đủ Oxi hoá hết bao nhiêu lít CH4 . Khí CO2 thoát ra đủ tác dụng bao nhiêu g CaO. Tìm số g CaCO3 kết tủa ?
![]()
Phân hủy hoàn toàn 31,6g KMnO4 ( ở nhiệt độ cao )
1. Tính thể tích khí oxi tạo thành ( ở đktc )
2. Lượng oxi trên đủ đốt cháy hết bao nhiêu lít CH4 ( ở đktc )
3. Biết cứ 1 mol CH4 cháy hoàn toàn thì sinh ra 880KJ , hãy tính nhiệt lượng Q tạo ra hóa ra khí trên cháy hết
Biết K=39 , Mn=55, O=12, H=1, Mg=24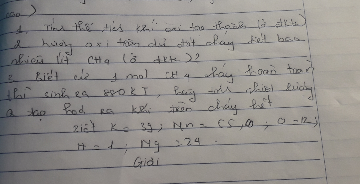
\(1) n_{KMnO_4}= \dfrac{31,6}{158} = 0,2(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{O_2} = \dfrac{1}{2}n_{KMnO_4} = 0,1(mol)\\ V_{O_2} = 0,1.22,4 = 2,24(lít)\\ 2) CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ V_{CH_4} = \dfrac{1}{2}V_{O_2} = 1,12(lít)\\ 3)n_{CH_4} = \dfrac{1,12}{22,4} = 0,05(mol)\\ \text{Nhiệt lượng tỏa ra = } = 0,05.880 = 44(KJ)\)
Đốt cháy hoàn toàn 18,6g Photpho thì cần dùng bao nhiêu lít ko khí có chứa 20% thể tích oxi?
Nếu dùng thuốc tím chứa 4& tạp chất về khối lượng để điều chế Oxi đủ cho phản ứng trên thì cần dùng bao nhiêu g chất này?
Help me - Gấp lắm
Nhiệt phân hoàn toàn 15,8g KMnO4 thu được bao nhiêu lít khí oxi ở điều kiện tiêu chuẩn? (K=39, Mn=55, O=16)
A. 1,12 lít B. 2,24 lít C. 3,36 lít D. 4,48 lít
\(n_{KMnO_4}=\dfrac{15,8}{158}=0,1mol\)
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,1 0,05 ( mol )
\(V_{O_2}=0,05.22,4=1,12l\)
-->A
\(n_{KMnO_4}=\dfrac{m}{M}=\dfrac{15,8}{158}=0,1mol\)
\(PTHH:2KMnO_4\underrightarrow{t^o}MnO_2+O_2+K_2MnO_4\)
\(2:1:1:1\) \(\left(mol\right)\)
\(0,1:0,05:0,05:0,05\) \(\left(mol\right)\)
\(V_{O_2}=n.22,4=0,05.22,4=1,12l\)
Chọn A
Nung hoàn toàn 12,15 g kali clorat KClO3 ở nhiệt độ cao thấy thoát ra V lít khí oxi thoát ra (đktc). a) Viết PTHH của phản ứng đã xảy ra b) Tính thể tích khí oxi thu được c) Tính khối lượng kẽm cần dùng khi phản ứng với lượng khí oxi được điều chế ở phản ứng trên
a)PTHH:2KClO\(_3\)➞\(^{t^o}\)2KCl+3O\(_2\)
b) n\(_{KClO_3}\)=\(\dfrac{m_{KClO_3}}{M_{KClO_3}}\)=\(\dfrac{12,15}{122,5}\)\(\approx\)0,1(m)
PTHH : 2KClO\(_3\) ➞\(^{t^o}\) 2KCl + 3O\(_2\)
tỉ lệ : 2 2 3
số mol : 0,1 0,1 0,15
V\(_{O_2}\)=n\(_{O_2}\).22,4=0,15.22,4=3,36(l)
c)PTHH : 2Zn + O\(_2\) -> 2ZnO
tỉ lệ : 2 1 2
số mol :0,3 0,15 0,3
m\(_{Zn}\)=n\(_{Zn}\).M\(_{Zn}\)=0,3.65=19,5(g)
Nung nóng 15,8g KMnO4 ở nhiệt độ cao.
a.Tính thể tích khí oxi ở đktc.
b tính khối lượng KMnO4 cần dùng để sinh ra một lượng oxi đủ để đốt cháy hết 1,68g sắt. Biết hiệu xuâtphản ứng điều chế khí oxi là 95‰
a) \(n_{KMnO_4}=\dfrac{15,8}{158}=0,1\left(mol\right)\)
\(PTHH:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
(mol)..........0,1................0,05..........0,05......0,05
\(V_{O_2}=0,05.22,4=1,12\left(l\right)\)
b) \(n_{Fe}=\dfrac{1.68}{56}=0,03\left(mol\right)\)
\(PTHH:3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
(mol).......0,03....0,02.......0,1
\(PTHH:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
(mol)..........0,04..............0,02............0,02....0,02
\(m_{KMnO_4}=0,04.158=6,32\left(g\right)\)
\(m_{KMnO_4\left(thựctế\right)}=6,32:95\%\approx6,65\left(g\right)\)
PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Ta có: \(n_{KMnO_4}=\dfrac{59,25}{158}=0,375\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{KMnO_4}=0,1875\left(mol\right)\)
Giả sử: \(\left\{{}\begin{matrix}n_{CO}=x\left(mol\right)\\n_{CO_2}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{6,72}{22,4}=0,3\left(1\right)\)
Các quá trình:
\(C^0\rightarrow C^{+2}+2e\)
x__________ 2x (mol)
\(C^0\rightarrow C^{+4}+4e\)
y__________ 4y (mol)
\(O_2^0+4e\rightarrow2O^{-2}\)
0,1875_0,75 (mol)
Theo ĐLBT mol e, có: 2x + 4y = 0,75 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,225\left(mol\right)\\y=0,075\left(mol\right)\end{matrix}\right.\)
Ở cùng điều kiện nhiệt độ và áp suất, % số mol cũng là %V.
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,225}{0,3}100\%=75\%\text{ }\\\%V_{CO_2}=25\%\end{matrix}\right.\)
Bạn tham khảo nhé!
cho 7(g) CaCO3 tác dụng với 5,475(g) HCl tạo thành CaCl2, khí CO2 và H2O. cần lấy thêm bao nhiêu Gam CaCO3 hay bao nhiêu Gam HCl để PƯ sảy ra hoàn toàn
\(n_{CaCO_3}=\dfrac{7}{100}=0,07\left(mol\right)\)
\(n_{HCl}=\dfrac{5,475}{36,5}=0,15\left(mol\right)\)
PTHH: CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
Xét \(\dfrac{n_{CaCO_3}}{1}=0,07< \dfrac{n_{HCl}}{2}=0,075\)
=> HCl dư
Do đó, ta có:
PTHH: CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
_______0,075<---0,15__________________________(mol)
=> \(m_{CaCO_3\left(cầnthêm\right)}=\left(0,075-0,07\right).100=0,5\left(g\right)\)
Nhiệt phân hoàn toàn 31,6 g kalipemanganat sinh ra V (lít) khí ở đktc
a. Viết các PTHH xảy ra. Tìm V.
b. Cho toàn bộ lượng khí oxi thu được ở trên tác dụng với 7,2 g magie. Chất nào còn dư sau khi phản ứng của oxi với magie, khối lượng chất dư là bao nhiêu gam? Tính khối lượng chất rắn sau phản ứng.
Mn giúp e với ạ
PTHH:
2KMnO4 -to> K2MnO4 + MnO2 + O2
0,2------------------------------------------0,1
n KMnO4=\(\dfrac{31,6}{158}\)=0,2 mol
=>VO2=0,1.22,4=2,24l
b)2Mg+O2-to>2MgO
0,2----0,1----0,2
n Mg=\(\dfrac{7,2}{24}\)=0,3 mol
=>Mg dư :0,1 mol
=>mMg=0,1.24=2,4g
=>m MgO=0,2.40=8g
Để điều chế khí oxi trong phòng thí nghiệm người ta nhiệt phân KMnO4 ở nhiệt độ cao
a) Để thu được 22,4 lít khí oxi ở đktc thì cần dùng bao nhiêu gam KMnO4
b) Dùng lượng khí oxi trên để đốt than (thành phần chính là cacbon C). Tính lượng CO2 sinh ra ở đktc
"M.n cứu em bài này với ạ không là em sắp thi rồi ạ"
a. \(n_{O_2}=\dfrac{22.4}{22.4}=1\left(mol\right)\)
PTHH : 2KMnO4 ----to----> K2MnO4 + MnO2 + O2
2 1
\(m_{KMnO_4}=2.158=316\left(g\right)\)
b. PTHH : C + O2 ---to--->CO2
1 1 1
\(m_{CO_2}=1.44=44\left(g\right)\)
a. n O 2 = 22.4 22.4 = 1 ( m o l ) PTHH : 2KMnO4 ----to----> K2MnO4 + MnO2 + O2 2 1 m K M n O 4 = 2.158 = 316 ( g ) b. PTHH : C + O2 ---to--->CO2 1 1 1 m C O 2 = 1.44 = 44 ( g )