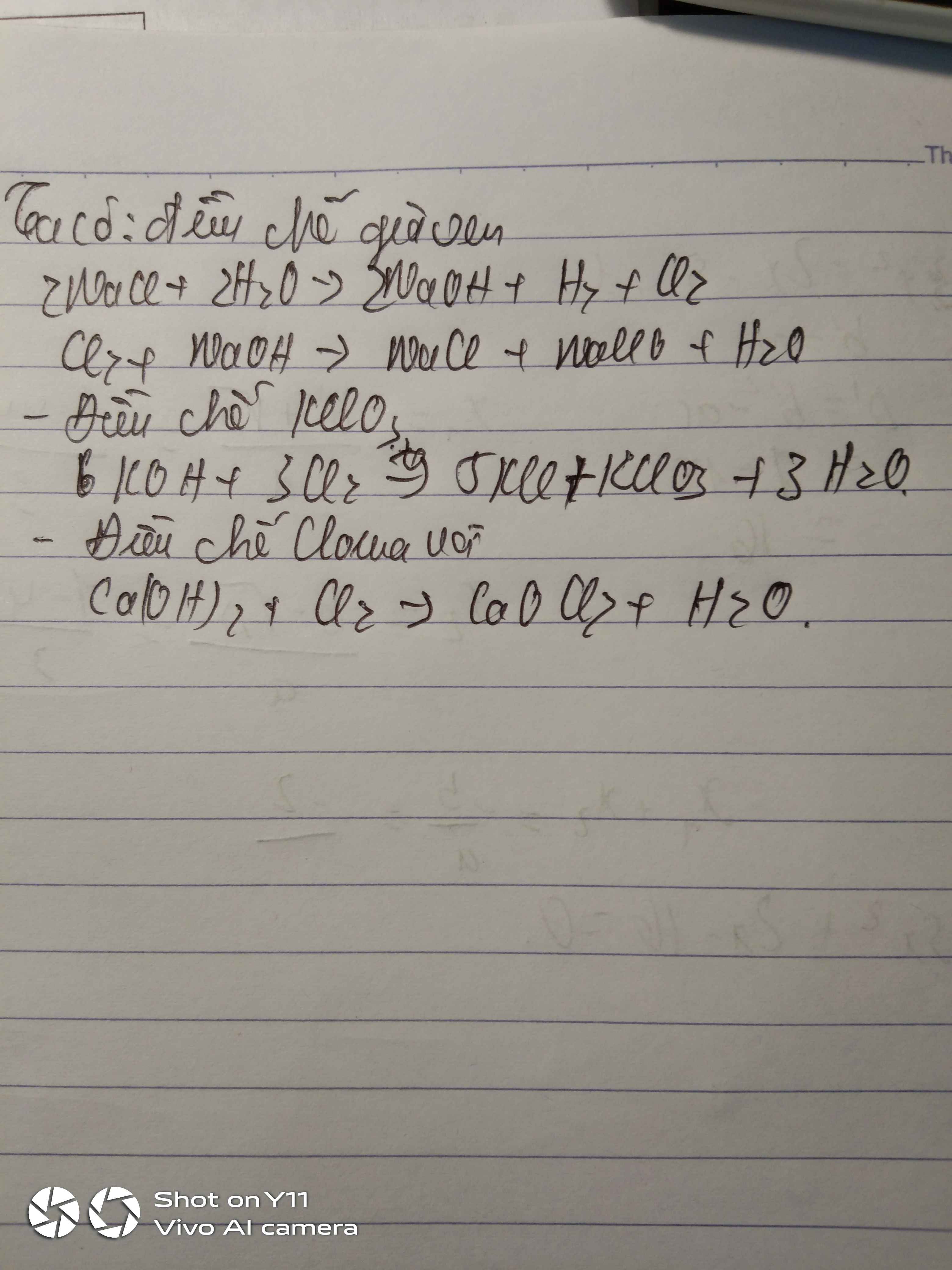Không dùng thêm hóa chất trong phòng thí nghiệm. Hãy tìm cách nhận biết 3 chất lỏng trong suốt Ca(OH)2, NaHCO3, H2O

Những câu hỏi liên quan
Bằng phương pháp hoá học hãy nhận biết 2 chất lỏng trong suốt không màu: nước H2O và nước vôi trong Ca(OH)2. Viết chương trình hoá học xảy ra (nếu có)
- Trích 2 chất thành các mẫu thử có đánh stt
- Sục CO2 vào từng mẫu thử, mẫu thử nào xuất hiện kết tủa trắng là dd nước vôi trong Ca(OH)2
PTHH : CO2 + Ca(OH)2 ----> CaCO3 + H2O
- Còn lại là H2O không hiện tượng
Đúng 0
Bình luận (2)
- Dùng quỳ tím
+) Quỳ tím hóa xanh: Ca(OH)2
+) Quỳ tím không đổi màu: H2O
Đúng 0
Bình luận (0)
Trích 2 chất thành các mẫu thử có đánh stt
- Sục CO2 vào từng mẫu thử, mẫu thử nào xuất hiện kết tủa trắng là dd nước vôi trong Ca(OH)2
PTHH : CO2 + Ca(OH)2 ----> CaCO3 + H2O
- Còn lại là H2O không hiện tượng
Đúng 0
Bình luận (0)
Câu 2 (2,0 điểm):Có các gói chất bột màu trắng đựng trong các lọ không ghi tên (nhãn): CaO, Ca, CaCO3, NaCl, Al. Hãy nêu cách tiến hành thí nghiệm để nhận biết mỗi chất trên. Biết rằng nhôm tan được trong kiềm theo sơ đồ phản ứng:Al + H2O + R(OH)xR(AlO2)x + H2(sủi bọt) (R là kim loại trong kiềm).
Đọc tiếp
Câu 2 (2,0 điểm):Có các gói chất bột màu trắng đựng trong các lọ không ghi tên (nhãn): CaO, Ca, CaCO3, NaCl, Al. Hãy nêu cách tiến hành thí nghiệm để nhận biết mỗi chất trên. Biết rằng nhôm tan được trong kiềm theo sơ đồ phản ứng:
Al + H2O + R(OH)x![]() R(AlO2)x + H2(sủi bọt) (R là kim loại trong kiềm).
R(AlO2)x + H2(sủi bọt) (R là kim loại trong kiềm).
Trích mẫu thử
Cho nước vào các mẫu thử :
- mẫu thử nào tan tạo khí không màu là Ca
\(Ca + 2H_2O \to Ca(OH)_2 + H_2\)
- mẫu thử nào tan tỏa nhiều nhiệt là CaO
\(CaO + H_2O \to Ca(OH)_2\)
- mẫu thử nào tan là NaCl
Cho dung dịch NaOH vào hai mẫu thử còn :
- mẫu thử nào tan, tạo khí không màu là Al
\(2NaOH + 2H_2O + 2Al \to 2NaAlO_2 + 3H_2\)
- mẫu thử không tan là CaCO3
Đúng 1
Bình luận (0)
Trong phòng thí nghiệm có 3 lọ hóa chất không màu gồm: dung dịch HCl, dung dịch H2SO4 loãng, nước cất. Em hãy trình bày phương pháp hóa học dùng để nhận biết mỗi lọ hóa chất đó. Viết phương trình hóa học minh họa (nếu có
Dùng quỳ tím:
+ Chuyển màu là \(H_2SO_4,HCl\)
+ Không chuyển màu là nước cất
Dùng \(BaCl_2\):
+ Tạo phản ứng kết tủa: \(H_2SO_4\)
+ Không phản ứng: \(HCl\)
\(PTHH:H_2SO_4+BaCl_2\rightarrow BaSO_4+2HCl\)
Đúng 1
Bình luận (1)
Nhận biếta/Có 3 lọ không nhãn, mỗi lọ đựng một dung dịch muối sau: CuSO4, AgNO3, NaCl. Hãy dùng những dung dịch có sẵn trong phòng thí nghiệm để nhận biết chất đựng trong mỗi lọ. Viết các phương trình hóa học.b/ Bằng phương pháp hóa học em hãy nhận biết 2 dung dịch HCl và H2SO4 loãng đựng trong hai lọ bị mất nhãn. Làm nhanh giúp mik vs ạ!
Đọc tiếp
Nhận biết
a/Có 3 lọ không nhãn, mỗi lọ đựng một dung dịch muối sau: CuSO4, AgNO3, NaCl. Hãy dùng những dung dịch có sẵn trong phòng thí nghiệm để nhận biết chất đựng trong mỗi lọ. Viết các phương trình hóa học.
b/ Bằng phương pháp hóa học em hãy nhận biết 2 dung dịch HCl và H2SO4 loãng đựng trong hai lọ bị mất nhãn.
Làm nhanh giúp mik vs ạ!
a, - Trích mẫu thử.
- Cho từng mẫu thử pư với dd NaCl.
+ Có tủa trắng: AgNO3.
PT: \(AgNO_3+NaCl\rightarrow AgCl_{\downarrow}+NaNO_3\)
+ Không hiện tượng: CuSO4, NaCl. (1)
- Cho mẫu thử nhóm (1) pư với dd BaCl2.
+ Có tủa trắng: CuSO4.
PT: \(CuSO_4+BaCl_2\rightarrow BaSO_{4\downarrow}+CuCl_2\)
+ Không hiện tượng: NaCl.
- Dán nhãn.
b, - Trích mẫu thử.
- Cho từng mẫu thử pư với dd BaCl2.
+ Có tủa trắng: H2SO4
PT: \(BaCl_2+H_2SO_4\rightarrow2HCl+BaSO_{4\downarrow}\)
+ Không hiện tượng: HCl
- Dán nhãn.
Đúng 2
Bình luận (0)
Cho các chất: NaCl, KMnO4, KOH, NaOH, Ca(OH)2, H2SO4, H2O. Từ các hóa chất đã cho, viết các phương trình hóa họcxảy ra khi điều chế các chất sau trong phòng thí nghiệm: a. nước giaven. b. clorua vôi.c. kaliclorat.
Đọc tiếp
Cho các chất: NaCl, KMnO4, KOH, NaOH, Ca(OH)2, H2SO4, H2O. Từ các hóa chất đã cho, viết các phương trình hóa họcxảy ra khi điều chế các chất sau trong phòng thí nghiệm:
a. nước giaven. b. clorua vôi.c. kaliclorat.
a) Nước Gia-ven:
\(2NaCl+H_2O\underrightarrow{đpkmn}NaCl+NaClO+H_2\)
b) Clorua vôi
\(2NaCl+2H_2O\underrightarrow{đpcmn}2NaOH+H_2+Cl_2\)
\(Cl_2+Ca\left(OH\right)_2\rightarrow CaOCl_2+H_2O\)
c)
\(6KOH+3Cl_2\underrightarrow{t^o}5KCl+KClO_3+3H_2O\)
Đúng 3
Bình luận (0)
5: Phản ứng nào dưới đây là phản ứng hóa hợp? A. CuO + H2_10 Cu +H2OB. CO2 + Ca(OH)21° CaCO3 + H2O C. 2KMnO4 10 KMnO4 + MnO2 + O2 D. CaO + H200 Ca(OH)2 Câu 6. Những chất được dùng để điều chế oxi trong phòng thí nghiệm là A. KClO3 và KMnO4 .B. KMnO4 và H2O. C. KClO3 và CaCO3 .D. KMnO4 và không khí. Câu 7: Nhóm công thức nào sau đây biểu diễn toàn oxit? A. CuO, CaCO3, SO3B. N2O5 ; Al2O3 ; SiO2C. FeO; KC1, P2O5 D. CO2 ; H2SO4; MgO Câu 8: Phản ứng hoá học có xảy ra sự oxi hoá làA. 4NH3 + 502 + 4NO...
Đọc tiếp
5: Phản ứng nào dưới đây là phản ứng hóa hợp?
A. CuO + H2_10> Cu +H2O
B. CO2 + Ca(OH)21° > CaCO3 + H2O
C. 2KMnO4 10 KMnO4 + MnO2 + O2
D. CaO + H200 Ca(OH)2
Câu 6. Những chất được dùng để điều chế oxi trong phòng thí nghiệm là
A. KClO3 và KMnO4 .
B. KMnO4 và H2O.
C. KClO3 và CaCO3 .
D. KMnO4 và không khí.
Câu 7: Nhóm công thức nào sau đây biểu diễn toàn oxit?
A. CuO, CaCO3, SO3
B. N2O5 ; Al2O3 ; SiO2
C. FeO; KC1, P2O5
D. CO2 ; H2SO4; MgO
Câu 8: Phản ứng hoá học có xảy ra sự oxi hoá là
A. 4NH3 + 502 + 4NO + 6H2O
B. Na2O + H2O → 2NaOH
C. CaCO3 +CaO + CO2
D. Na2SO4 + BaCl2 → BaSO4 + 2NaCl
Câu 9: Đốt cháy hoàn toàn 2,4 gam Mg trong khí oxi dư thu được khối lượng MgO làm
A. 4 gam.
B. 4,3 gam.
C. 4,6 gam.
D. 4.9 gam.
Câu 10: Khối lượng KMnO4 cần dùng để điều chế 1,12 lít khí oxi là
A. 7,9 gam.
B. 15,8 gam.
C. 3,95 gam.
D. 14,2 gam.
Câu 11: Người ta không nên dùng nước để dập tắt đám cháy bằng xăng dầu vì
A. xăng dầu không tan trong nước, nhẹ hơn nước.
B. xăng dầu cháy mạnh trong nước.
C. xăng dầu nặng hơn nước.
D. xăng dầu cháy mạnh hơn khi có nước.
Câu 12: Đốt cháy hoàn toàn 3,1 gam P trong bình chứa 5,6 lít khí oxi thu được khối lượng P2O5 là
A.9,1 gam. B. 8,1 gam. C. 7,1 gam. D. 6,1 gam.
5: Phản ứng nào dưới đây là phản ứng hóa hợp?
A. CuO + H2_10> Cu +H2O
B. CO2 + Ca(OH)21° > CaCO3 + H2O
C. 2KMnO4 10 KMnO4 + MnO2 + O2
D. CaO + H200 Ca(OH)2
Câu 6. Những chất được dùng để điều chế oxi trong phòng thí nghiệm là
A. KClO3 và KMnO4 .
B. KMnO4 và H2O.
C. KClO3 và CaCO3 .
D. KMnO4 và không khí.
Câu 7: Nhóm công thức nào sau đây biểu diễn toàn oxit?
A. CuO, CaCO3, SO3
B. N2O5 ; Al2O3 ; SiO2
C. FeO; KC1, P2O5
D. CO2 ; H2SO4; MgO
Câu 8: Phản ứng hoá học có xảy ra sự oxi hoá là
A. 4NH3 + 502 + 4NO + 6H2O
B. Na2O + H2O → 2NaOH
C. CaCO3 +CaO + CO2
D. Na2SO4 + BaCl2 → BaSO4 + 2NaCl
Câu 9: Đốt cháy hoàn toàn 2,4 gam Mg trong khí oxi dư thu được khối lượng MgO làm
A. 4 gam.
B. 4,3 gam.
C. 4,6 gam.
D. 4.9 gam.
Câu 10: Khối lượng KMnO4 cần dùng để điều chế 1,12 lít khí oxi là
A. 7,9 gam.
B. 15,8 gam.
C. 3,95 gam.
D. 14,2 gam.
Câu 11: Người ta không nên dùng nước để dập tắt đám cháy bằng xăng dầu vì
A. xăng dầu không tan trong nước, nhẹ hơn nước.
B. xăng dầu cháy mạnh trong nước.
C. xăng dầu nặng hơn nước.
D. xăng dầu cháy mạnh hơn khi có nước.
Câu 12: Đốt cháy hoàn toàn 3,1 gam P trong bình chứa 5,6 lít khí oxi thu được khối lượng P2O5 là
A.9,1 gam. B. 8,1 gam. C. 7,1 gam. D. 6,1 gam.
Đúng 2
Bình luận (0)
có 3 lọ không nhãn mỗi lọ đựng một dung dịch muối sau cuso4, AgNO3, Na2SO4. Hãy dùng những dung dịch có sẵn trong phòng thí nghiệm để nhận biết chất đựng trong mỗi lọ. VIết các phương trình hóa học
- Trích mẫu thử, cho \(Ba\left(OH\right)_2\) vào các mẫu thử:
+ Tạo dd màu xanh lá và kết tủa trắng là \(CuSO_4\)
- Cho 2 mẫu thử còn lại vào dd \(HCl\):
+ Tạo kết tủa trắng là \(AgNO_3\)
+ Ko ht là \(Na_2SO_4\)
\(PTHH:CuSO_4+BaCl_2\rightarrow CuCl_2+BaSO_4\downarrow\\ AgNO_3+HCl\rightarrow AgCl\downarrow+HNO_3\)
Đúng 1
Bình luận (1)
Có 3 lọ không nhãn, mỗi lọ đựng dung dịch muối sau: CuSO4, AgNO3, NaCl. Hãy dùng những dung dịch muối BaCl2 trong phòng thí nghiệm để nhận biết chất đựng trong mỗi lọ. Viết các phương trình hóa học.
CuSO4, AgNO3, NaCl
BaCl2 ↓trắng ↓trắng ∅
NaCl ↓nâu ↓trắng sữa
- Lấy mỗi chất một ít cho vào ống nghiệm, đánh STT, sau đó nhỏ dung dịch BaCl2 vào từng ống.
(BaCl2+2AgNO3→Ba(NO3)2+2AgCl ; BaCl2+CuSO4→BaSO4+CuCl2)
+ Thấy xuất hiện kết tủa là AgNO3 và CuSO4 còn lại là NaCl.
- Nhỏ dung dịch NaCl vào 2 dung dịch AgNO3 và CuSO4
+ Xuất hiện kết tủa màu trắng sữa là AgCl chất ban đầu là AgNO3.
( AgNO3 + NaCl ➝ AgCl + NaNO3 )
+ Thấy dung dịch có màu xanh lá cây và có kết tủa màu nâu là CuCl2 và chất ban đầu là CuSO4.
( CuSO4 + NaCl → CuCl2 + Na2SO4 )
Đúng 0
Bình luận (1)
Trong phòng thí nghiệm có các dung dịch và chất lỏng đựng trong các bình mất nhãn riêng biệt gồm NH4HCO3, Ba(HCO3)2, C6H5ONa (natri phenolat), C6H6 (benzen), C6H5NH2 (anilin) và KAlO2 hoặc K[Al(OH)4]. Hãy chọn một thuốc thử để nhận biết trực tiếp các dung dịch và chất lỏng trên? A. Dung dịch NaOH. B. Dung dịch H2SO4. C. Dung dịch BaCl2. D. Quỳ tím.
Đọc tiếp
Trong phòng thí nghiệm có các dung dịch và chất lỏng đựng trong các bình mất nhãn riêng biệt gồm NH4HCO3, Ba(HCO3)2, C6H5ONa (natri phenolat), C6H6 (benzen), C6H5NH2 (anilin) và KAlO2 hoặc K[Al(OH)4]. Hãy chọn một thuốc thử để nhận biết trực tiếp các dung dịch và chất lỏng trên?
A. Dung dịch NaOH.
B. Dung dịch H2SO4.
C. Dung dịch BaCl2.
D. Quỳ tím.