̣Cho 10g MgO tác dụng hoàn toàn với dd 500ml dd (axit clohidric) HCl dư.
a. Tính nồng độ mol dd axit
b. Tính nồng độ mol dd MgCl 2
mong moi nguoi giup em
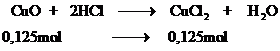
Cho 10g CuO tác dụng hoàn toàn với dd 500ml dd (axit clohidric) HCl dư. Tính nồng độ dd CuCl2 tạo thành?

 Số mol
Số mol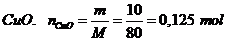
Pt:

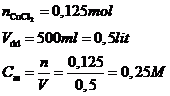
Số mol  tạo thành
tạo thành
Thể tích dd :
Nồng độ dd
cho 43,5gam MnO2 tác dụng hết với 250gam dd HCl thu được khí A. dẫn khí A qua 400ml dd NaOH 5M thu được dd B
a) tính nồng độ mol các muối trong dd B
b) Tính C% của dd HCl ban đầu (dùng dư 10% so với phản ứng)
MnO2+4HCl->MnCl2+H2O+Cl2
0,5---------2------0,5--------0,5---0,5
Cl2+2NaOH->NaClO+NaCl+H2O
0,5-----1--------0,5----------0,5------0,5
n MnO2 =\(\dfrac{43.5}{87}\)=0,5 mol
n NaOH=5.0,4=2 mol
=>NaOH dư :0,1 mol
=>CM NaCl= CM NaClO =\(\dfrac{1}{0,4}\)=2,5M
=>CM NaOH dư =1\(\dfrac{1}{0,4}\)=2,5M
b)
C%HCl =\(\dfrac{2.36,5}{250}100\)=29,2%
dùng dư 10%
=>C%HCl=29,2+10=39,2%
Bài 3: Hòa tan 200ml dd BaCl2 0,5M với 400ml dd Na2SO4 0,2M. Tính nồng độ mol các ion sau pư.
Bài 4: Cho 150ml dd HCl 2M tác dụng với 50ml dd Ba(OH)2 2,8M. Tính nồng độ mol các ion sau pư.
3.
\(n_{Ba^{2+}}=0,5.0,2=0,1\left(mol\right)\Rightarrow\left[Ba^{2+}\right]=\dfrac{0,1}{0,2+0,4}=0,17M\)
\(n_{Cl^-}=2.0,5.0,2=0,2\left(mol\right)\Rightarrow\left[Cl^-\right]=\dfrac{0,2}{0,2+0,4}=0,33M\)
\(n_{Na^+}=2.0,2.0,4=0,16\left(mol\right)\Rightarrow\left[Na^+\right]=\dfrac{0,16}{0,2+0,4}=0,27M\)
\(n_{SO_4^{2-}}=0,2.0,4=0,08\left(mol\right)\Rightarrow\left[SO_4^{2-}\right]=\dfrac{0,08}{0,2+0,4}=0,13M\)
4.
\(n_{H^+}=n_{Cl^-}=2.0,15=0,3\left(mol\right)\Rightarrow\left[Cl^-\right]=\left[H^+\right]=\dfrac{0,3}{0,15+0,05}=1,5M\)
\(n_{Ba^{2+}}=0,05.2,8=0,14\left(mol\right)\Rightarrow\left[Ba^{2+}\right]=\dfrac{0,14}{0,15+0,05}=0,7M\)
\(n_{OH^-}=2.0,05.2,8=0,28\left(mol\right)\Rightarrow\left[OH^-\right]=\dfrac{0,28}{0,15+0,05}=1,4M\)
cho 100g dd CH3cooh 12% tác dụng vừa đủ dd NaHCo3 8,4%.
a, tính khối lượng NaHCo3 đã dùng.
b, Tính nồng độ % của dd muối thu đc sau sản phẩm
a) \(n_{CH_3COOH}=\dfrac{100.12\%}{60}=0,2\left(mol\right)\)
PTHH: CH3COOH + NaHCO3 --> CH3COONa + CO2 + H2O
0,2-------->0,2----------->0,2--------->0,2
=> mNaHCO3 = 0,2.84 = 16,8 (g)
=> \(m_{dd.NaHCO_3}=\dfrac{16,8.100}{8,4}=200\left(g\right)\)
b) mCH3COONa = 0,2.82 = 16,4 (g)
mdd sau pư = 100 + 200 - 0,2.44 = 291,2 (g)
=> \(C\%_{dd.muối}=\dfrac{16,4}{291,2}.100\%=5,632\%\)
cho 100g dd CH3cooh 12% tác dụng vừa đủ dd NaHCo3 8,4%.
a, tính khối lượng NaHCo3 đã dùng.
b, Tính nồng độ % của dd muối thu đc sau sản phẩm
\(m_{ct}=\dfrac{12.100}{100}=12\left(g\right)\)
\(n_{CH3COOH}=\dfrac{12}{60}=0,2\left(mol\right)\)
Pt : \(CH_3COOH+NaHCO_3\rightarrow CH_3COONa+CO_2+H_2O|\)
1 1 1 1 1
0,2 0,2 0,2 0,2
a) \(n_{NaHCO3}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{NaHCO3}=0,2.84=16,8\left(g\right)\)
\(m_{ddNaHCO3}=\dfrac{16,8.100}{8,4}=200\left(g\right)\)
b) \(n_{CH3COONa}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{CH3COONa}=0,2.82=16,4\left(g\right)\)
\(m_{ddspu}=100+200-\left(0,2.44\right)=291,2\left(g\right)\)
\(C_{CH3COONa}=\dfrac{16,4.100}{291,2}=5,63\)0/0
Chúc bạn học tốt
1.cho dd chua 100 ml dd AgNO3 1M tac dung hoan toan voi 200 ml dd NaCl 1M
a. Tinh khôi lượng kết tủa tạo thành
b. Tinh nồng độ mol/lit cua các chất trong dd tạo thành.
2, cho 2.74 g Ba hoa tan hoan toan vao H2O tao thanh dd X .
a. Tinh khoi luong H2 tao thanh
b. Cho dd X pứ voi dd H2SO4 dư. Tinh so gam ket tủa tao thanh.
3, Cho m gam (sắt ôxit) FeO tác dụng hết với 600ml dd HCl (axit clohidric) đặc tạo thành dd (sắt clorua) FeCl2 0,2M. Tính m?
hòa tan hoàn toàn 9,6 gam hỗn hợp mgco3 cần 100 gam dd hcl 14,6%
a) tính thể tích mỗi khi thu được
b) tính nồng độ phần trăm của dd sau phản ứng
Ta có ptpu
MgCO3+ 2HCl ----> MgCl2 + H2O+ CO2
\(n_{MgCO3}\)= \(\frac{9,6}{84}\)= \(\frac{0,8}{7}\) ( mol)
\(m_{HCl}\)= \(\frac{14,6}{100}.100\)= 14,6(g)
=> \(n_{HCl}\)= \(\frac{14,6}{36,5}=0,4\left(mol\right)\)
Theopt ta thấy sau phản ứng HCl dư và dư \(\frac{1,2}{7}\) mol==> m dư= 6,26 (g)
=> \(n_{CO2}\)= \(n_{MgCO3}\)= \(\frac{0,8}{7}\) mol
=> \(V_{CO2}\)= \(\frac{0,8}{7}.22,4=2,56\left(l\right)\)
b)
Ta có \(m_{CO2}\)= \(\frac{0,8}{7}.44=\frac{35,2}{7}\left(g\right)\)
\(m_{H2O}\)= \(\frac{0,8}{7}.18=\frac{14,4}{7}\)( g)
\(m_{MgCl2}\)= \(\frac{0,8}{7}.95=\frac{76}{7}\)(g)
=> \(m_{dd_{MgCl2}}\)= (9,6+100)-( \(\frac{49,6}{7}\))= 102,5(g)
=> \(C\%_{MgCl2}\)= \(\frac{\frac{76}{7}}{102,5}\). 100%= 10,6 ( %)
\(C\%_{HCl_{dư}}\)= \(\frac{6,26}{102,5}.100\)=6,107 ( %)
đề có hơi vô lý một tý nha: hỗn hợp thì phải 2 chất trở lên, nhưng trong đề chỉ có mỗi MgCO3....Đề ghi vậy thì anh làm theo đề nha
mHCl=(14.6*100)/100=14.6g=>nHCl=0.4 mol
nMgCO3=9.6/84=4/35\(\approx\) 0.114mol
theo pthh,HCl dư 2/7 mol=>mHCl dư=73/7g
MgCO3+2HCl --> MgCl2 + CO2+H2O
4/35 0.4 4/35 4/35
a)Vco2=(4/35)*22.4=2.56l
b)C%HCl dư=(73/7)/100*100=76/7\(\approx\) 10.42%
mMgCl2=4/35*95=76.7g
C%MgCl2=(76.7)/100*100=76/7\(\approx\) 10.85%
Chúc em học tốt!!1
Cho 30 , 6 g hỗn hợp X Cu và Fe3O4 tác dụng vs 500 ml dd HNO3. loãng , đun nóng và khuấy đều . Sau khi p /ứ xảy ra hoàn toàn thu đc 1.8 lít khí NO ( sản phẩm khử duy nhất , ở đktc ) dd Y và còn lại 1,2 g kim loại
a) viết phương trình phản ứng xảy ra ?
b) tính nồng độ mol của axit HNO3 ?
Tính theo PTHH, lượng dư, Nồng độ dung dịch?
cho 11,2g sắt tác dụng với 400ml dung dịch HCL
a, Tính thể tích H2 sinh ra ở đktc?
b, Tính nồng độ mol của dung dịch HCL đã dùng ?
c, Nếu dùng lượng H2 của phản ứng trên khử 8g CuO ở nhiệt độ cao. Hỏi thu đc bao nhiêu gam Fe
Trả Lời
nFe=11.2\56=0.2(o)nFe=11.2\56=0.2(mol)
+
0.2.......0.4...................0.2
VH2=0.2⋅22.4=4.48(l)VH2=0.2⋅22.4=4.48(l)
CMHCl=0.4\0.4=1(M)CMHCl=0.4\0.4=1(M)
nCuO=8\80=0.1(mol)nCuO=8\80=0.1(mol)
CuO+H2t0→Cu+H2OCuO+H2t0→Cu+H2O
1............11............1
0.1.........0.20.1.........0.2
LTL:0.11<0.21⇒H2dưLTL:0.11<0.21⇒H2dư
nCu=nCuO=0.1(mol)nCu=nCuO=0.1(mol)
mCu=0.1⋅64=6.4(g)
CHO HỎi
NFe = 11.2\56 = 0,2 mol thì 56 lấy đâu ra ạ
56 là nguyên tử khối cùa Fe nhé , em có thể xem lại trong bảng.