Cho H2 khử 16g hỗn hợp gồm Fe2O3 và CuO trong đó mCuO chiếm 25%
a)Tính mFe và mCu sau pứ
b)Tính VH2 đã tham gia pứ
Cho H2 khử 16g hỗn hợp gồm Fe2O3 và CuO trong đó mCuO chiếm 25%
a)Tính mFe và mCu sau pứ
b)Tính VH2 đã tham gia pứ
Cho 1 hỗn hợp gồm 75% Fe(III) oxit và 25% Cu(II) Oxit . Người ta dùng H2 để khử 16g hỗn hợp đó
a)Tính mFe và mCu sau pứ
b)Tính VH2 đã pứ
mFe2O3=16.75%=12(g)
mCuO=16-12=4(g)
Fe2O3 + 3H2 -> 2Fe + 3H2O (1)
CuO + H2 -> Cu + H2O (2)
nFe2O3=\(\dfrac{12}{160}=0,075\left(mol\right)\)
nCuO=\(\dfrac{4}{80}=0,05\left(mol\right)\)
Theo PTHH 1 và 2 ta có:
3nFe2O3=nH2=0,225(mol)
nCuO=nH2=0,05(mol)
VH2=22,4.0,275=6,16(lít)
Cho H 2 khử 16g hỗm hợp FeO và CuO trong đó CuO chiếm 25% khối lượng. Tính tổng thể tích khí H 2 (đktc) đã tham gia phản ứng.
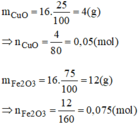
Từ pt (1), n H 2 = n C u = 0,05 mol,
Từ pt (2), n H 2 = 3 . n F e 2 O 3 = 3. 0,075 = 0,225 mol
Tổng thể tích khí H 2 tham gia phản ứng:
V H 2 =(0,05 + ,225).22,4 = 6,16(lit)
có 40g hỗn hợp gồm 40% Fe2O3 và 60% CuO người ta dùng h2 ( dư) để khử hỗn hợp đó . a, Tính klg Fe và Cu thu đc sau phản ứng b, Tính số mol H2 đã tham gia phản ứng
Người ta dùng H2 (dư) để khử 16g hỗn hợp gồm 75% Fe2O3 và 25% CuO.
a. Tính khối lượng Fe và khối lượng Cu thu được sau phản ứng
b. Tính số mol H2 đã tham gia phản ứng.
\(m_{Fe_2O_3}=16\cdot75\%=12\left(g\right)\)
\(n_{Fe_2O_3}=\dfrac{12}{160}=0.075\left(mol\right)\)
\(n_{CuO}=16\cdot25\%=4\left(g\right)\)
\(n_{CuO}=\dfrac{4}{80}=0.05\left(mol\right)\)
\(Fe_2O_3+3H_2\underrightarrow{^{^{t^0}}}2Fe+3H_2O\)
\(CuO+H_2\underrightarrow{^{^{t^0}}}Cu+H_2O\)
\(n_{H_2}=3\cdot0.075+0.05=0.275\left(mol\right)\)
a,\(m_{Fe_2O_3}=16.75\%=12\left(g\right)\Rightarrow n_{Fe_2O_3}=\dfrac{12}{160}=0,075\left(mol\right)\)
\(m_{CuO}=16-12=4\left(g\right)\Rightarrow n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)\)
PTHH: Fe2O3 + 3H2 → 2Fe + 3H2O
Mol: 0,075 0,225 0,15
PTHH: CuO + H2 → Cu + H2O
Mol: 0,05 0,05 0,05
\(\Rightarrow m_{Fe}=0,15.56=8,4\left(g\right);m_{Cu}=0,05.64=3,2\left(g\right)\)
b,\(n_{H_2}=0,225+0,05=0,275\left(mol\right)\)
\(a) n_{Fe_2O_3} = \dfrac{16.75\%}{160} = 0,075(mol)\\ n_{CuO} = \dfrac{16.25\%}{80} = 0,05(mol)\\ Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O\\ CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ n_{Fe} = 2n_{Fe_2O_3} = 0,15(mol) \Rightarrow m_{Fe} = 0,15.56 = 8,4(gam)\\ n_{Cu} = n_{CuO} = 0,05(mol) \Rightarrow m_{Cu} = 0,05.64 = 3,2(gam)\\ b) n_{H_2} = 3n_{Fe_2O_3} + n_{CuO} = 0,075.3 + 0,05 = 0,275(mol)\\ V_{H_2} = 0,275.22,4 = 6,16(lít)\)
Hỗn hợp gồm 60% Fe2O3 va 40 % CuO . Người ta dùng H2 để khử 20g hỗn hợp đó.
a) Tính mFe và mCu thu được ?
b) tính \(V_{H_2}\) tham gia phản ứng .
PTHH
Fe2O3 + 3H2 -> 2Fe + 3H2O
0.075 0.225 mol
CuO + H2 -> Cu + H2O
0.1 0.1 mol
a) mFe2O3 = 20*60%=12g
mCuO = 20 - 12 = 8g
b) nFe2O3 = 12/160 = 0.075mol
nCuO = 8/80 = 0.1 mol
VH2 = (0.225+0.1)*22.4 = 7.28 lit
giúp em câu này với ạ,em đang cần gấp.em cảm ơn.
dùng hidro khử hoàn toàn 40g hỗn hợp gồm Fe2O3 và CuO,trong hỗn hợp tỉ lệ khối lượng Fe2O3 và CuO là 3:2. Tính khối lượng Fe và Cu thu được sau pứ
\(Tacó:m_{Fe_2O_3}:m_{CuO}=3:2\\ m_{Fe_2O_3}+m_{CuO}=40\\ \Rightarrow m_{Fe_2O_3}=24\left(g\right)\Rightarrow n_{Fe_2O_3}=0,15\left(mol\right)\\ \Rightarrow m_{CuO}=16\left(g\right)\Rightarrow n_{CuO}=0,2\left(mol\right)\\ Fe_2O_3+3H_2-^{t^o}\rightarrow2Fe+3H_2O\left(1\right)\\ CuO+H_2O-^{t^o}\rightarrow Cu+H_2O\left(2\right)\\TheoPT\left(1\right): n_{Fe}=2n_{Fe_2O_3}=0,3\left(mol\right)\\ \Rightarrow m_{Fe}=16,8\left(g\right)\\TheoPT\left(2\right): n_{Cu}=n_{CuO}=0,2\left(mol\right)\\ \Rightarrow m_{Cu}=0,2.64=12,8\left(g\right)\)
Có một hỗn hợp gồm 60% F e 2 O 3 và 40% CuO. Người ta dùng H 2 ( dư) để khử 20g hỗn hợp đó. Tính số mol H 2 tham gia phản ứng.