Cho 10g CuO tác dụng hoàn toàn với dd 500ml dd (axit clohidric) HCl dư. Tính nồng độ dd CuCl2 tạo thành?

Những câu hỏi liên quan
̣Cho 10g MgO tác dụng hoàn toàn với dd 500ml dd (axit clohidric) HCl dư.
a. Tính nồng độ mol dd axit
b. Tính nồng độ mol dd MgCl 2
mong moi nguoi giup em
PTHH: \(MgO+2HCl\rightarrow MgCl_2+H_2O\)
Ta có: \(n_{MgO}=\dfrac{10}{40}=0,25\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,5\left(mol\right)\\n_{MgCl_2}=0,25\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{HCl}}=\dfrac{0,5}{0,5}=1\left(M\right)\\C_{M_{MgCl_2}}=\dfrac{0,25}{0,5}=0,5\left(M\right)\end{matrix}\right.\)
Đúng 4
Bình luận (1)
Ta có: nMgO = \(\dfrac{10}{40}=0,25\left(mol\right)\)
a. PTHH: MgO + 2HCl ---> MgCl2 + H2O
Theo PT: nHCl = 2.nMgO = 2.0,25 = 0,5(mol)
Đổi 500ml = 0,5 lít
=> \(C_{M_{HCl}}=\dfrac{0,25}{0,5}=0,5M\)
b. Ta có: \(V_{dd_{MgCl_2}}=10+0,5=10,5\left(lít\right)\)
Theo PT: \(n_{MgCl_2}=n_{MgO}=0,25\left(mol\right)\)
=> \(C_{M_{MgCl_2}}=\dfrac{0,25}{10,5}=0,024M\)
Đúng 1
Bình luận (3)
1. K2O + SO2 ---> K2SO3.
2. K2O + N2O5 ---> 2KNO3.
3. K2O + CO2 ---> K2CO3.
4. BaO + SO2 ---> BaSO3.
5. BaO + N2O5 ---> N2O + BaO5.
6. BaO + CO2 ---> BaCO3.
7. CuO + CO2 ---> CuCO3.
Đúng 1
Bình luận (1)
Xem thêm câu trả lời
1.cho dd chua 100 ml dd AgNO3 1M tac dung hoan toan voi 200 ml dd NaCl 1M a. Tinh khôi lượng kết tủa tạo thànhb. Tinh nồng độ mol/lit cua các chất trong dd tạo thành.2, cho 2.74 g Ba hoa tan hoan toan vao H2O tao thanh dd X .a. Tinh khoi luong H2 tao thanhb. Cho dd X pứ voi dd H2SO4 dư. Tinh so gam ket tủa tao thanh.3, Cho m gam (sắt ôxit) FeO tác dụng hết với 600ml dd HCl (axit clohidric) đặc tạo thành dd (sắt clorua) FeCl2 0,2M. Tính m?
Đọc tiếp
1.cho dd chua 100 ml dd AgNO3 1M tac dung hoan toan voi 200 ml dd NaCl 1M
a. Tinh khôi lượng kết tủa tạo thành
b. Tinh nồng độ mol/lit cua các chất trong dd tạo thành.
2, cho 2.74 g Ba hoa tan hoan toan vao H2O tao thanh dd X .
a. Tinh khoi luong H2 tao thanh
b. Cho dd X pứ voi dd H2SO4 dư. Tinh so gam ket tủa tao thanh.
3, Cho m gam (sắt ôxit) FeO tác dụng hết với 600ml dd HCl (axit clohidric) đặc tạo thành dd (sắt clorua) FeCl2 0,2M. Tính m?
cho 43,5gam MnO2 tác dụng hết với 250gam dd HCl thu được khí A. dẫn khí A qua 400ml dd NaOH 5M thu được dd B
a) tính nồng độ mol các muối trong dd B
b) Tính C% của dd HCl ban đầu (dùng dư 10% so với phản ứng)
MnO2+4HCl->MnCl2+H2O+Cl2
0,5---------2------0,5--------0,5---0,5
Cl2+2NaOH->NaClO+NaCl+H2O
0,5-----1--------0,5----------0,5------0,5
n MnO2 =\(\dfrac{43.5}{87}\)=0,5 mol
n NaOH=5.0,4=2 mol
=>NaOH dư :0,1 mol
=>CM NaCl= CM NaClO =\(\dfrac{1}{0,4}\)=2,5M
=>CM NaOH dư =1\(\dfrac{1}{0,4}\)=2,5M
b)
C%HCl =\(\dfrac{2.36,5}{250}100\)=29,2%
dùng dư 10%
=>C%HCl=29,2+10=39,2%
Đúng 0
Bình luận (2)
Cho m gam (sắt ôxit) FeO tác dụng hết với 600ml dd HCl (axit clohidric) đặc tạo thành dd (sắt clorua) FeCl2 0,2M. Tính m?
Nồng độ FeCl2: CM=0,2M thể tích dd: Vdd = 600ml = 0,6lit
 Vậy số mol FeCl2
Vậy số mol FeCl2 
Pt:

 khối lượng
khối lượng
Vậy m là 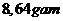
Đúng 0
Bình luận (0)
Cho 10g dd muối sắt clorua 32,5% tác dụng với dd AgNO3 tạo thành 8,61g kết tủa.Tìm CTHH của muối sắt đã dùng.
Gọi x là hóa trị của sắt
\(m_{FeCl_x}=\dfrac{10\cdot32,5\%}{100\%}=3,25\left(g\right)\\ n_{AgCl}=\dfrac{8,61}{143,5}=0,06\left(mol\right)\\ PTHH:FeCl_x+AgNO_3\rightarrow Fe\left(NO_3\right)_x+xAgCl\)
Theo PTHH: \(n_{FeCl_x}=\dfrac{n_{AgCl}}{x}=\dfrac{0,06}{x}\left(mol\right)\)
\(\Rightarrow M_{FeCl_x}=\dfrac{3,25}{\dfrac{0,06}{x}}=54x\\ \Rightarrow56+35,5x=54x\\ \Rightarrow x=3\)
Vậy CTHH cần tìm là \(FeCl_3\)
Đúng 2
Bình luận (0)
cho 6,5g Zn tác dụng với 500ml dd HCL nồng độ 1M
a, tính thể tích khí h2 thoát ra ở đktc
b, Tính khối lượng muối tạo thành
c, tính nồng độ mol các chất trong dd
nZn=6,5/65=0,1mol
đổi 500ml = 0,5l
nHCl = 0,5.1 =0,5mol
pt : Zn + 2HCl ------> ZnCl2 + H2
n có: 0,1 0,5
n pứ: 0,1 ----->0,2----------->0,1-------->0,1
n dư: 0 0,3
VH2= 0,1.22.4 =2,24l
mZnCl2= 0,1.136=13,6g
Vdd sau pứ =VddHCl =0,5l
CM(HCl dư) = 0,3/0,5=0,6M
CM(ZnCl2) = 0,1/0,5 =0,2M
Đúng 0
Bình luận (0)
a)
nZn = \(\dfrac{6,5}{65}=0,1mol\)
500ml = 0,5 (l)
Ta có: CM = \(\dfrac{n}{V}=\dfrac{n}{0,5}=1\Rightarrow n_{HCl}=0,5mol\)
Zn + 2HCl -----> ZnCl2 + H2
0,1 0,5
Xét: \(\dfrac{0,1}{1}< \dfrac{0,5}{2}\Rightarrow\) Zn hết, HCl dư
\(\Rightarrow\) \(n_{H_2}=0,1mol\) \(\Rightarrow V_{H_2}=0,1.22,4=2,24l\)
b) \(n_{ZnCl_2}=0,1mol\)
\(\Rightarrow\)\(m_{ZnCl_2}=0,1.136=13,6g\)
c) CM = \(\dfrac{n_{ZnCl_2}}{V}\) = \(\dfrac{0,1}{0,5}\)= 0,2M
nHCl dư = 0,5 - 0,2 = 0,3 mol
CM = \(\dfrac{n_{HCL}}{V}\) = \(\dfrac{0,3}{0,5}\) = 0,6M
Đúng 0
Bình luận (0)
1. Trộn 800ml dung dịch H2SO4 nồng độ M với 200 ml dung dịch H2SO4 nồng độ 1.5 M, thu được dung dịch mới có nồng độ 0,5M. Tính nồng độ M
2. Hòa tan 20,4g kim lọai hóa trị 3 cần vừa đủ a gam dung dịch HCl 20%. Sau phản ứng thu được dung dịch chứa 53,4g muối
a,Xác định công thức hóa học của oxit
b,Tính a?
c,tính nồng độ phần trăm của muối sau phản ứng
3. Đốt cháy 9.76 g hỗn hợp X gồm cu và Fe trong O2 dư thu được 12.64 hỗn hợp chất rắn Y. Htht Y trong dung dịch HCl dư dung dịch A. Thêm dung dịc...
Đọc tiếp
1. Trộn 800ml dung dịch H2SO4 nồng độ M với 200 ml dung dịch H2SO4 nồng độ 1.5 M, thu được dung dịch mới có nồng độ 0,5M. Tính nồng độ M
2. Hòa tan 20,4g kim lọai hóa trị 3 cần vừa đủ a gam dung dịch HCl 20%. Sau phản ứng thu được dung dịch chứa 53,4g muối
a,Xác định công thức hóa học của oxit
b,Tính a?
c,tính nồng độ phần trăm của muối sau phản ứng
3. Đốt cháy 9.76 g hỗn hợp X gồm cu và Fe trong O2 dư thu được 12.64 hỗn hợp chất rắn Y. Htht Y trong dung dịch HCl dư =>dung dịch A. Thêm dung dịch NaOH dư vào dd A thu được kết tủa B. Tính m B
4. Làm lạnh m gam một dung dịch bão hòa KNO3 từ 40 độ C xuống 10 độ C thì thấy có 118,2 gam KNO3 khan tách ra khỏi dung dịch. Biết độ tan của KNO3 ở 10 độ C và 40 độ C lần lượt là 21,9 gam và 61,3 gam. Tính m
5. Làm lạnh 805 gam dung dịch bão hòa MgCl2 từ 60 độ C xuống còn 10 độ C thì có bao nhiêu gam tinh thể MgCl2.6H2O tách ra khỏi dung dịch. Biết rằng độ tan của MgCl2 trong nước ở 10 độ C và 60 độ C lần lượt là 52,9 gam và 61 gam
6. Cho 1,2 gam Mg tác dụng hoàn toàn với dd AgNO3 dư. Tính khối lượng Ag sinh ra.
7. Cho dd chứa 4,25 gam AgNO3 tác dụng hoàn toàn với NaCl dư. Tính khối lượng kết tủa tạo thành.
8. Cho m gam kim loại Ca tác dụng với H2O dư sinh ra 0,03gam khí H2. tính m?
9. Cho m gam Na2O tác dụng hoàn toàn với dd H2SO4 dư, sau pứ cô cạn dd thu được2,84 gam muối khan, tính m.
10. Cho 2,74 gam Ba hòa tan hoàn toàn vào H2O tạo thành dd X.
a. Tính khối lượng H2 tạo thành.
b. Cho dd X pứ với dd H2SO4 dư. Tính số gam kết tủa tạo thành.
Cho 400 g dd NaOH 30% tác dụng vừa hết với 100 g dd HCl , tính:
a) nồng độ % muối thu dc sau phản ứng .
b) tính nồng độ % axit HCl . Biết phản ứng xảy ra hoàn toàn ?
ta có mNaOH= 400. 30%= 120( g)
\(\rightarrow\) nNaOH= 120/ 40= 3(mol)
PTPU
NaOH+ HCl\(\rightarrow\) NaCl+ H2O
3.............3..........3............
a) ta có mNaCl= 3. 58,5= 175,5( g)
mdd NaCl= 400+ 100= 500( g)
\(\Rightarrow\) C%NaCl= \(\dfrac{175,5}{500}\). 100%=35,1%
Đúng 0
Bình luận (0)
1/ Cho 100ml dd NaOH 0,2M tác dụng với 250ml dd H2SO4 1M được dd A. Cho dd A tác dụng với dd BaCl2 12% .Hãy tính khối lượng kết tủa tạo thành và khối lượng dd BaCl2 càn dùng2/Đổ từ từ 200ml dd H2SO4 4,5M vào để trung hòa 400ml dd NaOH 3M. Tính:a)khối lượng mỗi muối thu được sau phản ứngb) để tác dụng hết với dd thu được sau phản ứng đó cần dùng bao nhiêu ml dd BaCl2 2M
Đọc tiếp
1/ Cho 100ml dd NaOH 0,2M tác dụng với 250ml dd H2SO4 1M được dd A. Cho dd A tác dụng với dd BaCl2 12% .Hãy tính khối lượng kết tủa tạo thành và khối lượng dd BaCl2 càn dùng
2/Đổ từ từ 200ml dd H2SO4 4,5M vào để trung hòa 400ml dd NaOH 3M. Tính:
a)khối lượng mỗi muối thu được sau phản ứng
b) để tác dụng hết với dd thu được sau phản ứng đó cần dùng bao nhiêu ml dd BaCl2 2M
Mấy bài này viết PTHH rồi tìm chất nào dư chất nào hết thôi nhé!
Đúng 0
Bình luận (1)
1.\(n_{NaOH}=0,1.0,2=0,02\left(mol\right)\)
\(n_{H_2SO_4}=0,25.1=0,25\left(mol\right)\)
2NaOH + H2SO4 → Na2SO4 + 2H2O
Lập tỉ lệ NaOH và H2SO4 : \(\dfrac{0,02}{2}< \dfrac{0,25}{1}\)
=> H2SO4 dư, NaOH hết
Na2SO4 + BaCl2 → BaSO4 + 2NaCl
H2SO4 + BaCl2 → BaSO4 + 2HCl
\(n_{Na_2SO_4}=\dfrac{1}{2}n_{NaOH}=0,01\left(mol\right)\)
\(n_{H_2SO_4\left(dư\right)}=0,25-0,01=0,24\left(mol\right)\)
=> \(n_{BaSO_4}=0,01+0,24=0,25\left(mol\right)\)
=> \(m_{BaSO_4}=0,25.233=58,25\left(g\right)\)
=> \(m_{ddBaCl_2}=\dfrac{\left(0,01+0,24\right).208}{12\%}=433,33\left(g\right)\)
Đúng 1
Bình luận (0)























