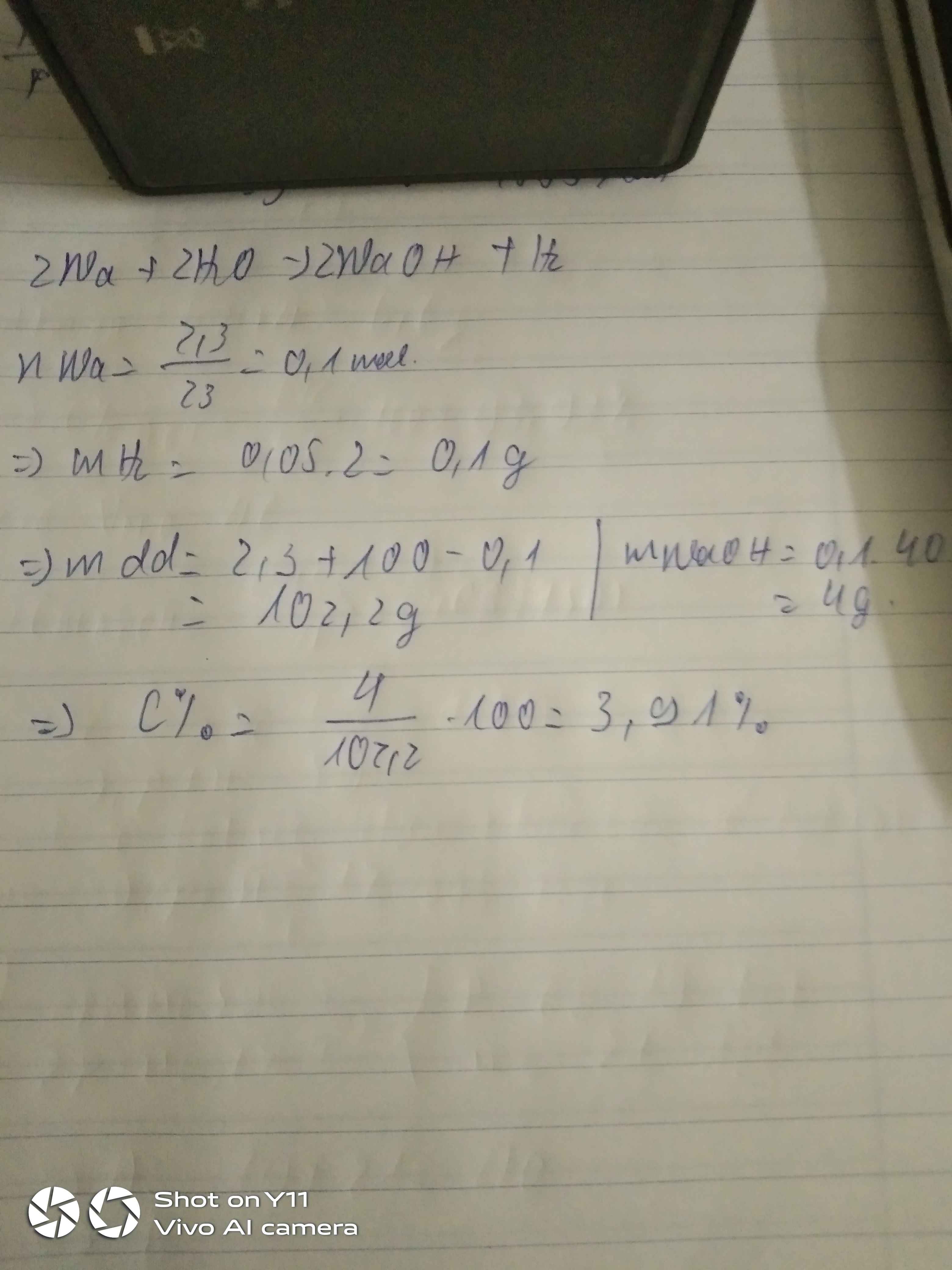Cho 2,3g Na phản ứng hoàn toàn với 197,7g nước dung dịch A .Tính nồng độ phần trăm của dung dịch A.

Những câu hỏi liên quan
cho 2,3g Na tác dụng với 197,8g nước. tính thể tích khí hidro sinh ra ở đktc tính nồng độ phần trăm của dung dịch sau phản ứng tính nồng độ mol/lít của dung dịch thu được. cho khối rượn riêng của dung dịch D=1,08g/mol
\(n_{Na}=\dfrac{2,3}{23}=0,1\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2
0,1-------------->0,1---->0,05
=> VH2 = 0,05.22,4 = 1,12 (l)
mdd sau pư = 2,3 + 197,8 - 0,05.2 = 200 (g)
=> \(C\%=\dfrac{0,1.40}{200}.100\%=2\%\)
\(V_{dd}=\dfrac{200}{1,08}=\dfrac{5000}{27}\left(ml\right)=\dfrac{5}{27}\left(l\right)\)
=> \(C_M=\dfrac{0,1}{\dfrac{5}{27}}=0,54M\)
Đúng 1
Bình luận (0)
cho 2,3g Na tác dụng với 197,8g nước.
tính thể tích khí hidro sinh ra ở đktc
tính nồng độ phần trăm của dung dịch sau phản ứng
tính nồng độ mol/lít của dung dịch thu được. cho khối rượn riêng của dung dịch D=1,08g/mol
Cho 4,6g Na vào 90g nước lấy dư,sau phản ứng hoàn toàn,viết phương trình hóa học của phản ứng và tính nồng độ phần trăm C% của dung dịch thu đc
\(n_{Na}=\frac{4,6}{23}=0,2\left(mol\right)\)
\(2Na+2H_2O->2NaOH+H_2\) (1)
theo (1) \(n_{NaOH}=n_{Na}=0,2\left(m0l\right)\)
=> \(m_{NaOH}=0,2.40=8\left(g\right)\)
theo (1) \(n_{H_2}=\frac{1}{2}n_{Na}=0,1\left(mol\right)\)
khối lượng dung dịch sau phản ứng là
4,6 + 90 - 0,1.2=94,4(g)
nồng độ % dung dịch thu được là
\(\frac{8}{94,4}.100\%\approx8,47\%\)
Đúng 0
Bình luận (0)
Na+H20-> NaOH + 1/2 H2
C%= mNaOH / mNa mH20 - mH2 nhân cho 100
Đúng 0
Bình luận (0)
Cho 44,8(l) khí HCl (đktc) hòa tan vào 327 gam nước được dung dịch A
a) Tính nồng độ phần trăm của dung dịch A
b) Cho 50 gam CaCO3 vào 250 gam dung dịch A, đun nhẹ đến khi phản ứng xảy ra hoàn toàn được dung dịch B. Tính nồng độ % các chất có trong dung dịch B
\(n_{HCl}=\dfrac{44,8}{22,4}=2\)
\(\Rightarrow m_{HCl}=2.36,5=73g\)
=> \(C\%_{HCl}=\dfrac{73}{73+327}\times100\%=18,25\%\)
b.
\(n_{HCl}=\dfrac{250.18,25\%}{36,5}=1,25mol\)
\(n_{CaCO_3}=\dfrac{50}{100}=0,5mol\)
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
\(n_{CaCl_2}=n_{CO_2}=0,5mol\)
\(n_{HClpu}=0,5.2=1mol\)
\(\Rightarrow n_{HCldu}=1,25-1=0,25\)
\(\Rightarrow m_{ddpu}=50+250-0,5.44=278g\)
\(C\%_{HCl}=\dfrac{0,25.36,5}{278}.100\%=3,28\%\)
\(C\%_{CaCl_2}=\dfrac{0,5.111}{278}.100\%=19,96\%\)
Đúng 3
Bình luận (0)
cho 2,3g Na vào 100g nước tính nồng độ phần trăm dung dịch thu được
\(n_{Na}=\dfrac{2,3}{23}=0,1\left(mol\right)\)
Pt : \(2Na+2H_2O\rightarrow2NaOH+H_2|\)
2 2 2 1
0,2 0,2
\(n_{NaOH}=\dfrac{0,2.2}{2}=0,2\left(mol\right)\)
⇒ \(m_{NaOH}=0,2.40=8\left(g\right)\)
\(m_{ddspu}=2,3+100=102,3\left(g\right)\)
\(C_{ddNaOH}=\dfrac{8.100}{102,3}=7,82\)0/0
Chúc bạn học tốt
Đúng 0
Bình luận (1)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(n_{H_2}=\dfrac{1}{2}n_{Na}=\dfrac{1}{2}.\dfrac{2,3}{23}=0,05\left(mol\right)\)
\(\Rightarrow m_{H_2}=0,05.2=0,1\left(g\right)\)
\(\Rightarrow m_{\text{dd sau pư}}=100+2,3-0,1=102,2\left(g\right)\)
\(n_{NaOH}=n_{Na}=0,1\left(mol\right)\)
\(\Rightarrow C\%=\dfrac{0,1.40}{102,2}.100\%=3,91\%\)
Đúng 0
Bình luận (0)
Cho 11,28g K2O phản ứng hoàn toàn với 100g nước. Tính nồng độ phần trăm dung dịch thu được.
\(n_{K_2O}=\dfrac{11,28}{94}=0,12\left(mol\right)\)
PTHH :
\(K_2O+H_2O\rightarrow2KOH\)
0,12 0,24
\(m_{KOH}=0,24.56=13,44\left(g\right)\)
\(m_{ddKOH}=11,28+100=111,28\left(g\right)\)
\(C\%=\dfrac{13,44}{111,28}.100\%\approx12,08\%\)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 4g NaOH có nồng độ 10% vào dung dịch CuCl2 có nồng độ 10% a) viết PTHH xảy ra b) Tính khối lượng dung dịch CuCl2 đã dùng c) tính nồng độ phần trăm (c%) của chất trong dung dịch sau phản ứng (Biệt Cu = 64 ; O = 16 ; Na = 23 ; Cl = 35,5 ; H=1)
\(a)2NaOH+CuCl_2\rightarrow Cu\left(OH\right)_2+2NaCl\\ b)n_{NaOH}=\dfrac{4}{40}=0,1mol\\ n_{CuCl_2}=n_{Cu\left(OH\right)_2}=0,1:2=0,05mol\\ m_{ddCuCl_2}=\dfrac{0,05.135}{10}\cdot100=67,5g\\ c)n_{NaCl}=n_{NaOH}=0,1mol\\ C_{\%NaCl}=\dfrac{0,1.58,5}{\dfrac{4}{10}\cdot100+67,5-0,05.98}\cdot100=14,0625\%\)
Đúng 1
Bình luận (0)
cho 200 gam dung dịch NaOH 20% tác dụng vừa hết với 100 g dung dịch HCl. Tính nồng độ phần trăm dung dịch muối sau phản ứng, tính nòng độ phần trăm dung dịch axit HCl đã dùng.Biết phản ứng xảy ra hoàn toàn
Cho 2,7 g nhôm tác dụng hoàn toàn hết với 441 gam dung dịch axit sunfuric sau phản ứng thu được dung dịch muối nhôm sunfat a viết phương trình phản ứng b tính nồng độ phần trăm của dung dịch axit C tính thể tích của dung dịch muối
a) $2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
b)
n Al = 2,7/27 = 0,1(mol)
Theo PTHH :
n H2SO4 = 3/2 n Al = 0,15(mol)
=> C% H2SO4 = 0,15.98/441 .100% = 3,33%
c)
Theo PTHH :
n H2 = 3/2 n Al = 0,15(mol)
=> V H2 = 0,15.22,4 = 3,36(lít)
Đúng 1
Bình luận (0)