Cho 6,5 g kẽm vào bình dung dịch chứa 0,25 mol axit clohiđric.
a/ Tính thể tích khí hiđro thu được ở đktc?
b. Sau phản ứng còn dư chất nào ? khối lượng là bao nhiêu gam?
cho 6,5 kẽm vào bình dung dịch chứa 0,25 mol axit clohidric .
a/ tính thể tích khí hidro thu được ở đktc
b/ sau phản ứng còn dư chất nào ? khối lượng là bao nhiêu gam
zn+2Hcl→zncl2+h2
a) nZn=6.5/65=0.1(mol)
ta có nZn/1=0.1/1<nHcl/2=0.25/2=0.125
→zn hết ,hcl dư
theo pt:nH2=nZn=0.1 (mol)
Vh2=0.1*22.4=2.24
b) sau pư zn hết ,Hcl dư
theo pt nHcl=2nZn=0.1*2=0.2( mol )
sô mol Hcl dư là:
0.25-0.2=0.05(mol)
mHcl dư là:0.05*36.5=1.825
xong ![]()
cho 6,5 g kẽm vào bình dung dịch chứa 0,25 mol axit HCl
a) tính thể tích khí Hidro thu được ở đktc
b) sau phản ứng nào còn dư ? dư bao nhiêu gam
Cho 13 gam kẽm vào bình đựng dung dịch axit clohiđric dư. a, Tính thể tích khí hiđrô thu được ở đktc. b, Cho toàn bộ khí hiđro thu được đi qua 6,4 gam Fe2O3 đang nung nóng . Hỏi - Chất nào còn dư sau phản ứng ? khối lượng dư là bao nhiêu? - Tính khối lượng sắt thu được sau phản ứng. ( Biết khối lượng mol của Zn= 65, Cl = 35,5, O = 16, Fe = 56)
a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, \(n_{Fe_2O_3}=\dfrac{6,4}{160}=0,04\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Xét tỉ lệ: \(\dfrac{0,04}{1}< \dfrac{0,2}{3}\), ta được H2 dư.
Theo PT: \(n_{H_2\left(pư\right)}=3n_{Fe_2O_3}=0,12\left(mol\right)\Rightarrow n_{H_2\left(dư\right)}=0,2-0,12=0,08\left(mol\right)\)
\(\Rightarrow m_{H_2\left(dư\right)}=0,08.2=0,16\left(g\right)\)
Theo PT: \(n_{Fe}=2n_{Fe_2O_3}=0,08\left(mol\right)\Rightarrow m_{Fe}=0,08.56=4,48\left(g\right)\)
3. Cho 19,5 gam kẽm tác dụng với dung dịch có chứa 14,6 gam axit HCl tạo sản phẩm là ZnCl2 và khí hiđro. a/ Sau phản ứng, chất nào còn dư và dư bao nhiêu gam? b/ Tính thể tích khí hiđro (đktc) thu được và khối lượng muối kẽm tạo thành? c/ Người ta dùng khí hiđro thu được ở trên để khử Fe3O4 thu được sắt kim loại và nước. Tính số gam sắt thu được?
Số mol của kẽm
nZn = \(\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
Số mol của axit clohidric
nHCl = \(\dfrac{m_{HCl}}{M_{HCl}}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
Pt : Zn + 2HCl → ZnCl2 + H2\(|\)
1 2 1 1
0,3 0,4 0,2 0,2
a) Lập tỉ số só sánh : \(\dfrac{0,3}{1}>\dfrac{0,4}{2}\)
⇒ Zn dư , HCl phản ứng hết
⇒ Tính toán dựa vào số mol của HCl
Số mol dư của kẽm
ndư = nban đầu - nmol
= 0,3 - (\(\dfrac{0,4.1}{2}\))
= 0,1 (mol)
Khối lượng dư của kẽm
mdư = ndư . MZn
= 0,1 . 65
= 6,5 (g)
b) Số mol của khí hidro
nH2 = \(\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
Thể tích của khí hidro ở dktc
VH2 = nH2 . 22,4
= 0,2 . 22,4
= 4,48 (l)
Số mol của muối kẽm clorua
nZnCl2 = \(\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
Khối lượng của muối kẽm clorua
mznCl2 = nZnCl2 . MZnCl2
= 0,2. 136
= 27,2 (g)
c) 4H2 + Fe3O4 → (to) 3Fe + 4H2O\(|\)
4 1 3 4
0,2 0,15
Số mol của sắt
nFe = \(\dfrac{0,2.3}{4}=0,15\left(mol\right)\)
Khối lượng của sắt
mFe = nFe. MFe
= 0,15 . 56
= 8,4 (g)
Chúc bạn học tốt
Cho 6,5 g kẽm(Zn) vào bình dung dịch axit clohiđric(HCl).
a. Tính thể tích khí hiđro (ở đktc) được tạo thành trong phản ứng trên.
b. Nếu dẫn toàn bộ khí Hidro ở phản ứng trên đem khử bột 12g CuO ở nhiệu độ cao thì chất nào còn dư? Dư bao nhiêu gam?
a)\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
b)\(n_{CuO}=\dfrac{12}{80}=0,15mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,15 0,1 0 0
0,1 0,1 0,1 0,1
0,05 0 0,1 0,1
\(CuO\) dư và dư 0,05mol
\(\Rightarrow m_{CuOdư}=0,05\cdot80=4g\)
a.\(n_{Zn}=\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,1 ( mol )
\(V_{H_2}=n_{H_2}.22,4=0,1.22,4=2,24l\)
b.\(n_{CuO}=\dfrac{m_{CuO}}{M_{CuO}}=\dfrac{12}{80}=0,15mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,15 < 0,1 ( mol )
Chất còn dư là \(CuO\)
\(m_{CuO\left(du\right)}=n_{CuO\left(du\right)}.M_{CuO}=\left(0,15-0,1\right).80=4g\)
a)nZn=6,5/65=0,1 mol
PTHH:Zn+HCl➜ZnCl2+H2
Theo PT trên ta thấy:nZn=nH2=0,1 mol
➩VH2=0,1 nhân 22,4=2,24l
b)nCuO=12/80=0,15 mol
PTHH:H2+CuO➝Cu+H2O
xét tỉ lệ:0,1/1<0,15/1
➙H2 hết CuO dư
Theo PT:nH2=nCuO pư=0,1 mol
⇒nCuO dư=0,15-0,1=0,05 mol
⇒mCuO dư=0,05 nhân 80=4 gam
Cho 2,6 g kẽm vào dung dịch Có chứ 0,5 mol axit clohiđric
a) chất nào còn sau phản ứng ? Có khối lượng là bao nhiêu
b) tính thể tích khí Hiđro thu được
Cho 19,5 gam kẽm vào dung dịch có 18,25 gam axit clohiđric.
a) Viết phương trình hóa học phản ứng xảy ra.
b) Khi phản ứng kết thúc, chất nào còn dư và dư bao nhiêu gam?
c) Tính thể tích chất khí sinh ra sau phản ứng (ở đktc).
(H = 1 ; Cl = 35,5 ; Zn = 65)
nZn=19,5/65=0,3(mol)
mHCl=18,25/36,5=0,5(mol)
pt: Zn+2HCl--->ZnCl2+H2
1______2
0,3_____0,5
Ta có: 0,3/1>0,5/2
=>Zn dư
mZn dư=0,05.65=3,25(mol)
Theo pt: nH2=1/2nHCl=1/2.0,5=0,25(mol)
=>VH2=0,25.22,4=5,6(l)
nZn = 0,3 mol
nHCl = 0,5 mol
Zn + 2HCl → ZnCl2 + H2
Đặt tỉ lệ ta có
0,3 < \(\dfrac{0,52}{2}\)
⇒ Zn dư và dư 3,25 gam
⇒ VH2 = 0,25.22,4 = 5,6 (l)
cho 2,5 gam nhôm vào bình chứa 0,25 mol dung dịch axit sunfuric loãng a,Viết phương trình phản ứng b,chất nào còn dư sau phản ứng Tính khối lượng chất dư c,Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn
a: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b: \(n_{Al}=\dfrac{2.5}{27}< \dfrac{1}{4}\)
=>H2SO4 dư, Al đủ
\(m_{H_2SO_4}=0.25\cdot98=24.5\left(g\right)\)
c: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{2.5}{54}=\dfrac{5}{108}\left(mol\right)\)
\(\Leftrightarrow n_{H_2}=\dfrac{5}{36}\left(mol\right)\)
\(V_{H_2}=\dfrac{5}{36}\cdot22.4=\dfrac{28}{9}\left(lít\right)\)
Mình thấy bạn Thịnh tính lượng dư sai
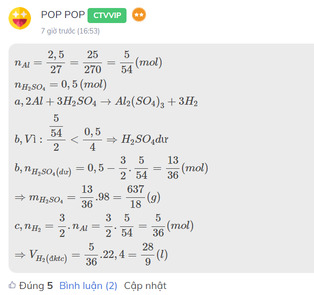
Đây là bài mình từng làm, bạn tham khảo nhé!
Cho 0,15 mol kẽm phản ứng với dung dịch có 9,125 gam axit
Clohiđric.
a/ Chất nào dư ? khối lượng dư là bao nhiêu?
b/ Tính thể tích khí H2 thu được ở đktc?
c/ Tính khối lượng muối sinh ra sau phản ứng?
Zn+2HCl->ZnCl2+H2
0,125-0,25---0,125-0,125
n HCl=\(\dfrac{9,125}{36,5}\)=0,25 mol
=>Zn dư
=>m Zn dư=(0,15-0,125).65=1,625 mol
=>VH2=0,125.22,4=2,8l
=>m ZnCl2=0,125.136=17g
nHCl = 9,125/36,5 = 0,25 (mol)
PTHH: Zn + 2HCl -> ZnCl2 + H2
LTL: 0,15 > 0,25/2 => Zn dư
nZn (p/ư) = nZnCl2 = nH2 = 0,25/2 = 0,125 (mol)
mZn (dư) = (0,15 - 0,125) . 65 = 1,625 (g)
VH2 = 0,125 . 22,4 = 2,8 (l)
mZnCl2 = 0,125 . 136 = 17 (g)
\(n_{HCl}=\dfrac{m_{HCl}}{M_{HCl}}=\dfrac{9,15}{36,5}=0,250mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
1 2 1 1 ( mol )
0,15 > 0,250 ( mol )
0,125 0,25 0,125 0,125 ( mol )
Chất dư là Zn
\(m_{Zn\left(du\right)}=n_{Zn\left(du\right)}.M_{Zn}=\left(0,15-0,125\right).65=1,625g\)
\(V_{H_2}=n_{H_2}.22,4=0,125.22,4=2,8l\)
\(m_{ZnCl_2}=n_{ZnCl_2}.M_{ZnCl_2}=0,125.136=17g\)