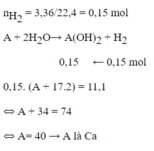Cho 4,6 gam kim loại R có hóa trị I tác dụng hoàn toàn với nước ở nhiệt độ thường , sau phản ứng thu được 8 gam base và thấy có khí hydrogen thoát ra ngoài .
a. Viết PTHH của phản ứng
b. Xác định kim loại R

Những câu hỏi liên quan
Cho 20 gam kim loại R có hóa trị II tác dụng hoàn toàn với nước ở nhiệt độ thường , sau phản ứng thu được dung dịch base và thấy có 11,2 lít khí hydrogen thoát ra ngoài .
a. Viết PTHH của phản ứng
b. Xác định kim loại R. Biết thể tích các khí đo ở đktc
\(a.R+2H_2O\rightarrow R\left(OH\right)_2+H_2\\
b.n_{H_2}=\dfrac{11,2}{22,4}=0,5mol\\
n_R=n_{H_2}=0,5mol\\
M_R=\dfrac{20}{0,5}=40g/mol\)
Vậy kim loại R là Ca
Đúng 2
Bình luận (0)
nhiệt phân hoàn toàn 94,8 gam KMnO4 sau phản ứng thấy thoát ra V (lít) khí oxi (đktc)
a) Viết PTHH của phản ứng trên và giá trị của V
b) để đốt cháy hoàn toàn 5,76 gam kim loại R (có hóa trị II) cần dùng 40% lượng oxi sinh ra từ phản ứng trên. Hãy xác định kim loại R
nKMnO4=94,8:158=0,6(mol)
PTHH: 2KMnO4-t--> K2MnO4+MnO2+O2
0,6----------------------------------->0,3(mol)
=>V= VO2=0,3. 22,4= 6,72(l)
b ) 40%nO2 =40%.0,3=0,12(mol)
2R + O2 -t--->2RO
0,24(mol)<- 0,12
=> M(Khối lượng Mol ) R= m:n=5,76:0,24=24(G/MOL)
=> R là Mg
Đúng 2
Bình luận (1)
a)-\(n_{KMnO_4}=\dfrac{m}{M}=\dfrac{94,8}{158}=0,6\left(mol\right)\)
-PTHH: \(2KMnO_4\rightarrow^{t^0}K_2MnO_4+MnO_2+O_2\uparrow\)
2 1
0,6 0,3
\(\Rightarrow V_{O_2\left(đktc\right)}=n.22,4=0,3.22,4=6,72\left(l\right)\)
b)-\(V_{O_2\left(cd\right)}=6,72.\dfrac{40}{100}=2,688\left(l\right)\)
\(\Rightarrow n_{O_2}=\dfrac{V}{22,4}=\dfrac{2,688}{22,4}=0,12\left(mol\right)\)
-PTHH: \(2R+O_2\rightarrow^{t^0}2RO\)
2 1
0,24 0,12
\(m_R=n.M=5,76\left(g\right)\)
\(\Rightarrow0,24.M_R=5,76\)
\(\Rightarrow M_R=24\) (g/mol)
-Vậy R là Crom
Đúng 0
Bình luận (2)
Cho kim loại A, hóa trị II tác dụng với nước ở nhiệt độ thường. Biết rằng sau phản ứng thu được 4,48 l khí thoát ra ở đktc và khối lượng của bazo thu được là 34,2 gam. Tìm kim loại A
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\); \(n_{A\left(OH\right)_2}=\dfrac{34,2}{M_A+34}\left(mol\right)\)
\(A+2H_2O\rightarrow A\left(OH\right)_2+H_2\)
\(\dfrac{34,2}{M_A+34}\) --> \(\dfrac{34,2}{M_A+34}\) ( mol )
\(\rightarrow n_{H_2}=\dfrac{34,2}{M_A+34}=0,2\left(mol\right)\)
\(\Leftrightarrow34,2=0,2M_A+6,8\)
\(\Leftrightarrow0,2M_A=27,4\)
\(\Leftrightarrow M_A=137\) ( g/mol )
--> A là Bari ( Ba )
Đúng 4
Bình luận (0)
\(A+H_2O\rightarrow A\left(OH\right)_2+H_2\\ n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ TheoPT:n_{H_2}=n_{A\left(OH\right)_2}=0,2\left(mol\right)\\ \Rightarrow M_{A\left(OH\right)_2}=A+17.2=\dfrac{34,2}{0,2}=171\\ \Rightarrow A=137\left(Ba\right)\)
Đúng 2
Bình luận (0)
nhiệt phân hoàn toàn 94,8 gam KMnO4 sau phản ứng thấy thoát ra V (lít) khí oxi (đktc)
a) Viết PTHH của phản ứng trên và giá trị của V
b) để đốt cháy hoàn toàn 5,76 gam kim loại R (có hóa trị không thay đổi) cần dùng 40% lượng oxi sinh ra từ phản ứng trên. Hãy xác định kim loại R
nKMnO4 = 94,8: 158=0,6(mol)
pthh : 2KMnO4 -t--> K2MnO4 + MnO2 + O2
0,6-------------------------------------->0,3(mol)
V= VO2 = 0,3.22,4 = 6,72 (l)
40%nO2 = 40%.0,3=0,12 (mol )
pthh : 2R+ O2 -t-> 2RO
0,24<-0,12(MOL)
=>MR =5,76: 0,24= 24(g/mol)
=> R là Mg
Đúng 1
Bình luận (0)
Cho kim loại A, hóa trị II tác dụng với nước ở nhiệt độ thường. Biết rằng sau phản ứng thu được 3,36 l khí thoát ra ở đktc và khối lượng của bazơ có trong dung dịch thu được là 11,1 gam. Tìm A
A. Ba
B. Ca
C. Na
D. Cu
Cho kim loại A, hóa trị II tác dụng với nước ở nhiệt độ thường. Biết rằng sau phản ứng thu được 4,48 l khí thoát ra ở đktc và khối lượng của bazơ có trong dung dịch thu được là 34,2 gam. Tìm A
`A + 2H_2 O -> A(OH)_2 + H_2`
`n_[H_2] = [ 4,48 ] / [22,4 ] = 0,2 (mol)`
`n_[A(OH)_2] = [ 34,2 ] / [ M_A + 34 ] (mol)`
Mà `n_[H_2] = n_[A(OH)_2]`
`=> [34,2] / [M_A + 34] = 0,2`
`<=>M_A = 137 ( g // mol)`
`-> A` là `Ba`
Đúng 2
Bình luận (0)
Câu 2.
Nhiệt phân hoàn toàn 31,6 gam KMnO4 sau phản ứng thấy thoát ra V (lít) khí oxi (đktc).
a) Viết PTHH của phản ứng trên và tính giá trị của V?
b) Để đốt cháy hoàn toàn 2,16 gam kim loại R (có hóa trị không đổi) cần dùng 60% lượng oxi sinh ra từ phản ứng trên. Hãy xác định kim loại R.
a.\(n_{KMnO_4}=\dfrac{m}{M}=\dfrac{31,6}{158}=0,2mol\)
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,2 0,1 ( mol )
\(V_{O_2}=n.22,4=0,1.22,4=2,24l\)
b.\(n_{O_2}=0,1.60\%=0,06mol\)
\(2R+\dfrac{1}{2}nO_2\rightarrow\left(t^o\right)R_2O_n\)
\(\dfrac{2,16}{M_R}\) \(\dfrac{2,16n}{M_R}\) ( mol )
\(\Rightarrow\dfrac{2,16n}{M_R}=0,06\)
\(\Rightarrow0,06M_R=2,16n\)
\(\Rightarrow M_R=36n\)
Biện luận:
-n=1 => Loại
-n=2 => Loại
-n=3 => \(M_R=108\) ( g/mol ) R là Bạc ( Ag )
Vậy R là Bạc (Ag)
Đúng 1
Bình luận (1)
1. Cho 8,64 gam kim loại R (có hoá trị n không đổi) tác dụng với O2, sau khi phản ứng hoàn toàn thu được 13,44 gam chất rắn. Hoà tan chất rắn sau phản ứng bằng dung dịch HCl dư thấy thoát ra 1,344 lít H2 (đktc). Xác định kim loại R.2. Cho m gam Al tác dụng với 0.05 mol O2 thu được chất rắn X. Hòa tan hết X trong dung dịch HCl dư thu được 0.03 mol H2. Tính giá trị của m.
\(2R+2nHCl\rightarrow2RCl_n+nH_2\)
.0,12/n...............0,12/n......0,06......
\(R_2O_n+2nHCl\rightarrow2RCl_n+nH_2O\)
.0,3/n......................................0,3....
\(n_{H_2O}=2n_{O_2}=0,3\left(mol\right)\)
Có : \(m=13,44=m_R+m_{R_2O_n}=\dfrac{0,12R}{n}+\dfrac{\left(2R+16n\right)0,3}{n}\)
\(\Rightarrow R=12n\)
=> R là Mg
Đúng 2
Bình luận (0)
\(n_{Al\left(I\right)}=\dfrac{3}{2}n_{H_2}=0,045\left(mol\right)\)
\(n_{Al\left(II\right)}=2n_{Al_2O_3}=\dfrac{2}{3}n_{H_2O}=\dfrac{2}{3}.2n_{O_2}=\dfrac{4}{3}n_{O_2}=\dfrac{1}{15}\left(mol\right)\)
\(\Rightarrow m_{Al}=m=3,015\left(g\right)\)
Đúng 1
Bình luận (0)
Cho kim loại A, hóa trị II tác dụng với nước ở nhiệt độ thường. Biết rằng sau phản ứng thu được 3,36 l khí thoát ra ở đktc và khối lượng của bazơ thu được là 11,1 gam. Tìm A
A. Ba
B. Ca
C. Na
D. Cu
giúp mk với
\(n_{H_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(A+2H_2O\rightarrow A\left(OH\right)_2+H_2\)
\(................0.15.....0.15\)
\(M_{A\left(OH\right)_2}=\dfrac{11.1}{0.15}=74\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow A=40\)
\(\Rightarrow B\)
Đúng 2
Bình luận (0)
$A + 2H_2O \to A(OH)_2 + H_2$
n A(OH)2 = n H2 = 3,36/22,4 = 0,15(mol)
M A(OH)2 = A + 34 = 11,1/0,15 = 74
=> A = 40(Ca)
Vậy A là Canxi
Đáp án B
Đúng 1
Bình luận (0)