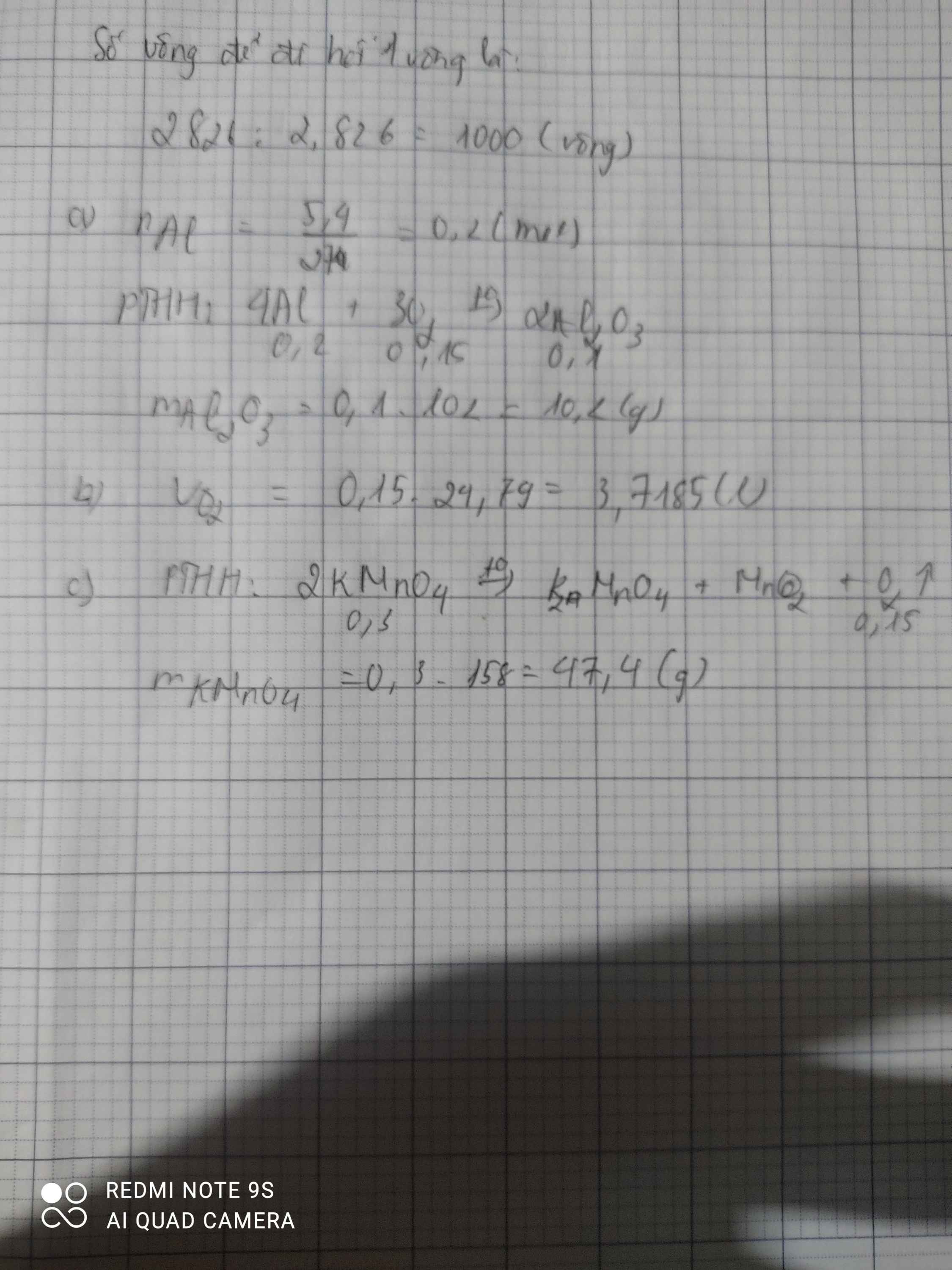Đốt cháy hết 0,54 gam Al trong không khí thu được aluminium oxide Lập phương trình hóa học của phản ứng rồi tính: a. Khối lượng aluminium oxide tạo ra. b. Thể tích khí oxygen tham gia phản ứng ở điều kiện chuẩn

Những câu hỏi liên quan
Đốt cháy hết 0,54 gam Al trong không khí thu được aluminium oxide theo sơ đồ phản ứng:
Al + O2 → Al2O3
Lập phương trình hoá học của phản ứng rồi tính:
a) Khối lượng aluminium oxide tạo ra.
b) Thể tích khí oxygen tham gia phản ứng ở điều kiện chuẩn.
Phương trình hoá học: 4Al + 3O2 → 2Al2O3.
Số mol Al tham gia phản ứng:
n Al = mAl : M Al = 0,54 : 27 = 0,02 mol
a) Từ phương trình hóa học ta có:
n Al2O3 = ½ n Al = 0,02 : 2 = 0,01 mol
n Al2O3 = 0,01 x 102 = 10,2 gam
b) theo phương trình hóa học ta có:
n O2 = ¾ n Al = ¾ x 0,02 = 0,015 mol
V O2 (đkc) = 0,015 x 24,79 = 0,37185 (lít)
Đúng 1
Bình luận (0)
\(PTHH:4Al+3O_2\left(t^o\right)\rightarrow2Al_2O_3\\ n_{Al}=\dfrac{0,54}{27}=0,02\left(mol\right)\Rightarrow n_{Al}=\dfrac{2}{4}.0,02=0,01\left(mol\right);n_{O_2}=\dfrac{3}{4}.0,02=0,15\left(mol\right)\\ a,m_{Al_2O_3}=0,01.27=0,27\left(g\right)\\ b,V_{O_2\left(đkc\right)}=0,15.24,79=3,7185\left(l\right)\)
Đúng 0
Bình luận (0)
Đốt cháy hết 5,4 gam aluminium (Al) trong không khí thu được aluminium oxide (Al2O3).
a) Tính khối lượng aluminium oxide thu được.
b) Tính thế tích khí oxygen tham gia phản ứng ở điều kiện chuẩn.
Đọc tiếp
Đốt cháy hết 5,4 gam aluminium (Al) trong không khí thu được aluminium oxide (Al2O3).
a) Tính khối lượng aluminium oxide thu được.
b) Tính thế tích khí oxygen tham gia phản ứng ở điều kiện chuẩn.
\(a)n_{Al}=\dfrac{5,4}{27}=0,2mol\\ 4Al+3O_2\xrightarrow[]{t^0}2Al_2O_3\\ n_{Al_2O_3}=\dfrac{0,2.2}{4}=0,1mol\\ m_{Al_2O_3}=0,1.102=10,2g\\ b)n_{H_2}=\dfrac{0,2.3}{4}=0,15mol\\ V_{O_2}=0,15.24,79=3,7185l\)
Đúng 1
Bình luận (0)
Đốt cháy mg kim loại Aluminium (Al) trong không khí thu được 10g hợp chất Aluminium oxide (AL2O3). Biết rằng khối lượng Aluminium (Al) tham gia bằng 1,5 lần khối lượng của oxygen (không khí) tham gia phản ứng.
a. Viết phản ứng hoá học.
b. Tính khối lượng của Al và oxygen đã phản ứng.
a, \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
b, Gọi: mO2 = x (g) ⇒ mAl = 1,5x (g)
Theo ĐLBT KL, có: mAl + mO2 = mAl2O3
⇒ 1,5x + x = 10
⇒ x = 4 (g) = mO2
mAl = 1,5.4 = 6 (g)
Đúng 1
Bình luận (0)
hòa tan m gam nhôm ( aluminium ) trong khí oxygen dư thu được 20,4 gam aluminium oxide ( AL2O3)
a) viết phương trình hóa học xảy ra
b) tính khối lượng nhôm (aluminium) đã tham gia phản ứng
c) tính khối lượng H2SO4 đã tham gia phản ứng
*Giúp mik vs mik cần gấp ạ*
\(a)4Al+3O_2\xrightarrow[]{t^0}2Al_2O_3\\ b)n_{Al_2O_3}=\dfrac{20,4}{102}=0,2mol\\ n_{Al}=\dfrac{0,2.4}{2}=0,4mol\\ m_{Al}=0,4.27=10,8g\)
c) bạn xem lại đề
Đúng 2
Bình luận (0)
Cho 2.7 gam Aluminium cháy trong oxygen tạo ra Aluminium oxide (Al2O3) a) viết Phương Trình phản ứng xảy ra b) Tính khối lượng Al2O3 thu được c) tính thể tích oxygen ở ĐkTC
a) PTHH:
\(4Al+3O_2\xrightarrow[]{t^o}2Al_2O_3\)
b) \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
Theo PTHH: \(n_{Al_2O_3}=\dfrac{0,1\cdot2}{4}=0,05\left(mol\right)\)
\(\Rightarrow m_{Al_2O_3}=0,05\cdot102=5,1\left(g\right)\)
c) Theo PTHH: \(n_{O_2}=\dfrac{0,1\cdot3}{4}=0,075\left(mol\right)\)
\(\Rightarrow V_{O_2\left(dktc\right)}=0,075\cdot22,4=0,168\left(l\right)\)
Đúng 2
Bình luận (0)
đốt cháy 0,54 gam aluminium trong khí oxygen, phản ứng hoàn toàn thu được bao nhiêu gam aluminium oxide ? có bao nhiêu lít oxygen điều kiện tiêu chuẩn tham gia phản ứng ? Giúp m với ạ :((
\(4Al+3O_2\underrightarrow{^{to}}2Al_2O_3\\ n_{Al}=\dfrac{0,54}{27}=0,02\left(mol\right)\\ \Rightarrow n_{Al_2O_3}=\dfrac{2}{4}.0,02=0,01\left(mol\right)\\ n_{O_2}=\dfrac{3}{4}.0,02=0,015\left(mol\right)\\ m_{Al_2O_3}=102.0,01=1,02\left(g\right)\\ V_{O_2\left(đktc\right)}=0,015.22,4=0,336\left(l\right)\)
Đúng 1
Bình luận (0)
Đốt cháy 5,4 gam aluminium thu được aluminium oxide
a) Tính khối lượng aluminium oxide thu được
b) Tính thể tích khí oxygen cần dùng (đkc)
c) Tính khối lượng thuốc tím cần để điều chế khí oxygen cho phản ứng trên ( Al=27, O=16, K=39, Mn=55 )
Đốt cháy Aluminium (AL) trong không khí thu được 10, 2g chất oxide (Al203) . Biết rằng, Al cháy là xảy ra phản ứng với oxygen (O2) trong không khí [1] Viết công thức về khối lượng của phan ứng [2] Tính khối lượng của khí oxygen đã phản ứng
1. Theo ĐLBT KL, có: mAl + mO2 = mAl2O3
2. \(n_{Al_2O_3}=\dfrac{10,2}{102}=0,1\left(mol\right)\)
PT: \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
Theo PT: \(n_{O_2}=\dfrac{3}{2}n_{Al_2O_3}=0,15\left(mol\right)\)
\(\Rightarrow m_{O_2}=0,15.32=4,8\left(g\right)\)
Đúng 1
Bình luận (0)
\(\left[1\right]BTKL:m_{Al}+m_{O_2}=m_{Al_2O_3}\\ \left[2\right]n_{Al_2O_3}=\dfrac{10,2}{102}=0,1mol\\ 4Al+3O_2\xrightarrow[]{t^0}2Al_2O_3\\ n_{O_2}=\dfrac{0,1.4}{2}=0,2mol\\ m_{Al}=0,2.27=5,4g\)
Đúng 0
Bình luận (0)
Đốt cháy aluminium trong bình chứa 9,6g khí oxygen thu được 20,4g aluminium oxide (Al 2 O 3 ).
a. Viết phương trình chữ của phản ứng.
b. Viết biểu thức khối lượng của phản ứng xảy ra.
c. Tính khối lượng aluminium đã phản ứng?
Cu = 64, O =16, H=1, P= 31, Ca =40, Fe =56, S=32, Al = 27
a. Aluminium + Khí oxygen -> Aluminium oxide
b. \(m_{Al}+m_O=m_{Al_{2_{ }}O_3}\)
c. Từ câu b => \(m_{Al}=m_{Al_{2_{ }}O_3}-m_O=20.4-9.6=10.8\)
Đúng 2
Bình luận (0)
Phương trình chữ:
aluminium + oxygen \(\rightarrow\) aluminium oxide
Biểu thức khối lượng:
\(m_{Al}+m_{O_2}=m_{Al_2O_3}\)
Khối lượng aluminium:
\(m_{Al}=m_{Al_2O_3}-m_{O_2}=20,4-9,6=10,8g\)
Đúng 1
Bình luận (0)