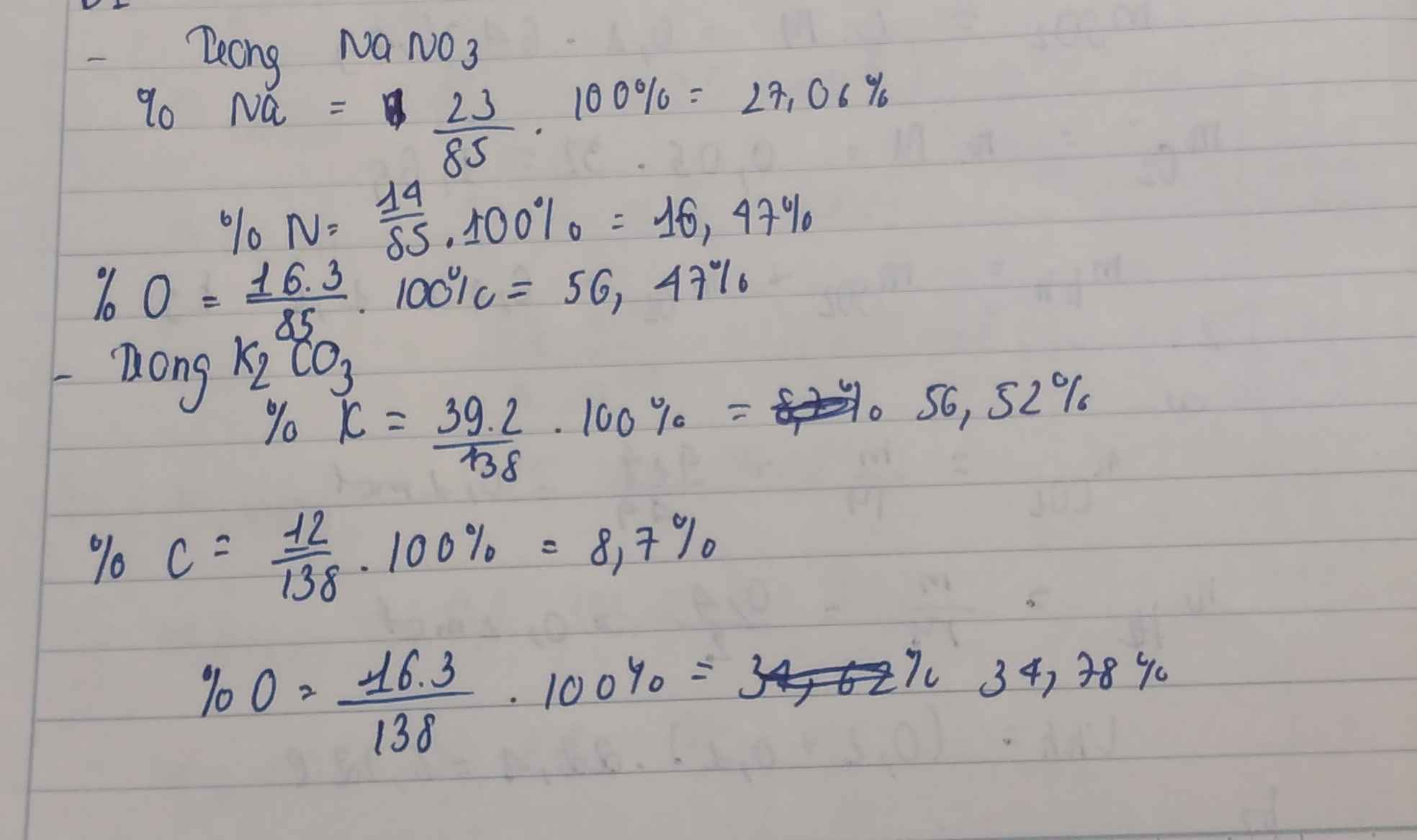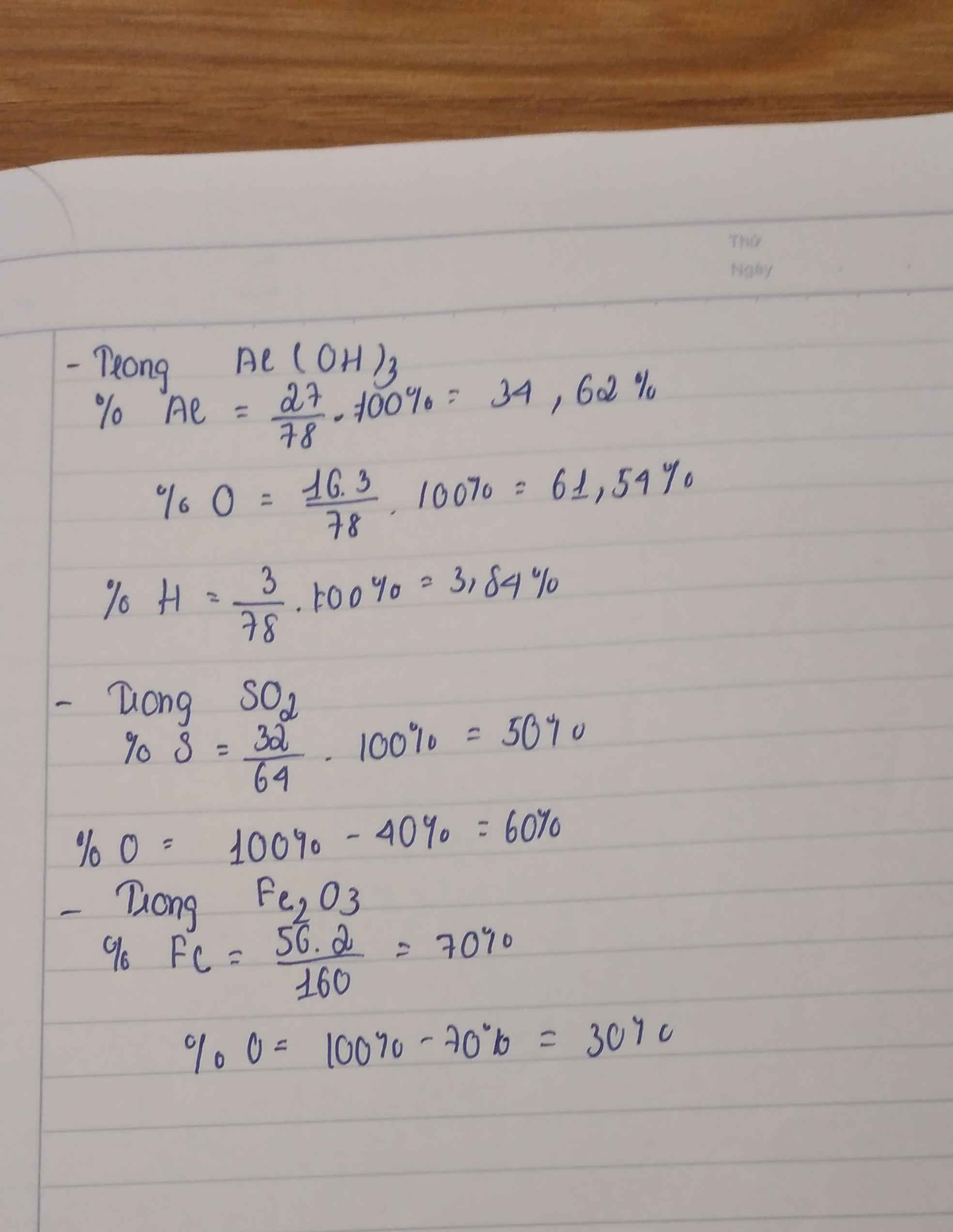Tính % khối lượng của N trong các hợp chất sau: CO2, HNO2, NaNO3, K2SO4

Những câu hỏi liên quan
. Tính thành phần % theo khối lượng của các nguyên tố trong mối hợp chất sau:
b/ K2SO4.
\(M_{K_2SO_4}=39.2+32+16.4=174(g/mol)\\ \%_K=\dfrac{39.2}{174}.100\%=44,83\%\\ \%_S=\dfrac{32}{174}.100\%=18,39\%\\ \%_O=100\%-44,83\%-18,39\%=36,78\%\)
Đúng 2
Bình luận (0)
\(\%K=\dfrac{39.2}{174}.100\%=44,8\%\)
\(\%S=\dfrac{32}{174}.100\%=18,4\%\)
\(\%O=100\%-44,8\%-18,4\%=36,8\%\)
Đúng 0
Bình luận (0)
tính khối lượng mol của hợp chất sau :
a,Cao b,Ba(OH)2 c,MgSO4 d,HNO2
a, \(M_{CaO}=40+16=56\left(g/mol\right)\)
b, \(M_{Ba\left(OH\right)_2}=137+17.2=171\left(g/mol\right)\)
c, \(M_{MgSO_4}=24+32+16.4=120\left(g/mol\right)\)
d, \(M_{HNO_2}=1+14+16.2=47\left(g/mol\right)\)
Bạn tham khảo nhé!
Đúng 1
Bình luận (1)
TÍNH THÀNH PHẦN PHẦN TRĂM THEO KHỐI LƯỢNG CỦA CÁC NGUYÊN TỐ CÓ CHỨA TRONG HỢP CHẤT K2SO4
Ta có: MK2SO4 = 39.2 + 32 + 16.4 = 174 (g/mol)
\(\Rightarrow\left\{{}\begin{matrix}\%K=\dfrac{39.2}{174}.100\%\approx44,8\%\\\%S=\dfrac{32}{174}.100\%\approx18,4\%\\\%O\approx36,8\%\end{matrix}\right.\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (1)
Ta có: MK2SO4 = 39.2 + 32 + 16.4 = 174 (g/mol)
Đúng 1
Bình luận (0)
Câu 1:Trình bày phương pháp nhận biết các chất sau:a) CuSO4, AgNO3, NAClb) NaOH, HCl, NaNO3, NaClc) KOH, K2SO4, K2CO3, KNO3Câu 2:Cho một khối lượng mạt sắt dư vào 150ml dung dịch HCl. Sau phản ứng thu được 10,08 l khí (đktc).a) tính khối lượng mạt sắt tham gia phản ứng.b) tính nồng độ mol của dung dịch HCl đã dùng.Câu 3:Cho 15,75g hỗn hợp 2 kim loại Cu và Zn vào dung dịch H2SO4 loãng dư, thu được 33,6 l khí (đktc).a) tính khối lượng mỗi kim loại trong hỗn hợp đầu.b) tính khối lượng dung dịch muố...
Đọc tiếp
Câu 1:Trình bày phương pháp nhận biết các chất sau:
a) CuSO4, AgNO3, NACl
b) NaOH, HCl, NaNO3, NaCl
c) KOH, K2SO4, K2CO3, KNO3
Câu 2:Cho một khối lượng mạt sắt dư vào 150ml dung dịch HCl. Sau phản ứng thu được 10,08 l khí (đktc).
a) tính khối lượng mạt sắt tham gia phản ứng.
b) tính nồng độ mol của dung dịch HCl đã dùng.
Câu 3:Cho 15,75g hỗn hợp 2 kim loại Cu và Zn vào dung dịch H2SO4 loãng dư, thu được 33,6 l khí (đktc).
a) tính khối lượng mỗi kim loại trong hỗn hợp đầu.
b) tính khối lượng dung dịch muối thu được.
(mik đang cần gấp lắm ạ, m.n giúp mik với. Cảm ơn m.n)
1. a) Quan sát màu sắc của các dung dịch ta thấy CuSO4 có màu xanh lam
AgNO3, NaCl không màu
Cho quỳ tím vào 2 dung dịch không màu trên
+ Quỳ hóa đỏ: AgNO3
+ Quỳ không đổi màu: NaCl
b) Cho quỳ tím vào các mẫu thử
+ Quỳ hóa đỏ: HCl
+ Quỳ hóa xanh: NaOH
+ Quỳ không đổi màu: NaNO3, NaCl
Cho AgNO3 vào 2 mẫu thử làm quỳ không đổi màu
+ Kết tủa: NaCl
\(NaCl+AgNO_3\rightarrow NaNO_3+AgCl\downarrow\)
+ Không hiện tượng: NaNO3
c) Cho quỳ tím vào từng mẫu thử
+ Quỳ hóa xanh: KOH, K2CO3
+ Quỳ không đổi màu: K2SO4, KNO3
Cho dung dịch HCl vào 2 mẫu làm quỳ hóa xanh
+ Có khí thoát ra: K2CO3
\(K_2CO_3+2HCl\rightarrow2KCl+CO_2+H_2O\)
+ Không hiện tượng: KOH
\(KOH+HCl\rightarrow KCl+H_2O\)
Cho dung dịch BaCl2 vào 2 mẫu không làm quỳ đổi màu
+ Kết tủa: K2SO4
\(BaCl_2+K_2SO_4\rightarrow BaSO_4+2KCl\)
+ Không hiện tượng: KNO3
Đúng 3
Bình luận (0)
2)\(a.Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{Fe}=n_{H_2}=0,45\left(mol\right)\\ \Rightarrow m_{Fe}=0,45.56=25,2\left(g\right)\\ b.n_{HCl}=2n_{H_2}=0,9\left(mol\right)\\ \Rightarrow CM_{HCl}=\dfrac{0,9}{0,15}=6M\)
Đúng 3
Bình luận (0)
\(3.a.Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ n_{H_2}=n_{Zn}=0,15\left(mol\right)\\ \Rightarrow m_{Zn}=0,15.65=9,75\left(g\right)\\ \Rightarrow m_{Cu}=15,75-9,75=6\left(g\right)\\ b.n_{ZnSO_4}=n_{H_2}=0,15\left(mol\right)\\ \Rightarrow m_{ZnSO_4}=0,15.161=24,15\left(g\right)\)
Đúng 3
Bình luận (0)
Tính phần trăm khối lượng của các nguyên tố trong hợp chất: NaNO3; K2CO3 , Al(OH)3, SO2, SO3, Fe2O3.
\(NaNO_3\\ \%m_{Na}=\dfrac{23}{23+14+3.16}.100\approx27,059\%\\ \%m_N=\dfrac{14}{23+14+3.16}.100\approx16,471\%\\ \%m_O=\dfrac{3.16}{23+14+3.16}.100\approx56,471\%\)
Em tương tự làm cho các chất còn lại!
Đúng 0
Bình luận (0)
CÂU 1Dãy chất chỉ gồm các đơn chất là
A.Na2SO4, K2SO4, CaCO3.
B.Cl2, CO2, ZnO.
C.H2, N2, Na.
D.NaOH, H2CO3, H2SO4.
CÂU 2 Hợp chất tạo bởi nguyên tố A hóa trị III và nguyên tố oxi, trong đó nguyên tố A chiếm 52,94% về khối lượng. Công thức hóa học của hợp chất là: ( Cho biết: P= 31; Fe= 56, Cr=52; Al= 27; O=16)
A.P2O3
B.Cr2O3
C.Al2O3
D.Fe2O3
Câu 1: Tính phần trăm khối lượng của các nguyên tố trong hợp chất: NaNO3; K2CO3, Al(OH)3, SO2, SO3, Fe2O3 .
Câu 1: Tính phần trăm khối lượng của các nguyên tố trong hợp chất: NaNO3; K2CO3 , Al(OH)3, SO2, SO3, Fe2O3.
\(PTK_{NaNO_3}=23+14+3.16=85\left(đvC\right)\)
\(\%m_{Na}=\dfrac{23}{85}.100=27,05\%\)
\(\%m_N=\dfrac{14}{85}.100=16,47\%\)
\(\%m_O=\dfrac{3.16}{85}=56,47\%\)
\(PTK_{K_2CO_3}=2.39+12+3.16=138\left(đvC\right)\)
\(\%m_K=\dfrac{78}{138}.100=56,52\%\)
\(\%m_C=\dfrac{12}{138}.100=8,69\%\)
\(\%m_O=\dfrac{3.16}{138}.100=34,78\%\)
các ý còn lại làm tương tự
Đúng 5
Bình luận (1)
Trong cốc B chứa hỗn hợp gồm 2 muối. Đổ nước vào cốc, khuấy đều thấy có khí CO2 thoát
ra, dung dịch thu được chỉ chứa muối K2SO4. Hai muối ban đầu có thể là những chất nào?
Tính tỉ lệ khối lượng của chúng trong hỗn hợp.
Hai muối ban đầu có thể là K2CO3 và KHSO4
PTHH: K2CO3 + 2KHSO4 --> 2K2SO4 + CO2 + H2O
Do dd chỉ chứa K2SO4
=> Pư vừa đủ
\(\dfrac{n_{K_2CO_3}}{n_{KHSO_4}}=\dfrac{1}{2}\)
Xét \(\dfrac{m_{K_2CO_3}}{m_{KHSO_4}}=\dfrac{138.n_{K_2CO_3}}{136.n_{KHSO_4}}=\dfrac{69}{136}\)
Đúng 4
Bình luận (0)