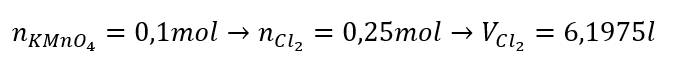CHO 15.8G

Những câu hỏi liên quan
Cho 15.8g KMnO4 tác dụng hoàn toàn với dung dịch HCL đậm đặc . Tính thể tích khí Cl2 thu được ở đkc
\(n_{KMnO_4}=\dfrac{15,8}{158}=0,1\left(mol\right)\\ 2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\\ n_{Cl_2}=\dfrac{5}{2}.0,1=0,25\left(mol\right)\\ V_{Cl_2\left(đkc\right)}=0,25.24,79=6,1975\left(l\right)\)
Đúng 0
Bình luận (0)
Cho 15.8g KMnO4 tác dụng hoàn toàn với dung dịch HCL đậm đặc . Tính thể tích khí Cl2 thu được ở đkc
Nung 15.8g KMnO4. Sau thời gian thu được 15.16g chất rắn. Tính hiệu suất
2KMnO4---->K2MnO4+MnO2+O2
Áp dụng định luật bảo toàn khối lượng ta có
m O2=m KMnO4- m chất rắn
=15,8-15,16=0,64(g)
n O2=0,64/32=0,02(mol)
Theo pthh
n KMnO4=2n O2=0,04(mol)
m KMnO4=0,04.158=6,32(g)
H%=\(\frac{6,32}{15,8}.100\%=40\%\)
https://i.imgur.com/jxTd7Dd.jpg
\(\text{nKMnO4}=\frac{15,8}{158}=0,1\left(mol\right)\)
Ta có:
1 mol kmno4---> 0,5 mol o2
=>0,1 mol kmno4----->0,05 mol o2
=>m O2(1)= 0,05×32=1,6g
Theo đề: \(\text{mO2(2)=15,8-15,16=0,64g}\)
=>H=mO2(1)/mO2(2)×100%
=>H=0,64/1,6×100%=\(\text{40%}\)
1. cho 7.2g 1 kim loại tác dụng vừa đủ với HCl cho 6.72l khí H2 (đktc). Cho biết kim loại đó?
2. cho 15.8g KMnO4 tác dụng hoàn toán với dd HCl đặc, dư. Thế tích khí thu được (đktc) là bao nhiêu?
1. gọi x là hóa trị của lim loại đó
nH2=\(\dfrac{6,72}{22,4}\)= 0,3
bảo toàn e:
\(x\times\dfrac{7,2}{M}=2\times0,3\)
với x=2 thì M=24 (Mg)
Đúng 0
Bình luận (0)
C1: trong phòng thí nghiệm, ng ta điều chế oxi bằng cách phân hủy hoàn toàn 15.8g KMnO4 a) Viết Phương trình phản ứng B) tính thể tích oxi điều chế đc(đktc)? C) tính khối lượng sắt cần dùng để phản ứng hết vs thể tích khí oxi thu đc hết ở trên
a) $2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
b) n KMnO4 = 15,8/158 = 0,1(mol)
Theo PTHH : n O2 = 1/2 n KMnO4 = 0,05(mol)
=> V O2 = 0,05.22,4 = 1,12(lít)
c)
$3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$
Theo PTHH : n Fe = 3/2 nO2 = 0,075(mol)
=> m Fe = 0,075.56 = 4,2(gam)
Đúng 2
Bình luận (0)
Theo gt ta có: $n_{KMnO_4}=0,1(mol)$
a, $2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2$
b, Ta có: $n_{O_2}=0,05(mol)\Rightarrow V_{O_2}=1,12(mol)$
c, $3Fe+2O_2\rightarrow Fe_3O_4$
Ta có: $n_{Fe}=0,075(mol)\Rightarrow m_{Fe}=4,2(g)$
Đúng 1
Bình luận (0)
tính thể tích khí oxi thu được ở đktc khi phân huỷ 15.8g KMnO4 ở nhiệt độ cao. Với thể tích khí oxi đó có đủ oxi hoá hoàn toàn 3.2g bột lưu huỳnh không?
\(2KMnO4-->K2MnO4+MnO2+O2\)
\(n_{KMnO4}=\frac{15,8}{158}=0,1\left(mol\right)\)
\(n_{O2}=\frac{1}{2}n_{KMnO4}=0,05\left(Mol\right)\)
\(V_{O2}=0,05.22,4=1,12\left(l\right)\)
\(S+O2-->SO2\)
\(n_S=\frac{3,2}{32}=0,1\left(mol\right)\)
\(n_S>n_{O2}\) \(\Rightarrow\) lượng O2 k đủ
Hòa toàn 15.8g hh Al,Mgvà Fe vào 500ml dd HCl 2.5M thu đượcb13.44 H2 (đktc) và dd A. Trong hh có số mol Al bằng số mol Mg. Tính % kl mỗi kim loại trong hh đã hòa tan và tính kl muối có trong dd A
Gọi x, x, y là số mol của Al Mg và Fe
mhh= 27x + 24x + 56y=15.8 (g)
<=> 51x + 56y= 15.8 (1)
2Al + 6HCl --> 2AlCl3 + 3H2(2)
Mg +2HCl --> MgCl2 + H2(3)
Fe + 2HCl --> FeCl2 + H2(4)
nH2= 1.5x + x + y=2.5x + y= 0.6 (mol) (5)
Giải pt (1) và (5) có:
x=0.2
y=0.1
%Al= 0.2*27/15.8 * 100= 34.17%
%Mg= 0.2*24/15.8 * 100=30.38%
%Fe= 100-34.17-30.38=35.48%
mAlCl3=0.2* 133.5=26.7g
mMgCl2= 0.2* 95=19g
mFeCl2= 0.1* 127=12.7g
Đúng 0
Bình luận (0)
2Al + 6HCl => 2AlCl3 + 3H2
Mg + 2HCl => MgCl2 + H2
Fe + 2HCl => FeCl2 + H2
nHCl = CM.V = 0.5 x 2.5 = 1.25 (mol)
nH2 = V/22.4 = 13.44/22.4 = 0.6 (mol)
Gọi x,y,z (mol) lần lượt là số mol của Al, Mg và Fe
Theo đề bài và phương trình, ta có:
27x + 24y + 56z = 15.8
1.5x + y + z = 0.6
x = y
Giải phương trình ta được:
x = 0.2; y = 0.2; z = 0.1 (mol)
mAl = n.M = 27 x 0.2 = 5.4 (g)
mMg = n.M = 24 x 0.2 = 4.8 (g)
mFe = n.M = 56 x 0.1 = 5.6 (g)
%Al = 34.18%;
%Mg = 30.38%;
%Fe = 35.44%;
mAlCl3 = n.M = 133.5 x 0.2 (g)
mMgCl2 = n.M = 95 x 0.2 (g)
mFeCl2 = n.M = 127 x 0.1 (g)
Đúng 0
Bình luận (0)
Tính VO2 sinh ra ở đktc và kim loại rắn sau PƯ trong các TH sau
a) Nhiệt phan hoàn tàn 15.8g KMnO4
b) Nhiệt phân hoàn toàn KClO3 có lẫn 10% tạp chất trơ
c) Nhiệt phân hoàn toàn hh gồm 31.6g KMnO4 ,20g KClO3 đến khi có 80% mỗi cất đã PƯ
GIÚP MÌNH VỚI huhuhu!!!!!!!!!!!!!!!!!
\(\text{a) 2KMnO4 }\rightarrow\text{K2MnO4 + MnO2 + O2}\)
\(\text{Ta có: nKMnO4=15,8/(39+55+16.4)=0,1 mol}\)
Theo ptpu: nO2=1/2nKMnO4=0,05 mol -> VO2=0,05.22,4=1,12 lít
b) Câu này thiếu đề bạn ơi
KClO3 -> KCl +3/2O2
c) 2KMnO4 -> K2MnO4 + MnO2 + O2
KClO3 -> KCl + 3/2 O2
\(\text{Ta có: nKMnO4=31,6/158=0,2 mol;}\)
\(\text{nKClO3=20/122,5=8/49 mol}\)
nKMnO4 phản ứng=0,2.80%=0,16 mol;
nKClO3 phản ứng=8/49.80%=32/245 mol
\(\text{Theo ptpu: nO2=1/2nKMnO4 + 3/2nKClO3=338/1225 mol}\)
-> VO2=nO2.22,4=6,18 lít
a) 2KMnO4---->MnO2+K2MnO2+O2
n\(_{KMnO4}=0,1\left(mol\right)\)
Theo pthh
n\(_{O2}=\frac{1}{2}n_{KMnO4}=0,05\left(mol\right)\)
V\(_{O2}=0,05.22,4=1,12\left(l\right)\)
b) Gọi khối lượng dd KClO3 là 100g
=> m KClO3 tham gia pư là 90(g)
n\(_{KClO3}=\frac{90}{122,5}=0,73\left(mol\right)\)
2KClO3--->2KCl+3O2
Theo pthh
n\(_{O2}=\frac{3}{2}n_{KClO3}=1,095\left(mol\right)\)
V\(_{02}=1,095.22,4=24,528\left(l\right)\)
( Đề bài có nghĩa khác:)
c) Nhiệt phân hoàn toàn hh gồm 31.6g KMnO4 ,20g KClO3 với hiệu suất 80%
GIÚP MÌNH VỚI
tìm số tự nhiên bé nhất khác không chia hết cho 2, cho 3, cho, cho 5, cho 7, cho 8, cho 9, cho 12, cho 15