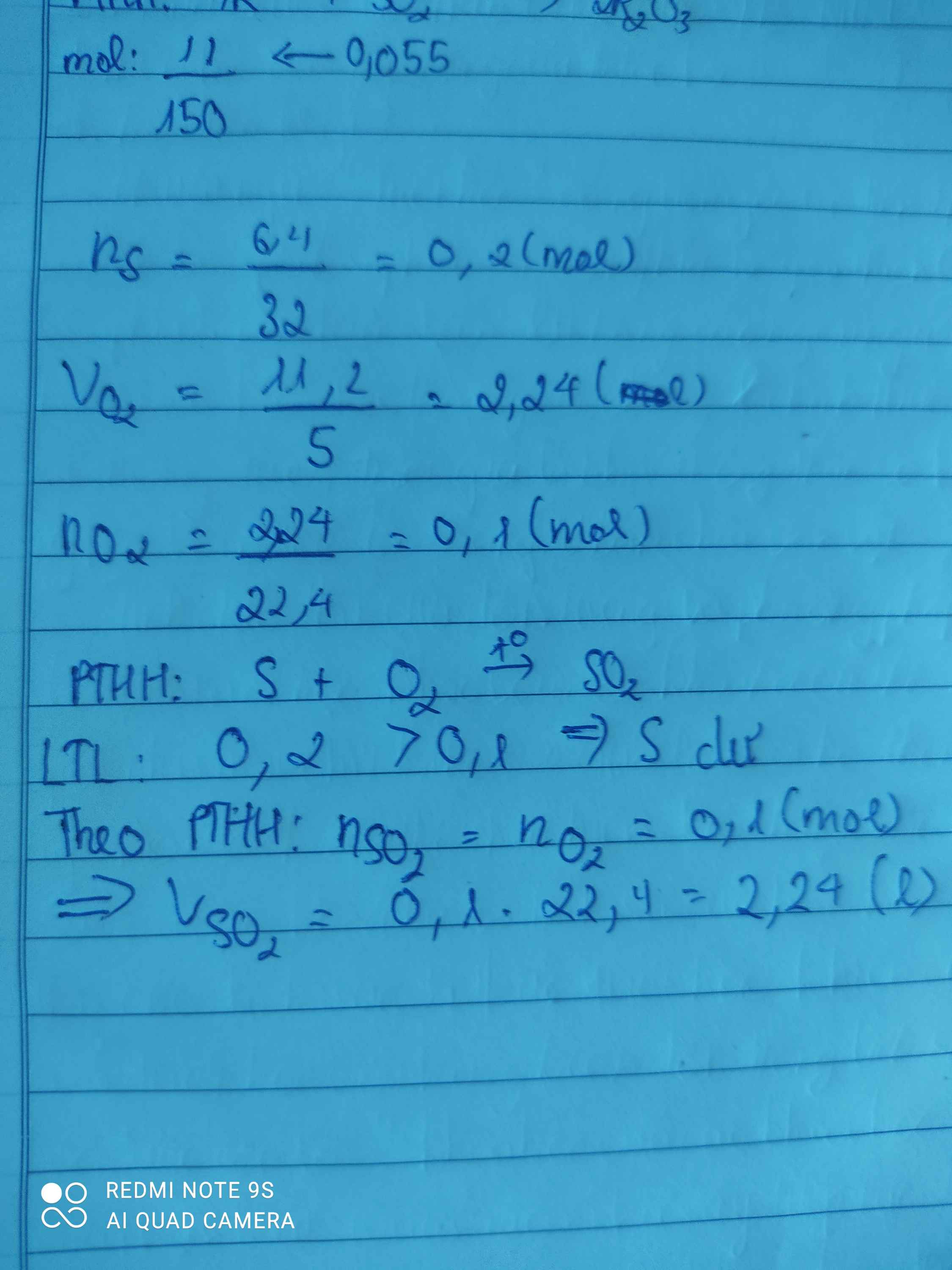thể tích khí oxi có trong bình chứa 28 lít không khí

Những câu hỏi liên quan
Trong V(lít) không khí có 28 lít khí oxi. Biết oxi chiếm 20% thể tích không khí. Giá trị của V là ... lít
\(V_{kk}=28:20\cdot100=140\left(l\right)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 2,768 Lít khí CH4 trong bình chứa khí oxi dư a,viết phương trình phản ứng,tính thể tích khí oxi đã tham gia phản ứng ở (điều kiện tiêu chuẩn) b,tính thể tích không khí cần dùng biết khí oxi chiếm 20 phần trăm thể tích không khí
\(a,CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
Vì n và V tỉ lệ thuận với nhau. Nên ta có:
\(V_{O_2}=2.V_{CH_4}=2.2,768=5,536\left(l\right)\)
\(b,V_{kk}=\dfrac{100}{21}.V_{O_2}=\dfrac{100}{21}.5,536=\dfrac{2768}{105}\left(l\right)\)
Đúng 5
Bình luận (1)
Đốt cháy 6,4 g lưu huỳnh trong một bình chứa 11,2 lít không khí ( chứa 20% thể tích khí oxi) ( đktc). Tính khối lượng khí sunfurơ thu được.
Đốt cháy 6,2 gam bột photpho trong bình chứa 22,4 lít không khí oxi ở đktc .Biết rằng thể tích oxi chiếm 1/5 thể tích không khí .Hỏi sau khi cháy :
a)photpho có cháy hết không
b)chât nào đc tạo thành và có khối lượng bao nhiêu
Xem chi tiết
\(n_P=\dfrac{m}{M}=0,2\left(mol\right)\)
- Ta có : \(V_{O_2}=\dfrac{V_{kk}}{5}=4,48\left(l\right)\)
\(n_{O_2}=\dfrac{V}{22,4}=0,2\left(mol\right)\)
\(4P+5O_2\rightarrow2P_2O_5\)
- Theo phương pháp đường chéo ta có :
=> Sau phản ứng O2 phản ứng hết, P còn dư ( dư 0,04 mol )
Vậy sau phản ứng photpho không cháy hết .
b, - Chất được tạo thành là P2O5 .
Theo PTHH : \(n_{P2O5}=\dfrac{n_P}{2}=\dfrac{0,16}{2}=0,08\left(mol\right)\)
\(\Rightarrow m_{P2O5}=n.M=11,36\left(g\right)\)
Đúng 1
Bình luận (0)
Nhiệt phân hoàn toàn m1 gam muối KClO3 ở trên, thu toàn bộ khí oxi thoát ra cho vào bình kín chứa không khí sao cho tỉ lệ thể tích . Cho hỗn hợp Y chứa m2 gam cacbon và lưu huỳnh vào bình rồi đốt cháy, lượng oxi trong bình vừa đủ để cháy hết Y. Sau phản ứng thu được hỗn hợp khí Z gồm 3 khí, trong đó khí SO2 chiếm 20% về thể tích.a) Tìm tỉ khối của khí Z đối với H2.b) Đưa nhiệt độ trong bình về 0 độ C, áp suất 760mmHg thì khí Z có thể tích là 13,44 lít. Tính m1, m2. Cho rằng không khí chứa 80% n...
Đọc tiếp
Nhiệt phân hoàn toàn m1 gam muối KClO3 ở trên, thu toàn bộ khí oxi thoát ra cho vào bình kín chứa không khí sao cho tỉ lệ thể tích . Cho hỗn hợp Y chứa m2 gam cacbon và lưu huỳnh vào bình rồi đốt cháy, lượng oxi trong bình vừa đủ để cháy hết Y. Sau phản ứng thu được hỗn hợp khí Z gồm 3 khí, trong đó khí SO2 chiếm 20% về thể tích.
a) Tìm tỉ khối của khí Z đối với H2.
b) Đưa nhiệt độ trong bình về 0 độ C, áp suất 760mmHg thì khí Z có thể tích là 13,44 lít. Tính m1, m2. Cho rằng không khí chứa 80% nitơ và 20% oxi về thể tích.
Câu 5.Đốt cháy 13,44 lít khí hiđro (ở đktc) trong bình chứa khí oxi .
a) Viết phương trình hóa học.
b) Tính khối lượng nước tạo thành sau phản ứng trên.
c) Tính thể tích không khí cần dùng cho phản ứng trên. Biết thể tích khí oxi chiếm 1/5 thể tích không khí.
\(n_{H_2}=\dfrac{13,44}{22,4}=0,6mol\)
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\)
0,6 0,3 0,6 ( mol )
\(m_{H_2O}=0,6.18=10,8g\)
\(V_{kk}=V_{O_2}.5=\left(0,3.22,4\right).5=33,6l\)
Đúng 1
Bình luận (0)
Đốt cháy hòa toàn 0,448 lít khí etilen trong không khí ( chứa 20% thể tích oxi ).a. Tính thể tích không khí tham gia phản ứng ( các khí đo ở đktc ).b. Dẫn toàn bộ khí cacbonic qua bình đựng dung dịch nưới vôi trong dư. Tính khối lượng kết tùa thu được.Biết ( H 1 ; C 12 ; O 16 ; Ca 40 ) ( Chú ý: Vkhôngkhí 5 . VO2 ).
Đọc tiếp
Đốt cháy hòa toàn 0,448 lít khí etilen trong không khí ( chứa 20% thể tích oxi ).
a. Tính thể tích không khí tham gia phản ứng ( các khí đo ở đktc ).
b. Dẫn toàn bộ khí cacbonic qua bình đựng dung dịch nưới vôi trong dư. Tính khối lượng kết tùa thu được.
Biết ( H = 1 ; C = 12 ; O = 16 ; Ca = 40 ) ( Chú ý: Vkhôngkhí = 5 . VO2 ).
Câu 1: Để đốt cháy hoàn toàn 6,72 lít khí Etilen:
a) Cần dùng bao nhiêu lít khí oxi ?
b) Bao nhiêu lít không khí ? (biết không khí có chứa 20% thể tích khí oxi)
C2H4 + 3 O2 => 2 CO2 + 2 H2O
nC2H4 = V/22,4 = 6,72/22,4 = 0,3 mol
nO2 phản ứng = 3nC2H4 = 0,9 mol
=> VO2 phản ứng = 0,9 . 22,4 = 20,16 lít
Vkk= 5VO2 = 20.16*5=100.8(l)
Đúng 3
Bình luận (0)
C2H4 + 3 O2 => 2 CO2 + 2 H2O
nC2H4 = V/22,4 = 6,72/22,4 = 0,3 mol
nO2 phản ứng = 3nC2H4 = 0,9 mol
=> VO2 phản ứng = 0,9 . 22,4 = 20,16 lít
Vkk= 5VO2 = 20.16*5=100.8(l)
Đúng 0
Bình luận (1)
Câu 8: Để đốt cháy 1 kg than có chứa 85% C, 10% S còn lại là tạp chất không cháy, thì:
a- Cần dùng hết bao nhiêu lít khí oxi đktc? Bao nhiêu lít kk
b- Tính thể tích khí CO 2 thu được trong không khí sau phản ứng, biết trong không khí trước
phản ứng có 78% khí nito, 20 % khí oxi, 2% khí cacbonic?( giả thiết phản úng xảy ra
trong bình không khí kín)
Bạn tham khảo tại đây nhé
https://sites.google.com/site/hoahocquan10/bai-tap/bai-tap-hoa-8/hoa-8-chuong-iv
Đúng 0
Bình luận (0)