Dựa vào Bảng 2.1, hãy lập tỉ lệ khối lượng của một proton với khối lượng của một electron. Kết quả này nói lên điều gì?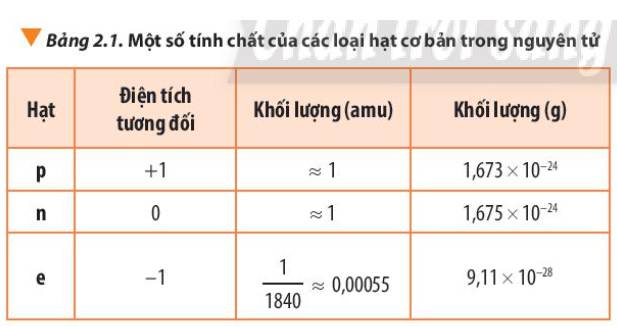

Những câu hỏi liên quan
Bài 5. Dựa vào bảng khối lượng của proton, nơtron và electron hãy tính khối lượng tuyệt đối của
các nguyên tử và tính khối lượng tuyệt đối sau:
a) 1 nguyên tử natri (gồm 11 proton, 12 nơtron và 11 electron)
b) 1 nguyên tử argon (gồm 18 proton, 22 nơtron, 18 electron)
Bài 5. Dựa vào bảng khối lượng của proton, nơtron và electron hãy tính khối lượng tuyệt đối củacác nguyên tử và tính khối lượng tuyệt đối sau:a) 1 nguyên tử natri (gồm 11 proton, 12 nơtron và 11 electron)b) 1 nguyên tử argon (gồm 18 proton, 22 nơtron, 18 electron)Bài 6. Tính tổng điện tích của các proton và tổng điện tích các electron trong nguyên tử oxi và chonhận xét, biết nguyên tử oxi có 8 hạt proton.
Đọc tiếp
Bài 5. Dựa vào bảng khối lượng của proton, nơtron và electron hãy tính khối lượng tuyệt đối của
các nguyên tử và tính khối lượng tuyệt đối sau:
a) 1 nguyên tử natri (gồm 11 proton, 12 nơtron và 11 electron)
b) 1 nguyên tử argon (gồm 18 proton, 22 nơtron, 18 electron)
Bài 6. Tính tổng điện tích của các proton và tổng điện tích các electron trong nguyên tử oxi và cho
nhận xét, biết nguyên tử oxi có 8 hạt proton.
Câu 4. Nguyên tử Cacbon có 6 proton, 6 nơtron và 6 electron.
a) Tính khối lượng các electron trong nguyên tử và khối lượng nguyên tử?
b) Tính tỉ số khối lượng của electron trong nguyên tử so với khối lượng của toàn nguyên tử.
c) Từ kết quả đó coi khối lượng nguyên tử thực tế bằng khối lượng hạt nhân được không?
dựa vào bảng 1.1/SGK trang 14 ,nêu nhận xét ,so sánh khối lượng của các hạt proton ,neutron ,electron ?Từ đó rút ra nhận xét về khối lượng nguyên tử
\(\dfrac{m_{proton}}{m_{electron}}\simeq1840\)
=>Khối lượng electron không đáng kể so với khối lượng proton và nơ trôn
=>Khối lượng nguyên tử gần bằng khối lượng hạt nhân
Đúng 0
Bình luận (0)
Các nguyên tử đều trung hòa về điện. Dựa vào bảng 2.1, em hãy lập luận để chứng minh rằng: Trong một nguyên tử, số proton và số electron luôn bằng nhau.

Giả sử trong một nguyên tử bất kì:
- Có x hạt proton, mỗi hạt proton có điện tích +1.
⇒ Tổng số điện tích dương là +x
- Có y hạt electron, mỗi hạt electron có điện tích -1
⇒ Tổng số điện tích âm là –y.
Nguyên tử trung hòa về điện nên: tổng số điện tích dương + tổng số điện tích âm = 0
⇒ (+x) + (-y) = 0 ⇔ x = y
Vậy trong một nguyên tử bất kì số proton và số electron luôn bằng nhau.
Đúng 0
Bình luận (0)
Một nguyên tử có Z hạt proton, Z hạt electron và N hạt neutron. Tính khối lượng (gần đúng theo amu) và số khối của nguyên tử này. Nhận xét về kết quả thu được.
Ta có:
+ Khối lượng nguyên tử = số proton + số neutron + số electron. 0,00055 = Z + N + 0,00055.Z ≈ Z + N
+ Số khối nguyên tử = số proton + số neutron = Z + N
Như vật khối lượng (gần đúng, theo amu) và số khối của nguyên tử có thể coi là bằng nhau.
Đúng 0
Bình luận (0)
a) Hãy tính khối lượng của nguyên tử nito (gồm 7 proton, 7 notron, 7 electron)
b) Tính tỉ số khối lượng của electron trong nguyên tử so với khối lượng của toàn nguyên tử
a)
$m_N = 7.1,67.10^{-27} + 7.1,67.10^{-27} + 7.9,1.10^{-31} = 2,339.10^{-26}(kg)$
b)
\(\dfrac{m_e}{m_{Ngtu}}=\dfrac{7.9,1.10^{-31}}{2,339.10^{-36}}=2,82.10^{-4}\)
Đúng 2
Bình luận (0)
a.
Khối lượng của electron: \(7\cdot9.1\cdot10^{-28}=63.7\cdot10^{-28}\left(g\right)\)
Khối lượng của proton: \(7\cdot1.67\cdot10^{-24}=11.6\cdot10^{-24}\left(g\right)\)
Khối lượng của nơtron : \(7\cdot1.675\cdot10^{-24}=11.72\cdot10^{-24}\left(g\right)\)
Khối lượng của nguyên tử nitơ là : \(23.42\cdot10^{-24}\left(g\right)\)
b.
\(\dfrac{63.7\cdot10^{-28}}{23.42\cdot10^{-24}}\cdot100\%=0.027\%\)
Đúng 0
Bình luận (2)
Cho biết: \(m_e=9,1095.10^{-31kg}\)
\(m_p=1,6726.10^{-27kg}\)
\(m_n=1,6750.10^{-27kg}\)
Tính khối lượng theo kg của một nguyên tử cacbon gồm 6 proton, 6 nơtron, 6 electron. Tính tỉ số khối của electron so với khối lượng của toàn nguyên tử
Tính khối lượng theo kg của một nguyên tử cacbon gồm 6 proton, 6 nơtron, 6 electron.
m = 6.me+6mp+6mn
= 6.9,1095.10−31 + 6.1,6726.10−27+ 6.1,6750.10−27
=2.10-26 (kg)
Tính tỉ số khối của electron so với khối lượng của toàn nguyên tử
\(\%m_e=\dfrac{6.9,1095.10^{-31}}{2.10^{-26}}.100=0,027\%\)
Đúng 3
Bình luận (0)
a. Tính khối lượng theo gam của một nguyên tử cacbon gồm: 6 proton, 6 electron và 6 nơtron
b. Tính tỉ số khối lượng electron so với khối lượng của toàn nguyên tử
Đúng 0
Bình luận (0)
















