Lấy 1 lượng vừa đủ nhôm oxit tác dụng với 300ml H2SO4 0,5M
a)Khối lượng nhôm oxit đã phản ứng
b)Khối lượng muối đã tạo thành
c) Cũng lượng oxit nhôm trên cần bao nhiêu ml 3M
cho một lượng nhôm oxit tác dụng vừa đủ với 300 ml dd axit sunfuric 4,9 % (d = 1,08)
a tính khối lượng nhôm oxit cần dùng để tác dụng hết với lượng axit đã cho
b tính số g muối thu được sau phản ứng
Nhôm (III) oxit tác dụng với axit sunfuric theo phương trình phản ứng sau :
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Tính lượng muối nhôm sunfat được tạo thành nếu đã sử dụng 49g axit sunfuric nguyên chất tác dụng với 60g nhôm oxit. Sau phản ứng chất nào còn dư ? Lượng dư của chất đó là bao nhiêu ?
Phương trình hóa học của phản ứng:
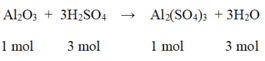
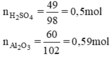
So sánh tỉ lệ 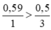 → Vậy Al2O3 dư
→ Vậy Al2O3 dư
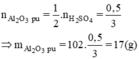
mAl2O3 (dư) = 60 - 17 = 43(g)
b. Cho axit sunfuric (H2SO4) phản ứng vừa hết với 20,4 gam nhôm oxit (Al2O3); tạo ra Al2(SO4)3 và nước. Tính khối lượng H2SO4 đã phản ứng và khối lượng muối (Al2(SO4)3) thu được
\(n_{Al2O3}=\dfrac{20,4}{102}=0,2\left(mol\right)\)
Pt : \(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O|\)
1 3 1 3
0,2 0,6 0,2
\(n_{H2SO4}=\dfrac{0,2.3}{1}=0,6\left(mol\right)\)
⇒ \(m_{H2SO4}=0,6.98=58,8\left(g\right)\)
\(n_{Al2\left(SO4\right)3}=\dfrac{0,6.1}{3}=0,2\left(mol\right)\)
⇒ \(m_{Al2\left(SO4\right)3}=0,2.342=68,4\left(g\right)\)
Chúc bạn học tốt
cho 5,4 g nhôm tác dụng vừa đủ với khí oxi thu được nhôm oxit theo phương trình hóa học sau :4Al+3O2->2Al2O3
a) tính khối lượng nhôm oxit (Al2O3) tạo thành
b)tính thể tích khí oxi(đktc) tham gia phản ứng
Làm gộp cả phần a và b
Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{O_2}=0,15mol\\n_{Al_2O_3}=0,1mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{O_2}=0,15\cdot22,4=3,36\left(l\right)\\m_{Al_2O_3}=0,1\cdot102=10,2\left(g\right)\end{matrix}\right.\)
Cho Al phản ứng vừa đủ vơí 6.72 lít khí O2 ở đktc. Sau phản ứng thu đc oxit nhôm Al2O3. Tính khối lượng nhôm tham gia? Tính khôí lượng oxit nhôm tạo thành?
nO2 = 6.72/22.4 = 0.3 (mol)
4Al + 3O2 -to-> 2Al2O3
0.4___0.3_______0.2
mAl = 0.4*27 = 10.8 (g)
mAl2O3 = 0.2*102 = 20.4 (g)
Hoà tan nhôm oxit vào 200ml dung dịch h2so4 9,8% có D=1,5g/ml thu được nhôm sunfat và nước.Hãy tính a,Khối lượng nhôm oxit tham gia phản ứng b,Khối lượng nhôm sunfat tạo thành sau pứ Nếu được mọi người ghi rõ công thức ra cho mình với
Ta có: m dd H2SO4 = D.V = 1,5.200 = 300 (g)
\(\Rightarrow m_{H_2SO_4}=m_{ddH_2SO_4}.C\%=300.9,8\%=29,4\left(g\right)\)
\(\Rightarrow n_{H_2SO_4}=\dfrac{m}{M}=\dfrac{29,4}{98}=0,3\left(mol\right)\)
PT: \(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
_____0,1_______0,3______0,1 (mol)
a, \(m_{Al_2O_3}=n.M=0,1.102=10,2\left(g\right)\)
b, \(m_{Al_2\left(SO_4\right)_3}=n.M=0,1.342=34,2\left(g\right)\)
Bạn tham khảo nhé!
Bài 2: Cho nhôm tác dụng với oxi tạo thành 40,8 g nhôm oxit Al2O3. a.Viết PTHH của phản ứng xảy ra.b.Tính khối lượng nhôm đã tham gia phản ứng.c.Tính thể tích (ở đktc) của khí oxi đã phản ứng. Giúp mình với
\(a,PTHH:4Al+3O_2\rightarrow^{t^o}2Al_2O_3\\ b,n_{Al_2O_3}=\dfrac{40,8}{102}=0,4\left(mol\right)\\ \Rightarrow n_{Al}=2n_{Al_2O_3}=0,8\left(mol\right)\\ \Rightarrow m_{Al}=0,8\cdot27=21,6\left(g\right)\\ b,n_{O_2}=\dfrac{3}{2}n_{Al_2O_3}=0,6\left(mol\right)\\ \Rightarrow V_{O_2\left(đktc\right)}=0,6\cdot22,4=13,44\left(l\right)\)
1) Cho 15,3 gam nhôm oxit tác dụng vừa đủ với m gam dung dịch axit clohiđric 20% a. Tìm giá trị m =? b. Tính khối lượng dung dịch thu được sau phản ứng? c. Tính C% của muối thu được? 2) Cho m gam nhôm oxit tác dụng vừa đủ với 54,75 gam dung dịch axit clohiđric 20% a. Tìm giá trị m=? b. Tính C% của muối thu được?
1)
a, \(n_{Al}=\dfrac{15,3}{102}=0,15\left(mol\right)\)
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
Mol: 0,15 0,9 0,3
\(m_{ddHCl}=\dfrac{0,9.36,5.100}{20}=164,25\left(g\right)\)
b, mdd sau pứ = 15,3 + 164,25 = 179,55 (g)
c, \(C\%_{ddAlCl_3}=\dfrac{0,3.133,5.100\%}{179,55}=22,31\%\)
2)
a, \(m_{HCl}=54,75.20\%=10,95\left(g\right)\Rightarrow n_{HCl}=\dfrac{10,95}{36,5}=0,3\left(mol\right)\)
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
Mol: 0,05 0,3 0,1
\(m_{Al_2O_3}=0,05.102=5,1\left(g\right)\)
b, mdd sau pứ = 5,1 + 54,75 = 59,85 (g)
\(C\%_{ddAlCl_3}=\dfrac{0,1.133,5.100\%}{59,85}=22,31\%\)
a/ PTHH
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
b/
Ta có: \(n_{Al_2O_3}=\dfrac{10.2}{102}=0.1\left(mol\right)\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
4 2
x 0.1
\(=>x=\dfrac{0.1\cdot4}{2}=0.2=n_{Al}\)
\(=>m_{Al}=0.2\cdot27=5.4\left(g\right)\)
Bài 1: Cho 5,4 gam Nhôm tác dụng hoàn toàn với khí oxi thu được nhôm oxit. Tính thể tích khí oxi đã phản ứng và khối lượng Nhôm oxit thu được
$n_{Al} = \dfrac{5,4}{27} = 0,2(mol)$
\(4Al+3O_2\xrightarrow[]{t^o}2Al_2O_3\)
0,2 0,15 0,1 (mol)
$V_{O_2} = 0,15.22,4 = 3,36(lít)$
$m_{Al_2O_3} =0,1.102 = 10,2(gam)$