Tính thể tích khí oxi (đktc) cần dùng để đốt cháy 9g Cacbon.

Những câu hỏi liên quan
Tính thể tích khí oxi ở đktc cần dùng để đốt cháy hết 24g than (cacbon)
\(n_C=\dfrac{24}{12}=2\left(mol\right)\)
Pt : \(C+O_2\underrightarrow{t_o}CO_2|\)
1 1 1
2 2
\(n_{O2}=\dfrac{2.1}{1}=2\left(mol\right)\)
\(V_{O2\left(dktc\right)}2.22,4=44,8\left(l\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 14,4 g cacbon trong bình đựng khí oxi .
a)Tính thể tích khí oxi cần dùng ( đktc) ?
b)Nếu đốt hoàn toàn lượng cacbon trên trong không khí thì thể tích không khí ( đktc) cần dùng
là bao nhiêu ?
c)Tính khối lượng KClO 3 bị nung nóng để thu được lượng oxi cần cho phản ứng trên, biết
trong quá trình thu khí có hao hụt 20% ?
\(n_C=\dfrac{14,4}{44}=\dfrac{18}{55}\left(mol\right)\\ C+O_2\rightarrow\left(t^o\right)CO_2\\ n_{O_2}=n_C=n_{CO_2}=\dfrac{18}{55}\left(mol\right)\\ a,V_{O_2\left(đktc\right)}=\dfrac{18}{55}.22,4=\dfrac{2016}{275}\left(lít\right)\\ b,V_{kk}=\dfrac{100}{21}.\dfrac{2016}{275}=\dfrac{381}{11}\left(lít\right)\\ c,2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\\ n_{KClO_3\left(LT\right)}=\dfrac{2}{3}.n_{O_2}=\dfrac{2}{3}.\dfrac{18}{55}=\dfrac{12}{55}\left(mol\right)\\ \Rightarrow n_{KClO_3\left(TT\right)}=120\%.\dfrac{12}{55}=\dfrac{72}{275}\left(mol\right)\\ \Rightarrow m_{KClO_3}=122,5.\dfrac{72}{275}=\dfrac{1764}{55}\left(g\right)\)
Đúng 3
Bình luận (0)
3: Tính thể tích Bài khí oxi ở đktc cần dùng để đốt cháy hết 24g than (Cacbon)?
\(n_C=\dfrac{24}{12}=2\left(mol\right)\\ C+O_2\underrightarrow{^{to}}CO_2\\ n_{O_2}=n_C=2\left(mol\right)\\ V_{O_2\left(đktc\right)}=2.22,4=4,48\left(l\right)\)
Đúng 1
Bình luận (0)
Hãy tìm thể tích khí oxi(đktc) cần dùng để đốt cháy hoàn toàn 24 g cacbon
tham khảo tại đây nka bn: https://hoc24.vn/cau-hoi/tinh-the-tich-khi-oxi-o-dktc-can-dung-de-dot-chay-het-24g-than-cacbon.1857970648802
Đúng 1
Bình luận (0)
C + \(O_2\) ➙ \(CO_2\)
Số mol của Cacbon là: \(n_C\) = \(\dfrac{24}{12}\) = 2 (mol)
Số mol của Oxi là: \(n_{O_2}\) = \(n_C\) = 2 (mol)
Thể tích Oxi cần dùng là: V = \(n_{O_2}\) x 22,4 = 44,8 (l)
Đúng 0
Bình luận (0)
\(TH1:n_C=\dfrac{m}{M}=\dfrac{24}{12}=2\left(mol\right)\\ PTHH:O_2+C\underrightarrow{t^o}CO_2\\ Theo.PTHH\Rightarrow n_{O_2}=n_C=2\left(mol\right)\\ V_{O_2\left(dktc\right)}=n.22,4=2.22,4=44,8\left(l\right)\)
\(TH2:n_C=\dfrac{m}{M}=\dfrac{24}{12}=2\left(mol\right)\\ PTHH:O_2+2C\underrightarrow{t^o}2CO\\ Theo.PTHH:n_{O_2}=\dfrac{1}{2}n_C=\dfrac{1}{2}.2=1\left(mol\right)\\ V_{O_2\left(dktc\right)}=n.22,4=1.22,4=22,4\left(l\right)\)
Đúng 0
Bình luận (4)
Thể tích không khí cần dùng là bao nhiêu để đốt cháy hoàn toàn 18g cacbon.( Biết khí oxi chiếm \(\dfrac{1}{5}\) thể tích không khí). Tính thể tích CO2 tạo thành( ở đktc)
C+O2-to>CO2
1,5--1,5 -----1,5mol
n C=\(\dfrac{18}{12}\)=1,5 mol
=>Vkk=1,5.22,4.5=168l
=>VCO2=1,5.22,4=33,6l
Đúng 2
Bình luận (0)
nC = 18/12 = 1,5 (mol)
PTHH: C + O2 -> (t°) CO2
Mol: 1,5 ---> 1,5 ---> 1,5
VO2 = 1,5 . 22,4 = 33,6 (l)
Vkk = 33,6 . 5 = 168 (l)
VCO2 = 1,5 . 22,4 = 33,6 (l)
Đúng 0
Bình luận (0)
Tính thể tích khí oxi và thể tích không khí (đktc) cần thiết để đốt cháy: 1mol cacbon
Cho biết oxi chiếm 20% thể tích không khí.
Phương trình phản ứng khi đốt cháy cacbon:
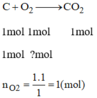
V O 2 = n O 2 .22,4 = 1.22,4 = 22,4(l)
→ V k k = 5 V O 2 = 5.22,4 = 112(l)
Đúng 0
Bình luận (0)
đốt cháy hoàn toàn 1,12dm3(đktc)khí axeliten C2H2 trong ko khí
a/tính thể tích khí cacbon dioxit thu được (ở đktc)
b/tính thể tích không khí cần dùng (đktc) biết Oxi chiếm 1/5 thể tích không khí
\(n_{C_2H_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(C_2H_2+\dfrac{5}{2}O_2\underrightarrow{^{^{t^0}}}2CO_2+H_2O\)
\(0.05.......0.125........0.1\)
\(V_{CO_2}=0.1\cdot22.4=2.24\left(l\right)\)
\(V_{kk}=5\cdot V_{O_2}=5\cdot0.125\cdot22.4=14\left(l\right)\)
Đúng 1
Bình luận (0)
Tính thể tích không khí (đktc) cần dùng để đốt cháy hoàn toàn 1 kg than tổ ong chứa 60% cacbon, 0,8% lưu huỳnh và phần còn lại là tạp chất không cháy. Biết oxi chiếm 1/5 thể tích không khí.
PTHH:
C + O2 ---to----> CO2
50.....50.......................................(mol)
S + O2 ----to---> SO2
0,25...0,25 ............................................(mol)
→ (cần dùng) = (50 + 0,25) . 22,4 = 1125,6 (l)
=>Vkk=1125.6.5=5628l
Đúng 0
Bình luận (0)
thể tích không khí tối thiểu (ở đktc, oxi chiếm 80% thể tích không khí) cần dùng để đốt cháy hoàn toàn 24 gam cacbon (tạo khí cacbonic) là bao nhiêu?

























