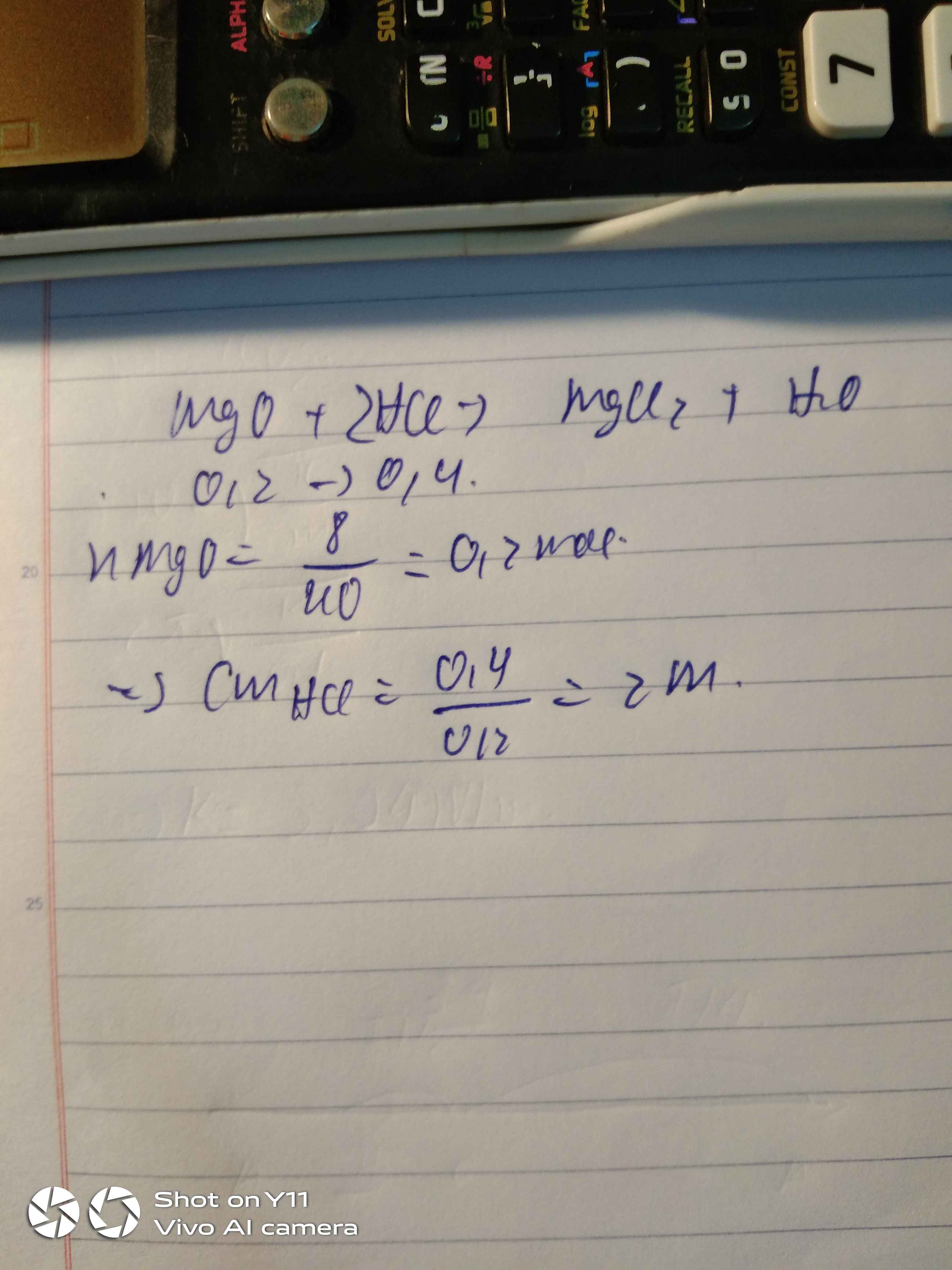Hòa tan hết 5,6 gam Fe cần vừa đủ 200 ml dung dịch HCl . a) Viết phương trình phản ứng . b) Tính nồng độ mol/lít của dung dịch HCl cần dùng .

Những câu hỏi liên quan
Hòa tan 8 gam MgO vào 200 ml dung dịch HCl, phản ứng xảy ra vừa đủ.
a. Viết phương trình phản ứng xảy ra.
b. Tính nồng độ mol của dung dịch HCl cần dùng. ( Mg = 24, O = 16, H =1 , Cl =
35,5)
\(a/\\MgO+2HCl \to MgCl_2+H_2O\\ n_{MgO}=\frac{8}{40}=0,2(mol)\\ b/\\ n_{HCl}=0,2.2=0,4(mol)\\ CM_{HCl}=\frac{0,4}{0,2}=2M\)
Đúng 1
Bình luận (5)
\(n_{MgO}=\dfrac{8}{40}=0,2\left(mol\right)\)
a) Pt : \(MgO+2HCl\rightarrow MgCl_2+H_2O|\)
1 2 1 1
0,2 0,4
b) \(n_{HCl}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
200ml =0,2l
\(C_{M_{ddHCl}}=\dfrac{0,4}{0,2}=2\left(M\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Biết 5,6 lít khí CO2 (đktc) tác dụng vừa hết với 200 ml dung dịch Ca(OH)2, sản phẩm là CaCO3 và H2Oa) Viết phương trình hóa họcb)Tính nồng độ mol của dung dịch Ca(OH)2 đã dùng.c) Tính khối lượng dung dịch HCl 15% cần dùng để trung hòa vừa đủ với lượng Ca(OH)2 ở phản ứng trên.
Đọc tiếp
Biết 5,6 lít khí CO2 (đktc) tác dụng vừa hết với 200 ml dung dịch Ca(OH)2, sản phẩm là CaCO3 và H2O
a) Viết phương trình hóa học
b)Tính nồng độ mol của dung dịch Ca(OH)2 đã dùng.
c) Tính khối lượng dung dịch HCl 15% cần dùng để trung hòa vừa đủ với lượng Ca(OH)2 ở phản ứng trên.![]()
a, \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
b, \(n_{CO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=n_{CO_2}=0,25\left(mol\right)\Rightarrow C_{M_{Ca\left(OH\right)_2}}=\dfrac{0,25}{0,2}=1,25\left(M\right)\)
c, \(Ca\left(OH\right)_2+2HCl\rightarrow CaCl_2+2H_2O\)
Theo PT: \(n_{HCl}=2n_{Ca\left(OH\right)_2}=0,5\left(mol\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{0,5.36,5}{15\%}\approx121,67\left(g\right)\)
Đúng 3
Bình luận (0)
\(n_{CO_2}=\dfrac{5,6}{22,4}=0,25mol\\ a)CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(OH\right)_2+H_2O\)
0,25 0,25 0,25
\(b)C_{M_{Ca\left(OH\right)_2}}=\dfrac{0,25}{0,2}=1,25M\\ c)2HCl+Ca\left(OH\right)_2\rightarrow CaCl_2+2H_2O\\ n_{HCl}=2n_{Ca\left(OH\right)_2}=2.0,25=0,5mol\\ m_{ddHCl}=\dfrac{0,5.36,5}{15\%}\cdot100\%\approx121,67g\)
Đúng 2
Bình luận (0)
1. (1,5 điểm) Hòa tan hết 36,1 gam hỗn hợp A gồm Fe và Al vào 200 mL dung dịch HCl (dùng vừa đủ).
Sau phản ứng thu được dung dịch B và 21,28 lít khí H2 (đktc). Hãy tính:
a. Khối lượng mỗi chất trong hỗn hợp A ban đầu.
b. Tính nồng độ dung dịch HCl đã dùng.
c. Tính nồng độ mol/l của chất tan trong dung dịch B.
a) PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
a_____2a______a_____a (mol)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
b_____3b_______b_____\(\dfrac{3}{2}\)b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}56a+27b=36,1\\a+\dfrac{3}{2}b=\dfrac{21,28}{22,4}=0,95\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,5\\b=0,3\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,5\cdot56=28\left(g\right)\\m_{Al}=8,1\left(g\right)\end{matrix}\right.\)
b+c) Theo các PTHH: \(\left\{{}\begin{matrix}n_{HCl}=2a+3b=1,9\left(mol\right)\\n_{FeCl_2}=0,5\left(mol\right)\\n_{AlCl_3}=0,3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{HCl}}=\dfrac{1,9}{0,2}=9,5\left(M\right)\\C_{M_{FeCl_2}}=\dfrac{0,5}{0,2}=2,5\left(M\right)\\C_{M_{AlCl_3}}=\dfrac{0,3}{0,2}=1,5\left(M\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Hòa tan 6,5 gam kẽm cần vừa đủ Vml dung dịch HCl 1M
a/ Viết phương trình hóa học xảy ra
b/ Tính V
c/ tính nồng độ mol của dung dịch sau phản ứng
\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
a) Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2|\)
1 2 1 1
0,1 0,2 0,1
b) \(n_{HCl}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
\(V_{ddHCl}=\dfrac{0,2}{1}=0,2\left(l\right)\)
c) \(n_{ZnCl2}=\dfrac{0,2.1}{2}=0,1\left(mol\right)\)
\(C_{M_{ZnCl2}}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
Chúc bạn học tốt
Đúng 2
Bình luận (0)
\(a/\\ Zn+2HCl \to ZnCl_2+H_2\\ b/\\ n_{Zn}=0,1(mol)\\ n_{HCl}=0,2(mol)\\ V_{HCl}=\frac{0,2}{1}=0,2(l)\\ c/\\ n_{ZnCl_2}=0,1(mol)\\ CM_{ZnCl_2}=\frac{0,1}{0,2}=0,5M\)
Đúng 0
Bình luận (0)
hòa tan 2,8g Fe trong 100ml dung dích HCL :
a, viết phương trình phản ứng . tính thể tích khi thoát ra .
b, tính nồng độ mol của dung dịch thu được sau phản ứng biết nồng độ mol của dung dịch acid cần dùng là 3 M
\(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)\\ a,PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{H_2}=n_{FeCl_2}=n_{Fe}=0,05\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,05.22,4=1,12\left(l\right)\\ V_{H_2\left(đkc\right)}=0,05.24,79=1,2395\left(l\right)\\ b,n_{HCl}=0,1.3=0,3\left(mol\right)\\ Vì:\dfrac{0,05}{1}< \dfrac{0,3}{2}\Rightarrow HCldư\\ n_{HCl\left(dư\right)}=0,3-0,05.2=0,2\left(mol\right)\\ n_{FeCl_2}=n_{Fe}=0,05\left(mol\right)\\ V_{ddsau}=V_{ddHCl}=0,1\left(l\right)\\ b,C_{MddFeCl_2}=\dfrac{0,05}{0,1}=0,5\left(M\right);C_{MddHCl\left(dư\right)}=\dfrac{0,2}{0,1}=2\left(M\right)\)
Đúng 2
Bình luận (0)
Câu 10. Hòa tan hoàn toàn 8,3 gam hỗn hợp Al và Fe bằng dung dịch HCl 0,2M (vừa đủ), sau phản ứng thu được 5,6 lít khí H2 và dung dịch X.
a. Tính thể tích dung dịch HCl đã dùng.
b. Tính nồng độ mol/l của dung dịch sau phản ứng
\(Đặt:n_{Al}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(m_{hh}=27a+56b=8.3\left(g\right)\left(1\right)\)
\(n_{H_2}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Tathấy:\)
\(n_{HCl}=2n_{H_2}=2\cdot0.25=0.5\left(mol\right)\)
\(V_{ddHCl}=\dfrac{0.5}{0.2}=2.5\left(l\right)\)
\(n_{H_2}=1.5a+b=0.25\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=b=0.1\)
\(C_{M_{AlCl_3}}=\dfrac{0.1}{2.5}=0.04\left(M\right)\)
\(C_{M_{FeCl_2}}=\dfrac{0.1}{2.5}=0.04\left(M\right)\)
Chúc em học tốt !!!
Đúng 3
Bình luận (0)
a, Ta có: \(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
BTNT H, có: \(n_{HCl}=2n_{H_2}=0,5\left(mol\right)\)
\(\Rightarrow V_{HCl}=\dfrac{0,5}{0,2}=2,5\left(l\right)\)
b, Giả sử: \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
⇒ 27x + 56y = 8,3 (1)
Các quá trình:
\(Al^0\rightarrow Al^{+3}+3e\)
x___________ 3x (mol)
\(Fe^0\rightarrow Fe^{+2}+2e\)
y____________2y (mol)
\(2H^++2e\rightarrow H_2^0\)
______0,5__0,25 (mol)
Theo ĐLBT mol e, có: 3x + 2y = 0,5 (2)
Từ (1) và (2) ⇒ x = y = 0,1 (mol)
BTNT Al và Fe, có: \(\left\{{}\begin{matrix}n_{AlCl_3}=n_{Al}=0,1\left(mol\right)\\n_{FeCl_3}=n_{Fe}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow C_{M_{AlCl_3}}=C_{M_{FeCl_3}}=\dfrac{0,1}{2,5}=0,04M\)
Bạn tham khảo nhé!
Đúng 3
Bình luận (2)
Để hòa tan hết 20 gam hỗn hợp CuO và Fe2O3 cần vừa đủ 200 ml dung dịch HCl 3,5M.
a.Tính khối lượng mỗi oxit trong hỗn hợp?
b.Tính nồng độ mol của các chất tan trong dung dịch sau phản ứng?
CuO + 2HCl -> CuCl2 + H2O (1)
Fe2O3 + 6HCl -> 2FeCl3 + 3H2O (2)
nHCl=0,2.3,5=0,7(mol)
Đặt nCuO=a
nFe2O3=b
Ta có hệ:
80a+160b=20
2a+6b=0,7
=>a=0,05;b=0,1
mCuO=80.0,05=4(g)
mFe2O3=20-4=16(g)
Theo PTHH 1 và 2 ta có:
nCuCl2=nCuO=0,05(mol)
nFeCl3=2nFe2O3=0,2(mol)
mCuCl2=135.0,05=6,75(g)
mFeCl3=162,5.0,2=32,5(g)
mdd =20+200.1,1=240(g)
C% dd CuCl2=6,72\240 .100%=2,8125%
C% dd FeCl3= 32,5\240 .100%=13,54%
Đúng 2
Bình luận (0)
Để hòa tan vừa đủ 8g CuO cần 300g dung dịch HCl (vừa đủ) thu được dung dịch A. Cho dung dịch A tác dụng vừa đủ với 200 ml dung dịch KOH tạo ra m (g) kết tủa.a/ Tính C% của dung dịch HCl phản ứng?b/ Tính nồng độ mol của dung dịch KOH và giá trị của m?c/ Lọc lấy kết tủa đem nung, hiệu suất phản ứng nung đạt 95% thì:c1/ Thu được bao nhiêu gam oxit?c2/ Thu được bao nhiêu gam chất rắn sau nung?
Đọc tiếp
Để hòa tan vừa đủ 8g CuO cần 300g dung dịch HCl (vừa đủ) thu được dung dịch A. Cho dung dịch A tác dụng vừa đủ với 200 ml dung dịch KOH tạo ra m (g) kết tủa.
a/ Tính C% của dung dịch HCl phản ứng?
b/ Tính nồng độ mol của dung dịch KOH và giá trị của m?
c/ Lọc lấy kết tủa đem nung, hiệu suất phản ứng nung đạt 95% thì:
c1/ Thu được bao nhiêu gam oxit?
c2/ Thu được bao nhiêu gam chất rắn sau nung?
PTHH: \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
\(CuCl_2+2KOH\rightarrow2KCl+Cu\left(OH\right)_2\downarrow\)
a+b) Ta có: \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
\(\Rightarrow n_{HCl}=0,2\left(mol\right)=n_{KOH}\) \(\Rightarrow\left\{{}\begin{matrix}C\%_{HCl}=\dfrac{0,2\cdot36,5}{300}\cdot100\%\approx2,43\%\\C_{M_{KOH}}=\dfrac{0,2}{0,2}=1\left(M\right)\end{matrix}\right.\)
c) PTHH: \(Cu\left(OH\right)_2\xrightarrow[]{t^o}CuO+H_2O\)
Theo các PTHH: \(n_{CuO\left(lý.thuyết\right)}=n_{Cu\left(OH\right)_2}=n_{Cu}=0,1\left(mol\right)\)
\(\Rightarrow n_{CuO}=0,1\cdot95\%=0,095\left(mol\right)\) \(\Rightarrow m_{CuO}=0,095\cdot80=7,6\left(g\right)\)
Đúng 4
Bình luận (1)