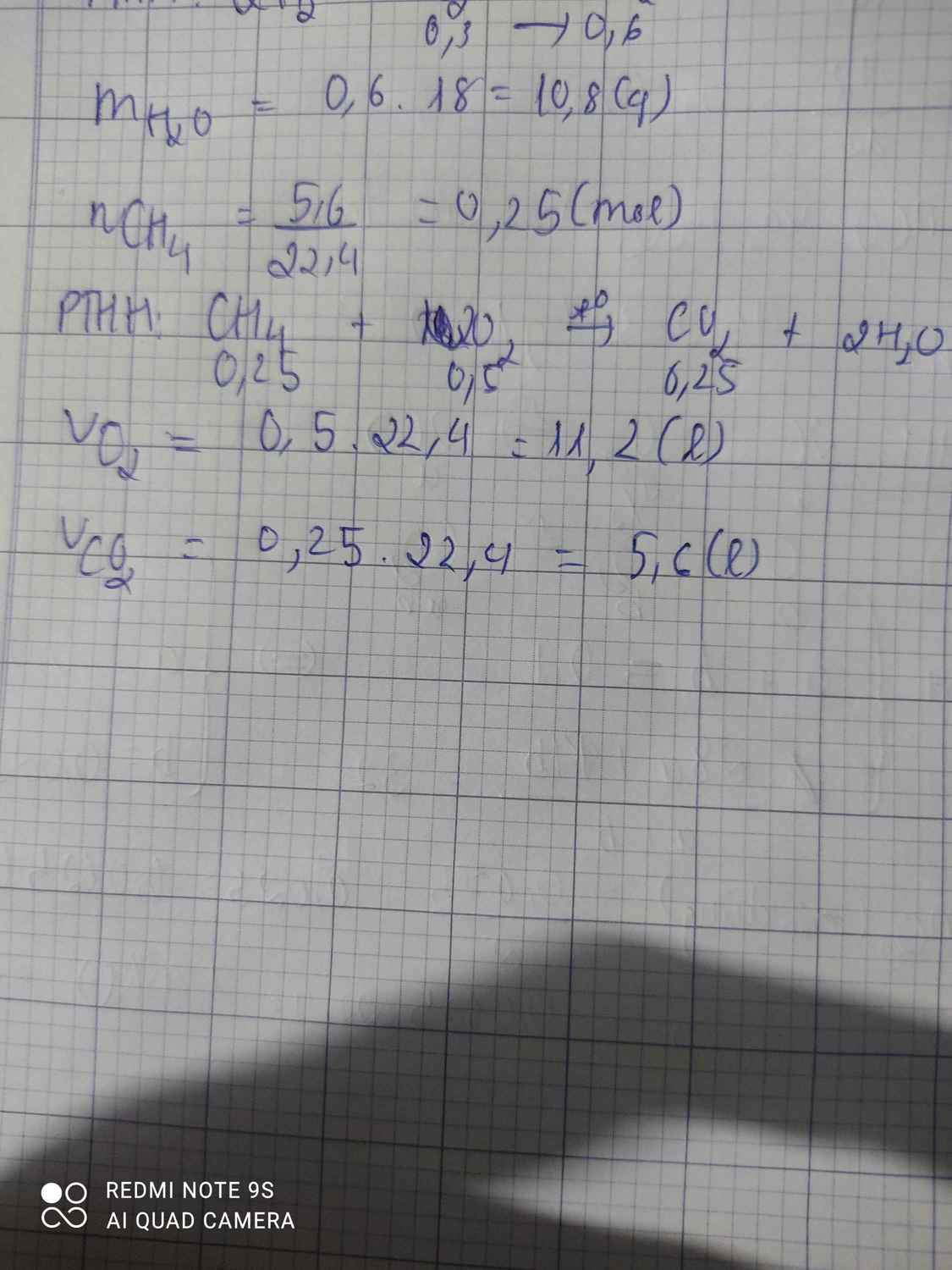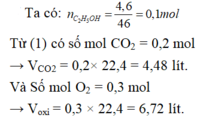Đốt cháy hoàn toàn 4,6 lít C2H5OH trong 224 ml oxi tính thể tích của khí cacbon dioxit tạo thành

Những câu hỏi liên quan
Đốt cháy hoàn toàn 24 gam cacbon trong không khí thu được khí cacbonic .
a. Viết ptpư xảy ra
b. tính khối lượng khí cacbon dioxit tạo thành sau phản ứng
c. tính thể tích không khí cần dùng , biết vo2 = 1/5 v kk
a) C + O2 --to--> CO2
b) \(n_C=\dfrac{24}{12}=2\left(mol\right)\)
=> nCO2 =2 (mol)
=> mCO2 = 2.44 = 88(g)
c)
nO2 = 2(mol)
=> VO2 = 2.22,4 = 44,8 (l)
=> Vkk = 44,8.5=224(l)
Đúng 1
Bình luận (0)
a)
$C + O_2 \xrightarrow{t^o} CO_2$
b)
$n_{CO_2} = n_C = \dfrac{24}{12} = 2(mol)$
$m_{CO_2} = 2.44 = 88(gam)$
c)
$n_{O_2} = n_C = 2(mol)$
$V_{O_2} = 2.22,4 = 44,8(lít)$
$V_{không\ khí} =5 V_{O_2} = 44,8.5 = 224(lít)$
Đúng 2
Bình luận (0)
a: \(C+O_2\rightarrow CO_2\)
b: \(n_C=\dfrac{24}{12}=2\left(mol\right)\)
\(\Leftrightarrow n_{CO_2}=2\left(mol\right)\)
\(\Leftrightarrow m_{CO_2}=2\cdot44=88\left(g\right)\)
Đúng 1
Bình luận (1)
Xem thêm câu trả lời
Đốt cháy hoàn toàn 5,6 lít khí metan hãy tính Thể tích khí oxi cần dùng và thể tích khí cacbon tạo thành biết các thể tích đó ở đktc ( biết C=12, H=1 S=32)
\(n_{CH_4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,25-->0,5-------->0,25
=> \(V_{O_2}=0,5.22,4=11,2\left(l\right)\)
\(V_{CO_2}=0,25.22,4=5,6\left(l\right)\)
Đúng 4
Bình luận (1)
đốt cháy hoàn toàn 1,12dm3(đktc)khí axeliten C2H2 trong ko khí
a/tính thể tích khí cacbon dioxit thu được (ở đktc)
b/tính thể tích không khí cần dùng (đktc) biết Oxi chiếm 1/5 thể tích không khí
\(n_{C_2H_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(C_2H_2+\dfrac{5}{2}O_2\underrightarrow{^{^{t^0}}}2CO_2+H_2O\)
\(0.05.......0.125........0.1\)
\(V_{CO_2}=0.1\cdot22.4=2.24\left(l\right)\)
\(V_{kk}=5\cdot V_{O_2}=5\cdot0.125\cdot22.4=14\left(l\right)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 0.3 mol khí metan ( CH4 ) trong không khí sinh ra 13.2 gam khí cacbon dioxit và 10.8 gam nước. Hãy tính thể tích không khí cần dùng ở đktc? ( Biết rằng khí metan cháy trong không khí là tác dụng với khí oxi. Và oxi chiếm 1/5 thể tích không khí). Giúp mình với:
\(m_{CH_4}=0,3.16=4,8(g)\)
Bảo toàn KL: \(m_{CH_4}+m_{O_2}=m_{CO_2}+m_{H_2O}\)
\(\Rightarrow m_{O_2}=10,8+13,2-4,8=19,2(g)\\ \Rightarrow V_{O_2}=\dfrac{19,2}{32}.22,4=13,44(l)\\ \Rightarrow V_{kk}=13,44.5=67,2(l)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 3,36 lít khí C2H2 trong không khí a,tính thể tích oxi phản ứng b,tính thể tích CO2 tạo thành Các thể tích đo ở đktc
nC2H2 = 3.36/22.4 = 0.15 (mol)
C2H2 + 5/2O2 -to-> 2CO2 + H2O
0.15........0.375...........0.3
VO2 = 0.375*22.4 = 8.4 (l)
VCO2 = 0.3*22.4 = 6.72 (l)
Đúng 1
Bình luận (0)
Để đốt cháy hoàn toàn 2,4g cacbon thành khí cacbon đioxit CO2 cần bao nhiêu lít không khí (đktc ) ? Biết thể tích khí oxi chiếm 1/5 thể tích không khí
nC = 2.4/12 = 0.2 mol
C + O2 -to-> CO2
0.2__0.2
VKK = 5VO2 = 5*0.2*22.4 = 22.4 (l)
Đúng 0
Bình luận (0)
Phản ứng hóa học xảy ra khi đèn cồn cháy (đèn cồn trong phòng thí nghiệm) là:
R
ư
ợ
u
e
t
y
l
i
c
C
2
H
5
O
H
+
o
x
i
−
t
o
→
k
h
í
c
a
c
b
o
n
i
c
C
O...
Đọc tiếp
Phản ứng hóa học xảy ra khi đèn cồn cháy (đèn cồn trong phòng thí nghiệm) là:
R ư ợ u e t y l i c C 2 H 5 O H + o x i − t o → k h í c a c b o n i c C O 2 + n ư ớ c
Tính thể tích oxi cần thiết để đốt cháy hết 4,6 gam rượu etylic và thể tích khí cacbonic tạo thành ở đktc.
Thể tích không khí cần dùng là bao nhiêu để đốt cháy hoàn toàn 18g cacbon.( Biết khí oxi chiếm \(\dfrac{1}{5}\) thể tích không khí). Tính thể tích CO2 tạo thành( ở đktc)
C+O2-to>CO2
1,5--1,5 -----1,5mol
n C=\(\dfrac{18}{12}\)=1,5 mol
=>Vkk=1,5.22,4.5=168l
=>VCO2=1,5.22,4=33,6l
Đúng 2
Bình luận (0)
nC = 18/12 = 1,5 (mol)
PTHH: C + O2 -> (t°) CO2
Mol: 1,5 ---> 1,5 ---> 1,5
VO2 = 1,5 . 22,4 = 33,6 (l)
Vkk = 33,6 . 5 = 168 (l)
VCO2 = 1,5 . 22,4 = 33,6 (l)
Đúng 0
Bình luận (0)
Câu 3: ( 2.5 điểm) Đốt cháy hoàn toàn 11.2 lít khí Etilen . Hãy tính thể tích khí oxi và thể tích khí CO2 tạo thành (đktc).
\(n_{C_2H_4}=\dfrac{11.2}{22.4}=0.5\left(mol\right)\)
\(C_2H_4+3O_2\underrightarrow{^{t^0}}2CO_2+2H_2O\)
\(0.5.......1.5.............1\)
\(V_{O_2}=1.5\cdot22.4=33.6\left(l\right)\)
\(V_{CO_2}=1\cdot22.4=22.4\left(l\right)\)
Đúng 2
Bình luận (0)
\(n_{C_2H_4}=\dfrac{11.2}{22.4}=0.5\left(mol\right)\\ C_2H_4+3O_2->2CO_2+2H_2O\\ =>n_{O_2}=3\cdot0.5=1.5\left(mol\right)\\ =>V_{O2}=1.5\cdot22.4=33.6\left(l\right)\\ n_{CO2}=2\cdot0.5=1\\ =>V_{CO2}=1\cdot22.4=22.4\left(l\right)\)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 2,24 lít khí metan a) viết phương trình hóa học của phản ứng b )tính thể tích khí oxi và thể tích khí cacbonic tạo thành (ở đktc)
\(n_{CH_4}=\dfrac{2,24}{22,4}=0,1mol\)
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
0,1 0,2 0,1
\(V_{O_2}=0,2\cdot22,4=4,48l\)
\(V_{CO_2}=0,1\cdot22,4=2,24l\)
Đúng 2
Bình luận (0)