cho viên natri vào cốc nước thu một dung dịch chứa 16gam a viết phương trình hóa học của phản ứng b tính khối lượng riêng kim loại natri c tính thể tích khí thoát ra ở điều kiện tiêu chuẩn

Những câu hỏi liên quan
một hỗn hợp gôm 4,6g NATRI và 3,9g KALI thả vào một cốc thủy tinh có chứa nước viết phương trình hóa học đọc tên sản phẩm cho biết thuôc loại phản ứng nào tính thể tích H2 thu được ở điều kiện tiêu chuẩn tính khối lượng hỗn hợp BAZơ tạo thành
\(n_{Na}=\dfrac{4.6}{23}=0.2\left(mol\right)\)
\(n_K=\dfrac{3.9}{39}=0.1\left(mol\right)\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\)
\(V_{H_2}=\left(\dfrac{0.2}{2}+\dfrac{0.1}{2}\right)\cdot22.4=3.36\left(l\right)\)
\(m_{bazo}=0.2\cdot40+0.1\cdot56=13.6\left(g\right)\)
Đúng 1
Bình luận (0)
: Cho kim loại Mg vào 140 ml dung dịch H2SO4 1,2M có khí thoát ra.
a) Viết phương trình phản ứng xảy ra.
b) Tính khối lượng kim loại tham gia phản ứng khối lượng muối tạo thành.
c) Tính thể tích khí thu được ở điều kiện tiêu chuẩn.
a) $Mg + H_2SO_4 \to MgSO_4 + H_2$
b)
Theo PTHH : $n_{Mg} = n_{MgSO_4} = n_{H_2SO_4} = 0,14.1,2 = 0,168(mol)$
$m_{Mg} = 0,168.24 = 4,032(gam)$
$m_{MgSO_4} = 0,168.120 = 20,16(gam)$
c)
$n_{H_2} = n_{H_2SO_4} = 0,168(mol)$
$V_{H_2} = 0,168.22,4=3,7632(lít)$
Đúng 2
Bình luận (0)
bạn có thể giải thích cho mik chổ nMg=nMgSO4=nH2SO4=0,14.1,2=0,168(mol) đc ko mik chx hiểu lắm chổ đó
Đúng 0
Bình luận (1)
Cho 21,2 g dung dịch Na2CO3 tác dụng với dung dịch axit HCL sau phản ứng thu được khi thoát ra (điều kiện tiêu chuẩn ) a. Viết phương trình hóa học b. Tính khối lượng axit HCL cần dùng c. Tính thể tích khí thoát ra
a, \(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2+H_2O\)
b,\(n_{Na_2CO_3}=\dfrac{21,2}{106}=0,2\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{Na_2CO_3}=0,4\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
c, \(n_{CO_2}=n_{Na_2CO_3}=0,2\left(mol\right)\)
\(\Rightarrow V_{CO_2}=0,2.22,4=4,48\left(l\right)\)
Đúng 2
Bình luận (0)
cho 2,5 gam nhôm vào bình chứa 0,5 mol dung dịch axit sunfuric loãng
a,Viết phương trình phản ứng
b,chất nào còn dư sau phản ứng Tính khối lượng chất dư
c,Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn
\(n_{Al}=\dfrac{2,5}{27}=\dfrac{25}{270}=\dfrac{5}{54}\left(mol\right)\\ n_{H_2SO_4}=0,5\left(mol\right)\\ a,2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ b,Vì:\dfrac{\dfrac{5}{54}}{2}< \dfrac{0,5}{4}\Rightarrow H_2SO_4dư\\ b,n_{H_2SO_4\left(dư\right)}=0,5-\dfrac{3}{2}.\dfrac{5}{54}=\dfrac{13}{36}\left(mol\right)\\ \Rightarrow m_{H_2SO_4}=\dfrac{13}{36}.98=\dfrac{637}{18}\left(g\right)\\ c,n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.\dfrac{5}{54}=\dfrac{5}{36}\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=\dfrac{5}{36}.22,4=\dfrac{28}{9}\left(l\right)\)
Đúng 5
Bình luận (2)
Tóm tắt:
mAl= 2,5(g)
\(n_{H_2SO_4}=0,5\left(mol\right)\)
---
a) PTHH?
b) Chất dư? m?
c) Thể tích khí sau phản ứng?
Anh ít tóm tắt lắm nên không biết tóm tắt như ri ổn không, vì em cần nên anh tóm tắt ra thử
Đúng 2
Bình luận (1)
cho 2,5 gam nhôm vào bình chứa 0,25 mol dung dịch axit sunfuric loãng a,Viết phương trình phản ứng b,chất nào còn dư sau phản ứng Tính khối lượng chất dư c,Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn
a: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b: \(n_{Al}=\dfrac{2.5}{27}< \dfrac{1}{4}\)
=>H2SO4 dư, Al đủ
\(m_{H_2SO_4}=0.25\cdot98=24.5\left(g\right)\)
c: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{2.5}{54}=\dfrac{5}{108}\left(mol\right)\)
\(\Leftrightarrow n_{H_2}=\dfrac{5}{36}\left(mol\right)\)
\(V_{H_2}=\dfrac{5}{36}\cdot22.4=\dfrac{28}{9}\left(lít\right)\)
Đúng 1
Bình luận (0)
Mình thấy bạn Thịnh tính lượng dư sai
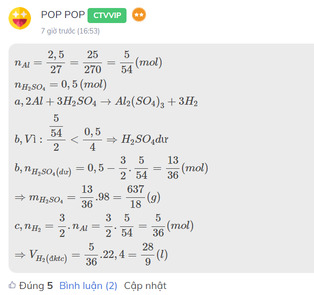
Đây là bài mình từng làm, bạn tham khảo nhé!
Đúng 1
Bình luận (2)
Hòa tan 32,5 gam kẽm vào trong 168,5 gam dung dịch axit sunfuric (vừa đủ) thì thu được một dung dịch muối và có một chất khí thoát ra. a. Viết phương trình hóa học của phản ứngb. Tính khối lượng muối và thể tích khí sinh ra ở điều kiện tiêu chuẩn. c. Tính nồng độ % của dung dịch axit sunfuric đã dùng.giúp mình với mọi người ơicảm ơn rất nhìu
Đọc tiếp
Hòa tan 32,5 gam kẽm vào trong 168,5 gam dung dịch axit sunfuric (vừa đủ) thì thu
được một dung dịch muối và có một chất khí thoát ra.
a. Viết phương trình hóa học của phản ứng
b. Tính khối lượng muối và thể tích khí sinh ra ở điều kiện tiêu chuẩn.
c. Tính nồng độ % của dung dịch axit sunfuric đã dùng.
giúp mình với mọi người ơi
cảm ơn rất nhìu![]()
a) $Zn + H_2SO_4 \to ZnSO_4 + H_2$
b) Theo PTHH :
$n_{H_2} = n_{ZnSO_4} = n_{Zn} = \dfrac{32,5}{65} = 0,5(mol)$
$V_{H_2} = 0,5.22,4 = 11,2(lít)$
$m_{ZnSO_4} = 0,5.161 = 80,5(gam)$
c)
$n_{H_2SO_4} = n_{Zn} = 0,5(mol)$
$C\%_{H_2SO_4} = \dfrac{0,5.98}{168,5}.100\% = 29,08\%$
Đúng 1
Bình luận (0)
Cho 1,3g kẽm (Zn) vào dung dịch HCl .A Viết phương trình hóa học của phản ứng B Tính V thoát ra ở điều kiện tiêu chuẩn C Tính khối lượng axit tham gia đã phản ứng
a) Zn + 2HCl --> ZnCl2 + H2
b) \(n_{Zn}=\dfrac{1,3}{65}=0,02\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,02-->0,04---------->0,02
=> VH2 = 0,02.22,4 = 0,448 (l)
c) mHCl = 0,04.36,5 = 1,46 (g)
Đúng 3
Bình luận (0)
Cho 5,6g Fe vào bình chứa axit HCl a, Viết phương trình hóa học sảy ra b, Tính thể tích khí Hiđro thu được sau phản ứng ở điều kiện tiêu chuẩn c, Nếu cho toàn bộ lượng khí Hiđro thu được ở trên đi qua 4g loại CuO, Tính khối lượng đồng thu được sau phản ứng
Số mol của 5,6g Fe:
\(n_{Fe}=\dfrac{m}{M}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
a,\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
b,thể tích của 0,1 mol H2:
\(V_{H_2}=n.22,4=0,1.22,4=2,24\left(l\right)\)
c,\(H_2+CuO\underrightarrow{t^o}Cu+H_2O\)
khối lượng của 0,1 mol Cu:
\(m_{Cu}=n.M=0,1.64=6,4\left(g\right)\)
Đúng 2
Bình luận (0)
Cho Mg tác dụng vừa đủ với dung dịch có chứa 18,25 g axit HCL a, viết phương trình hóa học xảy ra b, tính khối lượng mg đã dùng và thể tích H thoát ra sau phản ứng c,nên hiệu suất quá trình thu được 90% thì thể tích khí thu được ở điều kiện tiêu chuẩn là bao nhiêu
\(n_{HCl}=\dfrac{18.25}{36.5}=0.5\left(mol\right)\)
\(a.Mg+2HCl\rightarrow MgCl_2+H_2\)
\(b.\)
\(n_{Mg}=n_{H_2}=\dfrac{1}{2}\cdot n_{HCl}=\dfrac{1}{2}\cdot0.5=0.25\left(mol\right)\)
\(m_{Mg}=0.25\cdot24=6\left(g\right)\)
\(V_{H_2}=0.25\cdot22.4=5.6\left(l\right)\)
\(c.\)
\(V_{H_2\left(tt\right)}=5.6\cdot90\%=5.04\left(l\right)\)
Đúng 0
Bình luận (0)