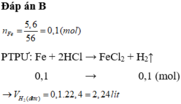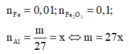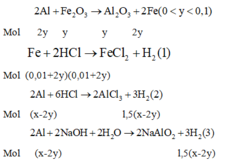Cho 32 gam Fe2O3 tác dụng với 16,8 lít khí H2 thu được Fe ( hiệu suất phản ứng là 80%) cho tác dụng với HCl dư thì được V lít khí H2 dktc. Tìm V?

Những câu hỏi liên quan
cho 1,12 gam fe và 1,6 gam cu tác dụng với dung dịch Hcl dư sau phản ứng thu được v lít khí h2. giá trị của v là
\(n_{Fe}=\dfrac{1,12}{56}=0,02\left(mol\right)\\
n_{Cu}=\dfrac{1,6}{64}=0,025\left(mol\right)\\
pthh:Fe+2HCl\rightarrow FeCl_2+H_2\)
0,02 0,02
\(Cu+HCl\) không phản ứng
\(V_{H_2}=0,02.22,4=0,448l\)
Đúng 6
Bình luận (0)
Fe+2HCl->Fecl2+H2
0,02------------------0,02
=>VH2=0,02.22,4=0,448l
Đúng 4
Bình luận (1)
Trộn 16,8 gam bột Fe với 6,4 gam bột S thu được hỗn hợp X.Nung nóng X một thời gian thu được hỗn hợp rắn Y. Cho Y tác dụng với dung dịc H2SO4 loãng dư thu được V lít(đktc) hỗn hợp khí Z có tỉ khối đối với H2 bằng 9.
a, Tìm giá trị V?
b,Tính hiệu suất phản ứng giữa Fe và S?
H2S:xmol;H2:ymol
ppe:x+y=0.3
nhh=x+y=0.3=>V=6.72l
34x+2y=18*(x+y)
x=0.15;y=0.15
FeS-->H2S
0.15 0.15
Fe+S-->FeS(1)
0.3 0.2 0.2
(1)=>nFeS lt=0.2
H=nFeS tt/nFeS lt *100=75%
Đúng 0
Bình luận (0)
H2S:xmol;H2:ymol
ppe:x+y=0.3
nhh=x+y=0.3=>V=6.72l
34x+2y=18*(x+y)
x=0.15;y=0.15
FeS-->H2S
0.15 0.15
Fe+S-->FeS(1)
0.3 0.2 0.2
(1)=>nFeS lt=0.2
H=nFeS tt/nFeS lt *100=75%
Đúng 0
Bình luận (0)
Cho 16,8 gam Fe vào dung dịch HCl dư sau khi phản ứng xảy ra hoàn toàn thu được V(lít) H2 (ĐKTC)
a. Tính V
b, Nếu dẫn khí H2 trên qua ống nghiệm đựng 20 gam chất rắn Fe2O3 sau khi kết thúc phản ứng thu được 16,4 gam chất rắn. Tính hiệu suất phản ứng?
(Làm 3 cách )
Nhiệt nhôm hỗn hợp A gồm 0,56 gam Fe, 16 gam Fe2O3 và m gam Al được hỗn hợp B. Cho B tác dụng với HCl dư thu được a lít H2. Nếu cho B tác dụng với dung dịch NaOH dư thì được 0,25a lít H2 (các khí ở đktc). Khoảng giá trị của m (gam) là: A. 0,06 m 6,66. B. 0,06 m 1,66 C. 0,6 m 6,66. D. 0,6 m l,66.
Đọc tiếp
Nhiệt nhôm hỗn hợp A gồm 0,56 gam Fe, 16 gam Fe2O3 và m gam Al được hỗn hợp B. Cho B tác dụng với HCl dư thu được a lít H2. Nếu cho B tác dụng với dung dịch NaOH dư thì được 0,25a lít H2 (các khí ở đktc). Khoảng giá trị của m (gam) là:
A. 0,06 < m < 6,66.
B. 0,06 < m < 1,66
C. 0,6 < m <6,66.
D. 0,6 < m < l,66.
Hoà tan hoàn toàn 57,6 gam hỗn hợp X gồm Fe3O4, Fe2O3, FeO và Fe trong dung dịch HCl thì cần dùng 360 gam dung dịch HCl 18,25% để tác dụng vừa đủ. Sau phản ứng thu được V lít khí H2 và dung dịch Y. Cho toàn bộ H2 sinh ra tác dụng hết với 43,2g CuO ở nhiệt độ cao, sau phản ứng thu được 40g rắn. a) cô cạn dung dịch Y thì thu được bao nhiêu gam muối khan ? b) Nếu trong X, nFe2O3=nFeO. tính C% các chất trong Y
Xem chi tiết
a) \(n_{HCl}=\dfrac{360.18,25\%}{36,5}=1,8\left(mol\right)\)
H2 + CuO ------t°----->Cu + H2O
\(n_{CuO}=\dfrac{43,2}{80}=0,54\left(mol\right)\)
Gọi nCuO phản ứng = x (mol)
Theo đề bài
m chất rắn = \(m_{CuO\left(dư\right)}+m_{Cu}=\left(0,54-x\right).80+x.64=40\)
=> x = 0,2 mol
=> n H2 = 0,2 (mol)
=> m H2 = 0,2 . 2 =0,4 (g)
Fe + 2HCl → FeCl2 + H2 (*)
Theo PT : \(n_{HCl}=2n_{H_2}=0,4\left(mol\right)\)
=> Số mol HCl tác dụng với Fe3O4, Fe2O3, FeO là 1,8 - 0,4 = 1,4 mol
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O (1)
Fe2O3 + 6HCl → 2FeCl3 + 3H2O (2)
FeO + 2HCl → FeCl2 + H2O (3)
Bảo toàn nguyên tố H : \(n_{H_2O}.2=n_{HCl}.1\)
\(\Rightarrow n_{H_2O}=\dfrac{1,4}{2}=0,7\left(mol\right)\)
Áp dụng định luật bảo toàn khối lượng, ta có:
mhỗn hợp + mHCl = mmuối + mH2O + mH2
57,6 + 1,8.36,5 = mmuối + 0,7.18 + 0,4
mmuối= a = 57,6 + 65,7 - 12,6 - 0,4 = 110,3 (gam)
Đúng 1
Bình luận (0)
b) Từ PT (*) => \(n_{Fe}=n_{H_2}=0,2\left(mol\right)\)
Nếu trong X, nFe2O3=nFeO
=> Gộp 2 oxit trên thành Fe3O4
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
\(n_{Fe_3O_4}=\dfrac{57,6-0,2.56}{232}=0,2\left(mol\right)\)
\(n_{FeCl_3}=2n_{Fe_3O_4}=0,4\left(mol\right)\)
\(n_{FeCl_2}=n_{Fe_3O_4}=0,2\left(mol\right)\)
\(m_{ddsaupu}=57,6+360-0,4=417,2\left(g\right)\)
=> \(C\%_{FeCl_3}=\dfrac{0,4.162,5}{417,2}.100=15,58\%\)
\(C\%_{FeCl_2}=\dfrac{0,2.127}{417,2}.100=6,09\%\)
Đúng 0
Bình luận (0)
Bài 10. Cho 6,72 lít H2 tác dụng với 4,48 lít Cl2 thu được hỗn hợp khí X. Cho hỗn hợp X tác dụng với dung dịch AgNO3 dư thu được 43,05 gam kết tủa trắng. Tính hiệu suất của phản ứng H2 tác dụng với Cl2?
\(n_{AgCl}=\dfrac{43.05}{143.5}=0.3\left(mol\right)\) \(\Rightarrow n_{HCl}=0.3\left(mol\right)\)
\(n_{HCl}=\dfrac{6.72}{22.4}=0.3\left(mol\right),n_{Cl_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(H_2+Cl_2\underrightarrow{^{^{t^0}}}2HCl\)
\(0.15....0.15.......0.3\)
\(H\%=\dfrac{0.15}{0.2}\cdot100\%=75\%\)
Đúng 2
Bình luận (1)
Cho 6,4 gam Cu và 5,6 gam Fe tác dụng với lượng dư dung dịch HCl. Sau khi phản ứng xảy ra hoàn toàn, thu được V lít khí H2 (đktc). Giá trị của V là A. 5,6 lít B. 4,48 lit C. 2,24 lít D. 3,36 lít
Đọc tiếp
Cho 6,4 gam Cu và 5,6 gam Fe tác dụng với lượng dư dung dịch HCl. Sau khi phản ứng xảy ra hoàn toàn, thu được V lít khí H2 (đktc). Giá trị của V là
A. 5,6 lít
B. 4,48 lit
C. 2,24 lít
D. 3,36 lít
Cho 6,4 gam Cu và 5,6 gam Fe tác dụng với lượng dư dung dịch HCl. Sau khi phản ứng xảy ra hoàn toàn, thu được V lít khí H2 (đktc). Giá trị của V là
A. 5,6 lít.
B. 2,24 lít.
C. 4,48 lit.
D. 3,36 lít.
. cho 1 lít khí H2 và 0,672 lít khí Cl2(dktc) tác dụng với nhau rồi hòa tan sản phẩm vào 38,54g nước ta thu được dung dịch A. Lấy dung dịch A trên cho tác dụng với dung dịch AgNO3 (lấy dư) thu được 7,175g kết tủa. Tính hiệu suất của phản ứng giữa H2 và Cl2
\(n_{H_2}=\dfrac{1}{22,4}=\dfrac{5}{112}\left(mol\right)\)
\(n_{Cl_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: H2 + Cl2 --as--> 2HCl
Xét tỉ lệ: \(\dfrac{\dfrac{5}{112}}{1}>\dfrac{0,03}{1}\) => Hiệu suất tính theo Cl2
\(n_{AgCl}=\dfrac{7,175}{143,5}=0,05\left(mol\right)\)
Bảo toàn Cl: \(n_{Cl_2\left(pư\right)}=0,025\left(mol\right)\)
\(H\%=\dfrac{0,025}{0,03}.100\%=83,33\%\)
Đúng 3
Bình luận (0)