Cho biết 1 mol chất khí ở điều kiện bình thường có thể tích là
A. 2,24 l
B. 0,224 l
C. 22,4 l
D. 22,4 ml
Cho 6,5g Zn phản ứng với dung dịch HCl thấy có khí bay lên với thể tích ở đktc là
A.22,4 (l) B. 0,224 (l) C. 2,24 (l) D. 4,8 (l)
Zn+2HCl->Zncl2+H2
0,1-------------------0,1
n Zn=0,1 mol
=>VH2=0,1.22,4=2,24l
=>C
Trong một bình kín dung tích 20 lít có chứa 4,4 kg khí cacbonic ở nhiệt độ 27 ° C. Tính áp suất của khí trong bình. Biết thể tích của một mol khí ở điều kiện chuẩn là V 0 = 22,4 lít.
Gọi n là số mol khí cacbonic chứa trong bình: n = m/ μ , trong đó M là khối lượng khí cacbonic có trong bình, μ là khối lượng mol của khí cacbonic.
Ta có n = 100 mol
Nếu gọi V 0 là thể tích của lượng khí cacbonic ở điều kiện chuẩn ( p 0 = 1,013. 10 5 Pa; T 0 = 273 K) thì V 0 = n v 0
Áp dụng phương trình trạng thái của khí lí tưởng cho lượng khí cacbonic:
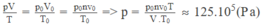
Thể tích của 0,4 mol khí H2 ở đktc là
A.4,48 (l)
B.8,96 (l)
C.22,4 (l)
D.6,72 (l)
Ở cùng điều kiện về nhiệt độ và áp suất, một mol bất kì chất khí nào cũng có thể tích là
A. 22,2 lít. B. 22 lít.
C. 22,4 lít. D. 24,2 lít.
Ở cùng điều kiện về nhiệt độ và áp suất, một mol bất kì chất khí nào cũng có thể tích là
A. 22,2 lít. B. 22 lít.
C. 22,4 lít. D. 24,2 lít.
1 mol N 2 có thể tích bằng 22,4 l. Hỏi 8 mol N 2 thì có thể tích bằng bao nhiêu lít? Biết khí đo ở đktc.
A. 179,2 l
B. 17,92 l
C. 0,1792 l
D. 1,792 l
Đáp án A
V = n.22,4 = 8.22,4 = 179,2 (l)
Thể tích mol chất khí bất kỳ ở điều kiện tiêu chuẩn đều có thể tích là:
A. 24 lít
B. 22,4 lít
C. 6.10 23
D. 6.10 22
Gọi n là số mol bất kì.
\(\Rightarrow V_{hợp.chất.bất.kì}=22,4n\left(lít\right)\)
Không có đáp án
Thể tích ở điều kiện tiêu chuẩn của 12.1023 phân tử SO2 là
A.
4,48 lit
B.
22,4 lit
C.
2,24 lit
D.
44,8 lit
\(n_{SO_2}=\dfrac{12.10^{23}}{6.10^{23}}=2mol\)
\(V_{SO_2}=2.22,4=44,8l\)
=> Đáp án D
Cho 11,2 gam Fe tác dụng 200 ml dưng dịch HCl 1 M. Thể tích khí H2 thu được (đktc) là:
A. 1,12 lít B. 2,24 lít C. 22,4 lít D. 1 lít
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{HCl}=0,2.1=0,2\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,2}{2}\) => HCl hết, Fe dư
PTHH: Fe + 2HCl --> FeCl2 + H2
__________0,2---------------->0,1
=> VH2 = 0,1.22,4 = 2,24(l)
=> B
Phát biểu nào dưới đây là sai?
A. Một mol của của bất kì chất khí nào, trong cùng điều kiện nhiệt độ và áp suất phải chiếm những thể tích bằng nhau. |
B. Thể tích của 1 mol chất khí bất kì luôn có giá trị là 22,4 lít. |
C. Khối lượng mol nguyên tử của một chất là khối lượng tính bằng gam của 6.1023 nguyên tử chất đó. |
D. Thể tích mol của chất khí là thể tích chiếm bởi 6.1023 phân tử chất khí đó |
Chọn B vì thể tích còn phải tùy thuộc vào áp suất và nhiệt độ, phải cùng nhiệt độ và áp suất mới có thể tích bằng nhau