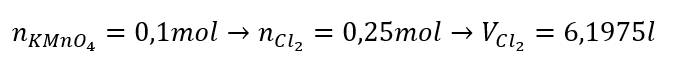Cho 14,2g KMnO4 tác dụng hoàn toàn vs dd HCl đặc dư. Thể tích khí thu được ở đktc là

Những câu hỏi liên quan
Cho a gam kmno4 tác dụng hoàn toàn với dung dịch hcl đặc, dư, thu được 5,6 lít khí ở đktc. Giá trị của a
Xem chi tiết
Khí thoát ra : Cl2 . \(n_{Cl_2} =\dfrac{5,6}{22,4} = 0,25(mol)\)
\(2KMnO_4 + 16HCl \to 2MnCl_2 + 2KCl + 5Cl_2 + 8H_2O\)
Theo PTHH :
\(n_{KMnO_4} = \dfrac{2}{5}n_{Cl_2} = 0,1(mol)\\ m_{KMnO_4} = 0,1.158 = 15,8(gam)\)
Đúng 3
Bình luận (0)
Cho 15.8g KMnO4 tác dụng hoàn toàn với dung dịch HCL đậm đặc . Tính thể tích khí Cl2 thu được ở đkc
\(n_{KMnO_4}=\dfrac{15,8}{158}=0,1\left(mol\right)\\ 2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\\ n_{Cl_2}=\dfrac{5}{2}.0,1=0,25\left(mol\right)\\ V_{Cl_2\left(đkc\right)}=0,25.24,79=6,1975\left(l\right)\)
Đúng 0
Bình luận (0)
Cho 15.8g KMnO4 tác dụng hoàn toàn với dung dịch HCL đậm đặc . Tính thể tích khí Cl2 thu được ở đkc
Nhiệt phân 22,12 gam KMnO4 một thời gian, thu được 21,16 gam hỗn hợp rắn X. Tính thể tích khí clo (đktc) thu được khi cho X tác dụng hoàn toàn với dung dịch HCl đặc, dư .
GIÚP MÌNH VỚI MÌNH ĐANG CẦN GẤP
\(n_{O_2}=\dfrac{22,12-21,16}{32}=0,03\left(mol\right)\)
\(n_{KMnO_4}=\dfrac{22,12}{158}=0,14\left(mol\right)\)
Mn+7 + 5e --> Mn+2
0,14-->0,7
2O-2 - 4e --> O20
0,12<--0,03
2Cl- - 2e --> Cl20
2a<---a
Bảo toàn e: 2a + 0,12 = 0,7
=> a = 0,29 (mol)
=> VCl2 = 0,29.22,4 = 6,496 (l)
Đúng 4
Bình luận (0)
13/ Cho 16,8g sắt tác dụng với dung dịch HCl dư. Tính thể tích khí H2 thu được ở đktc.
14/ Cho 25g CaCO3 vào dung dịch HCl dư. Tính thể tích khí CO2 thu được (ở đktc).
15/ Cho 16 g hỗn hợp hai kim loại Fe và Mg tác dụng hoàn toàn với dung dịch HCl dư, sinh ra 6,72 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu.
\(13,n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\\ PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\\ .....0,3.....0,6......0,3......0,3\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,3\cdot22,4=6,72\left(l\right)\\ 14,n_{CaCO_3}=\dfrac{25}{40+12+16\cdot3}=0,25\left(mol\right)\\ PTHH:CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\\ .....0,25.....0,5......0,25......0,25......0,25\left(mol\right)\\ V_{CO_2\left(đktc\right)}=0,25\cdot22,4=5,6\left(l\right)\)
Đúng 1
Bình luận (0)
cho 14,2 gam KMnO4 tác dụng hoàn toàn với dung dịch HCl đặc, dư.Thể tích khí thu được ở (đktc) là?
giúp dùm mình mình cần gấp tối nay lúc 8h giúp dùm mình
PTHH: \(2KMnO_4+16HCl_{\left(đ\right)}\rightarrow2KCl+2MnCl_2+5Cl_2\uparrow+8H_2O\)
Ta có: \(n_{KMnO_4}=\dfrac{14,2}{158}=\dfrac{71}{790}\left(mol\right)\)
\(\Rightarrow n_{Cl_2}=\dfrac{71}{316}\left(mol\right)\) \(\Rightarrow V_{Cl_2}=\dfrac{71}{316}\cdot22,4\approx5,03\left(l\right)\)
Đúng 2
Bình luận (0)
Cho hỗn hợp gồm 5,6 gam fe và 4,8 gam mg tác dụng hoàn toàn với dd hcl dư sinh ra V lít khí h2(đktc)
a) tính thể tích khí thoát ra ở đktc?
b)tính thể tích dd hcl2m cần dùng?
c)tính khối lượng muối thu được sau phản ứng
\(a)n_{Fe}=\dfrac{5,6}{56}=0,1mol\\ n_{Mg}=\dfrac{4,8}{24}=0,2mol\\ Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,2 0,1 0,1
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2 0,4 0,2 0,2
\(V_{H_2}=\left(0,1+0,2\right).22,4=6,72l\\ b)V_{ddHCl}=\dfrac{0,2+0,4}{2}=0,3l\\ c)m_{muối}=0,1.127+95.0,2=31,7g\)
Đúng 2
Bình luận (0)
Cho hỗn hợp kim loại Zn, Mg, Fe tác dụng hoàn toàn với 400 ml dd HCl 1,5M sau phản ứng thu được khí H2 ở đktc. Thể tích khí H2 thu được ở đktc là: A. 13,44 lít B. 8,96 lít B. 6,72 lít B. 67,2 lít
Đọc tiếp
Cho hỗn hợp kim loại Zn, Mg, Fe tác dụng hoàn toàn với 400 ml dd HCl 1,5M sau phản ứng thu được khí H2 ở đktc. Thể tích khí H2 thu được ở đktc là: A. 13,44 lít B. 8,96 lít B. 6,72 lít B. 67,2 lít
Ta có: \(n_{HCl}=0,4\cdot1,5=0,6\left(mol\right)\)
Bảo toàn Hidro: \(n_{H_2}=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\) \(\Rightarrow V_{H_2}=0,3\cdot22,4=6,72\left(l\right)\)
\(\Rightarrow\) Chọn B
Đúng 2
Bình luận (0)
Cho 15,8g KMnO4 tác dụng với dung dịch HCl đặc, tính thể tích khí Cl2 thu được ở đktc, biết quá trình thu khí Cl2 hao hụt 10 phần trăm
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,1--------------------------------------------------0,25 mol
n KMnO4=\(\dfrac{15,8}{158}\)=0,1 mol
Hao hụt 10%
=>VCl2=0,25.22,4.90%=5,04l
Đúng 1
Bình luận (0)