Đốt cháy hoàn toàn 7,5g hidrocacbon X , ng ta thu đc H2O và 22g CO2 . Tìm CTPT và viết CTCT của X . Bik khối lượng mol của X là 30g/mol

Những câu hỏi liên quan
Đốt cháy hoàn toàn một hidrocacbon X ở thể khí thu được 0,14 mol CO2 và 1,89g H2O. Tìm CTPT và CTCT của X biết X có thể trùng hợp tạo thành cao su?
đốt cháy hoàn toàn 3gr hidrocacbon A thu đc 5.4 gr H2o biết khối lượng mol của A là 30g
a) lập CTPT của A
b) viết CTCT có thể có của A
9. Đốt cháy hoàn toàn 3g hợp chất hữu cơ (X), sau phản ứng thu được 6,6g CO2 và 3,6g H2O. Xác định CTPT, biết khối lượng mol là 60g/mol. Viết CTCT, biết (X) phản ứng được với Na
$n_{CO_2} = \dfrac{6,6}{44} = 0,15(mol)$
$n_{H_2O} = \dfrac{3,6}{18} = 0,2(mol)$
Bảo toàn nguyên tố C, H :
$n_C = n_{CO_2} = 0,15(mol) ; n_H = 2n_{H_2O} = 0,4(mol)$
$\Rightarrow n_O = \dfrac{3 - 0,15.12 - 0,4.1}{16} = 0,05(mol)$
Ta có :
$n_C : n_H : n_O = 0,15 : 0,4 : 0,05 = 3 : 8 : 1$
Vậy CTHH của X là $C_3H_8O$
CTCT thỏa mãn :
$CH_3-CH_2-CH_2-OH$
$CH_3-CH(CH_3)-OH$
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 7,5g 1 hidrocacbon A thu đc 11,2 lít khí CO2(đktc). Biết tỉ khối hơi của 2 h/chất đối vs hidro là 15.Tìm CTPT của A.Viết CTCT của A
\(M_A=15.M_{H_2}=15.2=30\left(\dfrac{g}{mol}\right)\\ Đặt:C_aH_b\left(a,b:nguyên,dương\right)\\ n_C=n_{CO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\ \Rightarrow m_C=0,5.12=6\left(g\right)\\ m_H=7,5-6=1,5\left(g\right)\\ \Rightarrow n_H=\dfrac{1,5}{1}=1,5\left(mol\right)\\ \Rightarrow a:b=0,5:1,5=1:3\\ \Rightarrow CTTQ:\left(CH_3\right)_t\left(t:nguyên,dương\right)\\ \Leftrightarrow15t=30\\ \Leftrightarrow t=2\\ \Rightarrow CTPT:C_2H_6\\ CTCT:CH_3-CH_3\)
Đúng 6
Bình luận (0)
Đốt cháy hoàn toàn một hidrocacbon A. Thu được 13.2g CO2 và 5.4g H2O. Biết khối lượng mol của A là 28g. Hãy xác định CTPT của A
Help me !!!
Ta có: \(n_{CO_2}=\dfrac{13,2}{44}=0,3\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\Rightarrow n_H=0,3.2=0,6\left(mol\right)\)
Giả sử: CTPT của A là CxHy
⇒ x : y = 0,3 : 0,6 = 1 : 2
⇒ CTĐGN của A là (CH2)n
Mà: MA = 28 (g/mol)
\(\Rightarrow n=\dfrac{28}{12+2}=2\)
Vậy: A là C2H4.
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Theo gt ta có: $n_{CO_2}=0,3(mol);n_{H_2O}=0,3(mol)$
Bảo toàn nguyên tố C và H ta có: $n_{A}=0,3.12+0,3.2=4,2(g)$
$\Rightarrow n_{A}=0,15(mol)$
Chia tỉ lệ số mol C và H cho mol A ta tìm được A là $C_2H_4$
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn V lít (đktc) hỗn hợp khí X gồm axetilen, etilen và hidrocacbon Y, thu được số mol CO2 đúng bằng số mol H2O. Nếu dẫn V lít (đktc) hỗn hợp khí X như trên qua lượng dư dung dịch Br2 thấy khối lượng bình đựng tăng 0,82 gam. Khí thoát ra khỏi bình đem đốt cháy hoàn toàn thì thu được 1,32 gam CO2 và 0,72 gam H2O. Công thức phân tử của hidrocacbon Y và giá trị của V là: A. C3H4 và 0,336 B. C3H8 và 0,672. C. C3H8 và 0,896. D. C4H10 và 0,448.
Đọc tiếp
Đốt cháy hoàn toàn V lít (đktc) hỗn hợp khí X gồm axetilen, etilen và hidrocacbon Y, thu được số mol CO2 đúng bằng số mol H2O. Nếu dẫn V lít (đktc) hỗn hợp khí X như trên qua lượng dư dung dịch Br2 thấy khối lượng bình đựng tăng 0,82 gam. Khí thoát ra khỏi bình đem đốt cháy hoàn toàn thì thu được 1,32 gam CO2 và 0,72 gam H2O. Công thức phân tử của hidrocacbon Y và giá trị của V là:
A. C3H4 và 0,336
B. C3H8 và 0,672.
C. C3H8 và 0,896.
D. C4H10 và 0,448.
Đáp án C
Khí thoát ra khỏi bình là Y ; nCO2 = 0,03 ; nH2O= 0,04
→ Y là ankan → nY = 0,04 - 0,03 = 0,01 → Y là C3H8
Đốt cháy X thu được nCO2 = nH2O
→ nC2H2= nC3H8 = 0,01 mol
→ nC2H4 = ( 0,82 - 0,01 × 26 ) : 28 = 0,02 mol
→ nX = 0,01 + 0,02 + 0,01 = 0,04 → VX = 0,896 (l)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 12g một hợp chất hữu cơ X thu được 35,2g CO2 và 21,6g H2O a) xác định CTPT của X biết Mx= 30g b) viết CTCT của X và cho biết X có thể có CTHH nào? viết PTHH minh hoạ
X + O2 -- (t^o) -- > CO2 và H2O
X gồm có C và H
nCO2 = 35,2 : 44 = 0,8 (mol)
-- > nC= 0,8(mol)
nH2O = 21,6 : 18 = 1,2(mol)
--> nH = 1,2 . 2 = 2,4 (mol)
mC= 0,8 . 12 = 9,6(g)
mH = 2,4 . 1 = 2,4(g)
h/c X = mC + mH = 12g = m hh
--> h/c X không có nguyên tử Oxi
Gọi CTHH đơn giản của X là CxHy
ta có : nC : nH = 0,8 : 2,4 = 1 : 3
=> CTĐG giản X là CH3
ta có : (CH3)n = 30
15.n=30
=> n= 2
Vậy CTHH của X là C2H6
CTCT của X là: CH3 - CH3
Đúng 5
Bình luận (0)
Đốt cháy hoàn toàn 7,5g hyđrocácbon A ta thu đc 22g khí CO2 và 13,5g H2O. Biết tỷ khối hơi so vs hyđro bằng 15. lập công thức phân tử của A.
\(n_{CO_2}=\dfrac{22}{44}=0,5\left(mol\right)\)
\(n_{H_2O}=\dfrac{13,5}{18}=0,75\left(mol\right)\)
Bảo toàn C: nC(A) = 0,5 (mol)
Bảo toàn H: nH(A) = 0,75.2 = 1,5 (mol)
Xét nC : nH = 0,5 : 1,5 = 1: 3
=> CTPT: (CH3)n
Mà MA = 15.2 = 30(g/mol)
=> n = 2
=> CTPT: C2H6
Đúng 2
Bình luận (0)
\(2C_2H_6+5O_2\underrightarrow{t^o}4CO_2+6H_2O\)
Đúng 0
Bình luận (0)
Có tỷ khối hơi của \(A\) so với \(H_2\) là \(15\)
\(MA=15.2=30g/mol\)
Có \(nA=\dfrac{7,5}{30}=0,25mol\)
Có \(nCO2=\dfrac{22}{44}=0,5mol\)
Có \(nH20=\dfrac{13,5}{18}=0,75mol\)
Gọi \(CTHH\) chung của \(A\) là \(C_xH_yO_z\)
Ta có PTHH sau:
\(CxHyOz+\left(x+\dfrac{y}{4}-\dfrac{z}{2}\right)O2\overset{t^o}{\rightarrow}xCO2+\dfrac{y}{2}H2O\)
Từ PTHH:
\(+\)) \(x=\dfrac{nCO2}{nA}=\dfrac{0,5}{0,25}=2\)
\(+\)) \(y=\dfrac{2nH2O}{nA}=\dfrac{0,75.2}{0,25}=6\)
\(+\)) \(z=\dfrac{30-\left(12.2\right)-\left(1.6\right)}{16}=0\)
Vì \(z=0\) chứng tỏ trong \(A\) không chứa \(O\)
\(\rightarrow\) Trong \(A\) chỉ chứa \(C,H\)
Vậy CTPT của \(A\) lúc bây giờ là \(C_2H_6\left(Etan\right)\)
Đúng 1
Bình luận (0)
hỗn hợp A gồm một ankan và một anken có tỉ lệ về phân tử khối tương ứng là 11:7. Đốt cháy hoàn toàn 0.2 mol hỗn hợp A thu được 22g co2 và 10,8g h20.Tìm ctpt của X
\(n_{CO_2}=\dfrac{22}{44}=0,5\left(mol\right)\)
\(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\)
Do \(n_{H_2O}>n_{CO_2}\Rightarrow n_{ankan}=0,6-0,5=0,1\left(mol\right)\)
Đặt CT của ankan :\(C_nH_{2n+2}\) 0,1 mol , anken : \(C_mH_{2m}\)0,1 mol
BT C : 0,1n+ 0,1 m=0,5 (1)
Lại có : \(\dfrac{14n+2}{14m}=\dfrac{11}{7}\Leftrightarrow98n-154m=0\left(2\right)\)
(1) , (2) : \(\Rightarrow\left\{{}\begin{matrix}m=3\\n=2\end{matrix}\right.\Rightarrow}\left\{{}\begin{matrix}C_3H_8\\C_2H_4\end{matrix}\right.\)
Đúng 1
Bình luận (0)




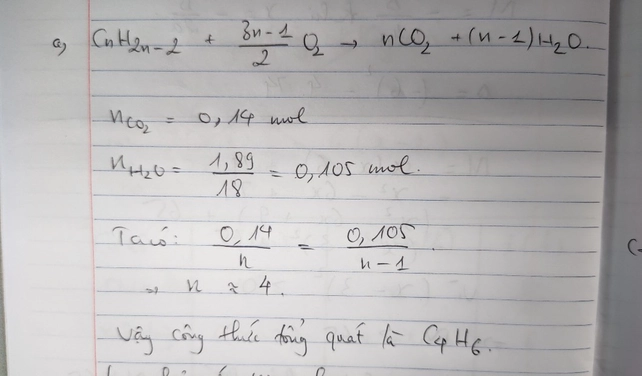
 Bạn tham khảo nhé!
Bạn tham khảo nhé!
























