Tính tỉ lệ phần trăm theo khối lượng các nguyên tố hóa học có trong những hợp chất sau:
a, \(NH_4NO_3\) b, \(Co\left(NH_2\right)_2\) c, \(H_2PO_4\)
Dùng \(Na_2CO_3\) có thể nhận biết được loại phân nào sau đây qua hiện tượng kết tủa trắng?
a. KCl
b. \(NH_4NO_3\)
c. \(Ca\left(H_2PO_4\right)_2\)
d. \(CO\left(NH_2\right)_2\)
\(c.\)
\(Ca\left(H_2PO_4\right)_2+Na_2CO_3\rightarrow CaCO_3\downarrow+2NaH_2PO_4\)
Đáp án C
$Ca(H_2PO_4)_2 + Na_2CO_3 \to CaCO_3 + 2NaH_2PO_4$
$CaCO_3$ là kết tủa trắng
Tính thành phần phần trăm nguyên tố N trong các hợp chất sau :
a) Urê - \(\left(NH_2\right)_2CO\)
b) Amôn nitrat - \(NH_4NO_3\)
Tìm thành phần phần trăm (theo khối lượng) các nguyên tố hóa học có trong những hợp chất sau:
a) CO và CO2.
b) Fe3O4 và Fe2O3.
c) SO2 và SO3.
a) Hợp chất CO có MCO = 12 + 16 = 28 g/mol
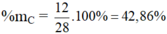
%mO = 100 – 42,86 = 57,14%
Hợp chất CO2: có MCO2 = 12 + 32 = 44 g/mol
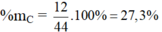
%mO = 100 – 27,3 = 72,7%
b) Hợp chất Fe3O4: MFe3O4 = 3.56 + 4.16 = 232 g/mol
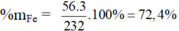
%mO = 100 – 72,4 = 27,6%
Hợp chất Fe2O3: MFe2O3 = 2.56 + 3.16 = 160 g/mol
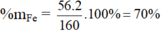
%mO = 100 – 70 = 30%
c) Hợp chất SO2 : MSO2 = 32 + 2.16 = 64 g/mol
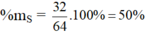
%mO = 100 – 50 = 50%
Hợp chất SO3 : MSO3 = 32 + 16.3 = 80 g/mol
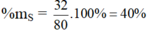
%mO = 100 – 40 = 60%
Tính thành phần phần trăm theo khối lượng các nguyên tố trong hợp chất: \(Ca_3\left(PO_4\right)_2\)
PTKCa3(PO4)2= 3.40+ 95.2=310(đ.v.C)
Ta có:
\(\%mCa=\dfrac{3.40}{310}.100=38,71\%\\ \%mP=\dfrac{31.2}{310}.100=20\%\\ \%mO=100\%-\left(38,71\%+20\%\right)=41,29\%\)
\(CaO:\%^MCa=\dfrac{40}{40+16}\cdot100\%=71,43\%\\ \%^MO=100\%-71,43\%=28,57\%\)
\(MgCO_3:\%^MMg=\dfrac{24}{24+12+16\cdot3}\cdot100\%=28,57\%\\ \%^MC=\dfrac{12}{24+12+16\cdot3}\cdot100\%=14,29\%\\ \%^MO=100\%-28,57\%-14,29\%=57,14\%\)
\(NaOH:\%^MNa=\dfrac{23}{23+16+1}\cdot100\%=57,5\%\\ \%^MO=\dfrac{16}{23+16+1}\cdot100\%=40\%\\ \%^MH=100\%-57,5\%-40\%=2,5\%\)
Nếu sử dụng cùng một khối lượng để bón cho cây thì loại phân đạm nào có hiệu quả hơn?
a. \(CO\left(NH_2\right)_2\)
b. \(NH_4NO_3\)
c. \(\left(NH_4\right)_2SO_4\)
d. \(NH_4Cl\)
\(\%N_{trongCO\left(NH_2\right)_2}=\dfrac{14.2}{60}.100=46,67\%\)
\(\%N_{trongNH_4NO_3}=\dfrac{14}{80}.100=17,5\%\)
\(\%N_{trong\left(NH_4\right)_2SO_4}=\dfrac{14.2}{132}.100=21,21\%\)
\(\%N_{trongNH4Cl}=\dfrac{14}{53,5}.100=26,17\%\)
- Trong 4 loại phân đạm trên, hàm lượng N trong phân CO(NH2)2 là cao nhất nên là loại phân đạm tốt nhất nên được sử dụng nhiều.
=> Chọn A
Một hợp chất có công thức hóa học là K\(_2\)CO\(_3\)
a) Khối lượng mol của chất đã cho
b)Thành phần phần trăm (theo khói lượng)của các nguyên tố có trong hợp chất
a.
M= 39*2 + 12 + 16*4=138 ( g/mol)
b. % K= ( 39*2) *100%;138= 56.52%
% C = 12*100% ; 138= 8.7%
==.> % O = 100% - 8.7% - 56.52% = 34.78%
Một hợp chất có công thức hóa học là K\(^{ }_2\)CO\(_3\).Em hãy cho biết:
a)Khói lượng mol ủa chất đã cho
b)Thành phần trăm(theo khối lượng)của các nguyên tố có trong hợp chất
a) Khối lượng mol của K2CO3 :
MK2CO3 = 39.2 + 12 + 16.3 = 138 (g/mol)
b) nK = 2 mol
nC = 1 mol
nO = 3 mol
Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất là :
mK = 39.2 = 78 (g)
mC = 12.1 = 12 (g)
mO = 16.3 = 48 (g)
Thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất :
\(\%m_K=\frac{m_K}{M_{K2CO3}}.100\%=\frac{78}{138}.100\%=56,5\%\)
\(\%m_C=\frac{m_C}{M_{K2CO3}}.100\%=\frac{12}{138}.100\%=8,7\%\)
\(\%m_O=\frac{m_O}{M_{K2CO3}}.100\%=\frac{48}{138}.100\%=34,8\%\)
a) khối lượng mol của chất đã cho là :
M K2CO3 = \(39\cdot2+12+16\cdot3\)= 138 g/mol ( đây là của 1 mol K2CO3 nhé)
b)
%m K = 39*2/138*100% ~~ 56%
%m C = 12/138*100% ~~ 8%
%m O= 100%-56%-8% ~~ 36%
1. Không tính tỉ lệ phần trăm, hãy lập luận, sắp xếp các chất sau theo hàm lượng kali giảm dần: KMnO4, KClO3, KNO3, KOH, KI.
2. Không tính tỉ lệ phần trăm, hãy lập luận, sắp xếp các chất sau theo hàm lượng nito giảm dần: \(N_2O_5;NO_2;N_2O;N_2O_3;NO\)
3. Không tính tỉ lệ phần trăm, hãy lập luận, sắp xếp các chất sau theo hàm lượng kali giảm dần: KClO3, KHCO3,KI,
KCl, \(KHSO_4\)
4. Cho các chất sau: \(Ca\left(NO_3\right)_2;NH_4NO_3;\left(NH_4\right)_2SO_4;\left(NH_2\right)_2CO\) , hãy lập luận để sắp xếp các trên theo hàm lượng đạm giảm dần.